题目
2015年32题(16分):下图是钠铊合金的立方晶系晶胞图,晶胞参数为a=7.488Å(1 Å =10—10 m)。a-|||-Na-|||-TI-|||-bigcirc Na 9 Tl(1)试写出该合金的化学式。(2)试计算该晶体的密度(保留三位有效数字)。(3)试写出该晶体的结构基元的化学式,并画出结构基元围成的最小几何构型。写出几何构型中Na、Tl原子的分数坐标。(4)若把Na原子看作密堆积,其它Na、Tl原子占有密堆积Na原子围成的何类空隙以及空隙占有率分别是多少?(5)若把一类金属原子全部抽掉,剩下的金属原子属于什么晶型?(6)该晶体属于何类点阵型式?《晶体结构》全国初赛题(4)2018年第4题(12分):4-1利用双离子交换膜 电解法可以从含硝酸铵的工业废水中生产硝酸和氨。4-1-1 阳极室得到的是哪种物质?写出阳极半反应方程式。4-1-2 阴极室得到的是哪种物质?写出阴极半反应及获得相应物质的方程式。4-2 电解乙酸钠水溶液,在阳极收集到X和Y的混合气体。气体通过新制的澄清石灰水,X被完全吸收,得到白色沉淀。纯净的气体Y冷却到90.23K,析出无色晶体,X-射线衍射表明,该晶体属立方晶系,体心立方点阵,晶胞参数a=530.4 pm,Z=2,密度ρ=0.669 g/cm3。继续冷却,晶体转化为单斜晶系,a=422.6 pm,b=562.3 pm,c=584.5 pm,β=90.41°。4-2-1 写出X的化学式;写出X和石灰水反应的方程式。4-2-2 通过计算推出Y的化学式(Y分子中存在三次旋转轴)。4-2-3 写出电解乙酸钠水溶液时阳极半反应的方程式。4-2-4 写出单斜晶系的晶胞中Y分子的数目。4-2-5 降温过程中晶系转化为对称性较低的单斜晶体,简述原因。(5)2017年第4题(10分)随着科学的发展和大型实验装置(如同步辐射和中子源)的建成,高压技术在物质研究中发挥着越来越重要的作用。高压不仅会引发物质的相变,也会导致新类型化学键的形成。近年来就有多个关于超高压下新型晶体的形成与结构的研究报道。4-1 NaCl晶体在50~300GPa的高压下和Na或Cl2反应,可以形成不同组成、不同结构的晶体。下图给出其中三种晶体的晶胞(大球为氯原子,小球为钠原子)。写出A、B、C的化学式。a-|||-Na-|||-TI-|||-bigcirc Na 9 Tla-|||-Na-|||-TI-|||-bigcirc Na 9 Tl a-|||-Na-|||-TI-|||-bigcirc Na 9 Tl a-|||-Na-|||-TI-|||-bigcirc Na 9 TlA B C4-2 在超高压(300 GPa)下,金属钠和氦可形成化合物。结构中,钠离子按简单立方排布,形成Na8立方体空隙(如右图所示),电子对(2e—)和氦原子交替分布填充在立方体的中心。4-2-1 写出晶胞内的钠离子数。4-2-2 写出体现该化合物结构特点的化学式。4-2-3 若将氦原子放在晶胞顶点,写出所有电子对(2e—)在晶胞中的位置。4-2-4 以氦原子为顶点的晶胞边长a=395 pm。计算此结构中Na-He的间距d和晶体的密度ρ(单位:g/cm3)。(6)2015年第5题(8分)有一类复合氧化物具有奇特的性质:受热密度不降反升。这类复合氧化物的理想结构属立方晶系,晶胞示意图如右。图中八面体中心是锆原子,位于晶胞的顶角和面心;四面体中心是钨原子,均在晶胞中。八面体和四面体之间通过共用顶点(氧原子)连接。锆和钨的氧化数分别等于它们在周期表里的族数。5-1 写出晶胞中锆原子和钨原子的数目。5-2 写出这种复合氧化物的化学式。5-3 晶体中,氧原子的化学环境有几种?各是什么类型?在一个晶胞中各有多少?5-4 已知晶胞参数a=0.916 nm,计算该晶体的密度(以g/cm3为单位)。(7)2016年第4题(10分)固体电解质以其在电池、传感器等装置中的广泛应用而备受关注。现有一种由正离子An+、Bm+和负离子X—组成的无机固体电解质,该物质50.7℃以上形成无序结构(高温相),50.7℃以下变为有序结构(低温相),二者结构示意图见下。图中浅色球为负离子;高温相中的深色球为正离子或空位;低温相中的大深色球为An+离子,小深色球为Bm+离子。a-|||-Na-|||-TI-|||-bigcirc Na 9 Tl高温相 低温相4-1 推出这种电解质的化学式,写出n和m的值。4-2 温度变化会导致晶体在立方晶系和四方晶系之间转换,上述哪种晶相属于立方晶系?4-3 写出负离子的堆积方式及形成的空隙类型。指出正离子占据的空隙类型及占有率。4-4 高温相具有良好的离子导电性,这源于哪种离子的迁移?简述导电性与结构的关系。
2015年32题(16分):下图是钠铊合金的立方晶系晶胞图,晶胞参数为a=7.488Å(1 Å =
10—10 m)。
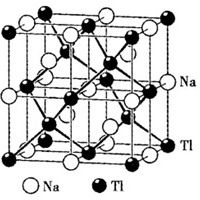
(1)试写出该合金的化学式。
(2)试计算该晶体的密度(保留三位有效数字)。
(3)试写出该晶体的结构基元的化学式,并画出结构基元围成的最小几何构型。写出几何构型中Na、Tl原子的分数坐标。
(4)若把Na原子看作密堆积,其它Na、Tl原子占有密堆积Na原子围成的何类空隙以及空隙占有率分别是多少?
(5)若把一类金属原子全部抽掉,剩下的金属原子属于什么晶型?
(6)该晶体属于何类点阵型式?
《晶体结构》全国初赛题
(4)2018年第4题(12分):4-1利用双离子交换膜 电解法可以从含硝酸铵的工业废水中生产硝酸和氨。
4-1-1 阳极室得到的是哪种物质?写出阳极半反应方程式。
4-1-2 阴极室得到的是哪种物质?写出阴极半反应及获得相应物质的方程式。
4-2 电解乙酸钠水溶液,在阳极收集到X和Y的混合气体。气体通过新制的澄清石灰水,X被完全吸收,得到白色沉淀。纯净的气体Y冷却到90.23K,析出无色晶体,X-射线衍射表明,该晶体属立方晶系,体心立方点阵,晶胞参数a=530.4 pm,Z=2,密度ρ=0.669 g/cm3。继续冷却,晶体转化为单斜晶系,a=422.6 pm,b=562.3 pm,c=584.5 pm,β=90.41°。
4-2-1 写出X的化学式;写出X和石灰水反应的方程式。
4-2-2 通过计算推出Y的化学式(Y分子中存在三次旋转轴)。
4-2-3 写出电解乙酸钠水溶液时阳极半反应的方程式。
4-2-4 写出单斜晶系的晶胞中Y分子的数目。
4-2-5 降温过程中晶系转化为对称性较低的单斜晶体,简述原因。
(5)2017年第4题(10分)随着科学的发展和大型实验装置(如同步辐射和中子源)的建成,高压技术在物质研究中发挥着越来越重要的作用。高压不仅会引发物质的相变,也会导致新类型化学键的形成。近年来就有多个关于超高压下新型晶体的形成与结构的研究报道。
4-1 NaCl晶体在50~300GPa的高压下和Na或Cl2反应,可以形成不同组成、不同结构的晶体。下图给出其中三种晶体的晶胞(大球为氯原子,小球为钠原子)。写出A、B、C的化学式。

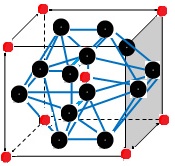
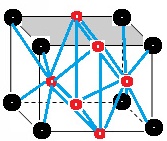
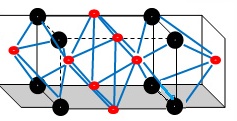
A B C
4-2 在超高压(300 GPa)下,金属钠和氦可形成化合物。结构中,钠离子按简单立方排布,形成Na8立方体空隙(如右图所示),电子对(2e—)和氦原子交替分布填
充在立方体的中心。
4-2-1 写出晶胞内的钠离子数。
4-2-2 写出体现该化合物结构特点的化学式。
4-2-3 若将氦原子放在晶胞顶点,写出所有电子对(2e—)在晶胞中的位置。
4-2-4 以氦原子为顶点的晶胞边长a=395 pm。计算此结构中Na-He的
间距d和晶体的密度ρ(单位:g/cm3)。
(6)2015年第5题(8分)有一类复合氧化物具有奇特的性质:受热密度不降反升。这类复合氧化物的理想结构属立方晶系,晶胞示意图如右。图中八面体中心是锆原子,位于晶胞的顶角和面心;四面体中心是钨原子,均在晶胞中。八面体和四面体之间通过共用顶点(氧原子)连接。锆和钨的氧化数分别等于它们在周期表里的族数。
5-1 写出晶胞中锆原子和钨原子的数目。
5-2 写出这种复合氧化物的化学式。
5-3 晶体中,氧原子的化学环境有几种?各是什么类型?
在一个晶胞中各有多少?
5-4 已知晶胞参数a=0.916 nm,计算该晶体的密度(以
g/cm3为单位)。
(7)2016年第4题(10分)固体电解质以其在电池、
传感器等装置中的广泛应用而备受关注。现有一种由正
离子An+、Bm+和负离子X—组成的无机固体电解质,该
物质50.7℃以上形成无序结构(高温相),50.7℃以下变为有序结构(低温相),二者结构示意图见下。图中浅色球为负离子;高温相中的深色球为正离子或空位;低温相中的大深色球为An+离子,小深色球为Bm+离子。
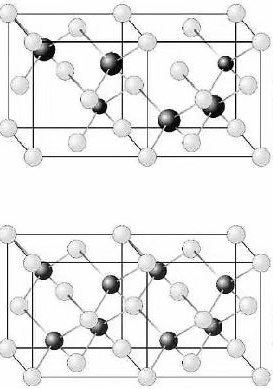
高温相 低温相
4-1 推出这种电解质的化学式,写出n和m的值。
4-2 温度变化会导致晶体在立方晶系和四方晶系之间转换,上述哪种晶相属于立方晶系?
4-3 写出负离子的堆积方式及形成的空隙类型。指出正离子占据的空隙类型及占有率。
4-4 高温相具有良好的离子导电性,这源于哪种离子的迁移?简述导电性与结构的关系。
题目解答
答案
答案
1、AC
2、33.(共14分)
 (1)XY2 3分
(1)XY2 3分(2)X占有Y围成的正八面体空隙 1分
空隙占有率50% 1分