18 、( 1 )晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,下图为 Ge 单晶的晶胞,其中原子坐标参数 A 为( 0,0,0 ); B 为(dfrac (1)(2), 0 ,dfrac (1)(2)); C 为(dfrac (1)(2),dfrac (1)(2), 0 )。则 D 原子的坐标参数为 ______ 。②晶胞参数,描述晶胞的大小和形状。已知 Ge 单晶的晶胞参数 a=565.76pm ,其密度为 __________g·cm-3 (列出计算式即可)。③ GaF3 的熔点高于 1000 ℃ , GaCl3 的熔点为 77.9℃ ,其原因是 __________________ 。 dfrac (1)(2) (2)单质铜及镍都是由______键形成的晶体。某镍白铜合金的立方晶胞结构如图所示。①晶胞中铜原子与镍原子的数量比为_____。②若合金的密度为dg/cm3,晶胞参数a=________nm。 dfrac (1)(2) ③第ⅡA族金属碳酸盐分解温度如下: BeCO3 MgCO3 CaCO3 SrCO3 BaCO3 分解温度 100 ℃ 540 ℃ 960 ℃ 1 289 ℃ 1 360 ℃ 分解温度为什么越来越高?_______________________。 (3)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如左图所示。该晶体的类型为_______,Ga与As以________键键合。Ga和As的摩尔质量分别为MGag·mol-1和MAsg·mol-1,原子半径分别为rGapm和rAspm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为_____。甲烷晶体的晶胞如右图所示,该晶胞中含有 个甲烷分子,此晶体在常温、常压下不能存在的原因______________________。 dfrac (1)(2)dfrac (1)(2) (4)金属镍与镧(La)形成的合金是一种良好的储氢材料,如图是一种镍镧合金储氢后的晶胞结构示意图,该合金储氢后,含1mol La的合金可吸附H2的数目为 。 dfrac (1)(2) (5)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中金原子位于顶点,铜原子位于面心,则该合金中金原子(Au)与铜原子(Cu)个数比为 ;若该晶体的晶胞棱长为apm,则该合金密度为 g/cm3。(列出计算式,不要求计算结果,阿伏加德罗常数的值为NA) (6)砷化镓为第三代半导体,以其为材料制造的灯泡寿命长,耗能少。已知立方砷化镓晶胞的结构如图所示,其晶胞边长为cpm,则密度为 g·cm-3(用含c的式子表示,设NA为阿伏加德罗常数的值),a位置As原子与b位置As原子之间的距离为 pm(用含c的式子表示)。 dfrac (1)(2) (7)碳化硅SiC是一种晶体,具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。在下列各种晶体:①晶体硅 ②硝酸钾 ③金刚石 ④碳化硅 ⑤干冰 ⑥冰,它们的熔点由高到低的顺序是________(填序号)。 (8)①科学家把C60和K掺杂在一起制造了一种富勒烯与钾的化合物,该物质在低温时是一种超导体,其晶胞如图所示,该物质中K原子和C60分子的个数比为________。 dfrac (1)(2) ②继C60后,科学家又合成了Si60、N60。请解释如下现象:熔点Si60>N60>C60,而破坏分子所需要的能量N60>C60>Si60,其原因是_________。 (9)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为________,微粒间存在的作用力是______。SiC晶体和晶体Si的熔沸点高低顺序是________。 氧化物MO的电子总数与SiC的相等,则M为________(填元素符号)。MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是_______________。Na、M、Ca三种晶体共同的物理性质是______(填序号)。 ①有金属光泽 ②导电性 ③导热性 ④延展性 如图甲所示为二维平面晶体示意图,所表示的物质化学式为AX3的是________(填“a”或“b”)。图乙为金属铜的晶胞,此晶胞立方体的边长为apm,金属铜的密度为ρg·cm-3,则阿伏加德罗常数可表示为________ mol-1(用含a、ρ的代数式表示)。 dfrac (1)(2) FeO、NiO的晶体结构与NaCl晶体结构相同,其中Fe2+与Ni2+的离子半径分别为7.8×10-2nm、6.9×10-2nm,则熔点FeO___(填“<”、“>”或“=”)NiO,原因是_____________。磷化硼是一种超硬耐磨的涂层材料,其晶胞如图2所示。P原子与B原子的最近距离为acm,则磷化硼晶胞的边长为________cm(用含a的代数式表示)。 dfrac (1)(2)
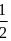 ,
0
,
,
0
,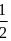 );
C
为(
);
C
为(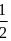 ,
,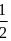 ,
0
)。则
D
原子的坐标参数为
______
。②晶胞参数,描述晶胞的大小和形状。已知
Ge
单晶的晶胞参数
a=565.76pm
,其密度为
__________g·cm-3
(列出计算式即可)。③
GaF3
的熔点高于
1000 ℃
,
GaCl3
的熔点为
77.9℃
,其原因是
__________________
。
,
0
)。则
D
原子的坐标参数为
______
。②晶胞参数,描述晶胞的大小和形状。已知
Ge
单晶的晶胞参数
a=565.76pm
,其密度为
__________g·cm-3
(列出计算式即可)。③
GaF3
的熔点高于
1000 ℃
,
GaCl3
的熔点为
77.9℃
,其原因是
__________________
。
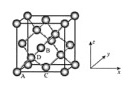
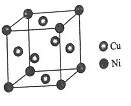
(2)单质铜及镍都是由______键形成的晶体。某镍白铜合金的立方晶胞结构如图所示。①晶胞中铜原子与镍原子的数量比为_____。②若合金的密度为dg/cm3,晶胞参数a=________nm。
③第ⅡA族金属碳酸盐分解温度如下:
|
BeCO3 |
MgCO3 |
CaCO3 |
SrCO3 |
BaCO3 |
分解温度 |
100 ℃ |
540 ℃ |
960 ℃ |
1 289 ℃ |
1 360 ℃ |
分解温度为什么越来越高?_______________________。
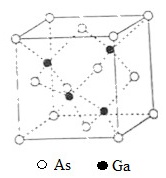
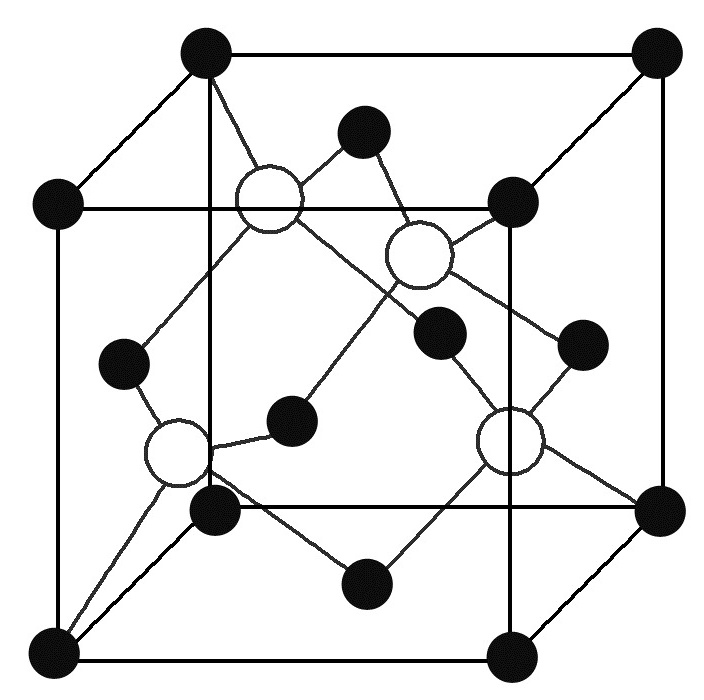
(3)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如左图所示。该晶体的类型为_______,Ga与As以________键键合。Ga和As的摩尔质量分别为MGag·mol-1和MAsg·mol-1,原子半径分别为rGapm和rAspm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为_____。甲烷晶体的晶胞如右图所示,该晶胞中含有 个甲烷分子,此晶体在常温、常压下不能存在的原因______________________。
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,如图是一种镍镧合金储氢后的晶胞结构示意图,该合金储氢后,含1mol La的合金可吸附H2的数目为 。
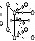
(5)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中金原子位于顶点,铜原子位于面心,则该合金中金原子(Au)与铜原子(Cu)个数比为 ;若该晶体的晶胞棱长为apm,则该合金密度为 g/cm3。(列出计算式,不要求计算结果,阿伏加德罗常数的值为NA)
(6)砷化镓为第三代半导体,以其为材料制造的灯泡寿命长,耗能少。已知立方砷化镓晶胞的结构如图所示,其晶胞边长为cpm,则密度为 g·cm-3(用含c的式子表示,设NA为阿伏加德罗常数的值),a位置As原子与b位置As原子之间的距离为 pm(用含c的式子表示)。
(7)碳化硅SiC是一种晶体,具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。在下列各种晶体:①晶体硅 ②硝酸钾 ③金刚石 ④碳化硅 ⑤干冰 ⑥冰,它们的熔点由高到低的顺序是________(填序号)。
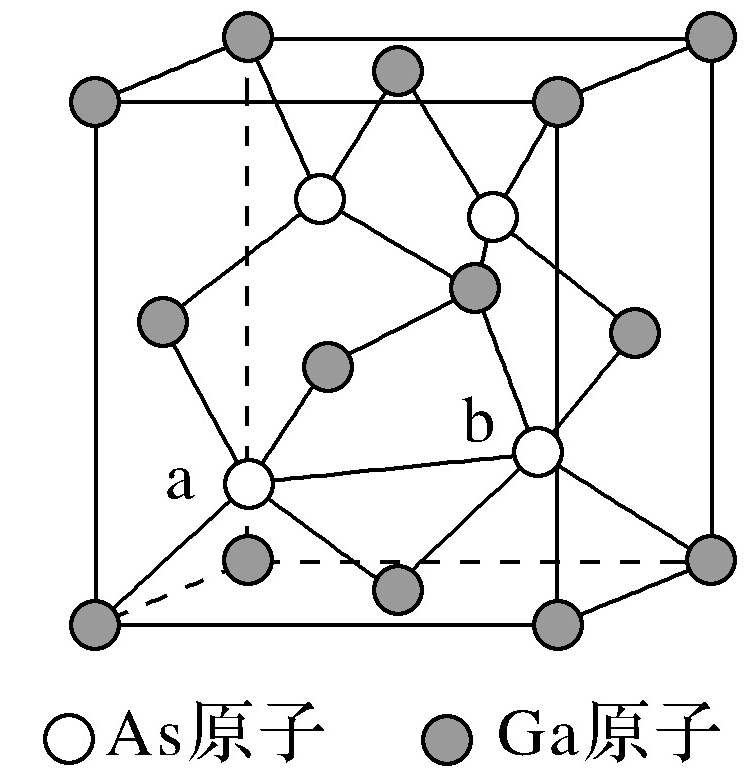
(8)①科学家把C60和K掺杂在一起制造了一种富勒烯与钾的化合物,该物质在低温时是一种超导体,其晶胞如图所示,该物质中K原子和C60分子的个数比为________。
②继C60后,科学家又合成了Si60、N60。请解释如下现象:熔点Si60>N60>C60,而破坏分子所需要的能量N60>C60>Si60,其原因是_________。
(9)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为________,微粒间存在的作用力是______。SiC晶体和晶体Si的熔沸点高低顺序是________。
氧化物MO的电子总数与SiC的相等,则M为________(填元素符号)。MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是_______________。Na、M、Ca三种晶体共同的物理性质是______(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
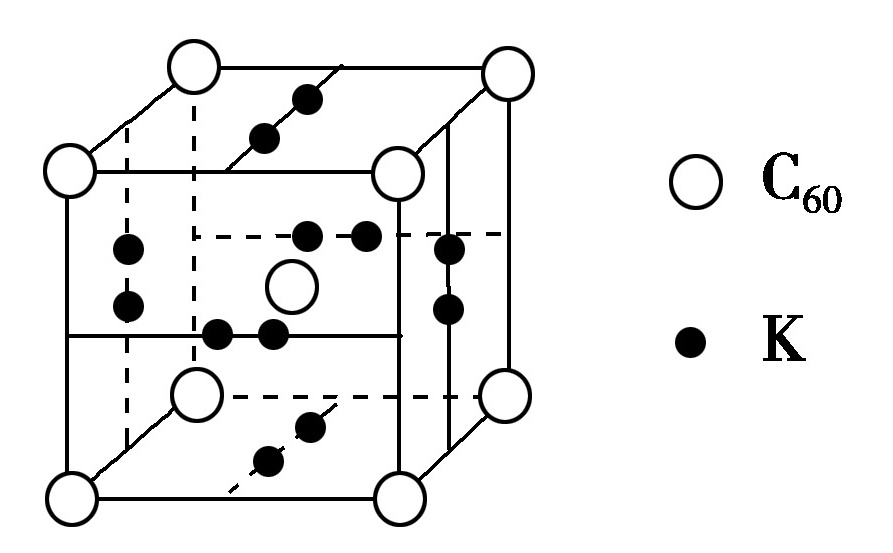
如图甲所示为二维平面晶体示意图,所表示的物质化学式为AX3的是________(填“a”或“b”)。图乙为金属铜的晶胞,此晶胞立方体的边长为apm,金属铜的密度为ρg·cm-3,则阿伏加德罗常数可表示为________ mol-1(用含a、ρ的代数式表示)。
FeO、NiO的晶体结构与NaCl晶体结构相同,其中Fe2+与Ni2+的离子半径分别为7.8×10-2nm、6.9×10-2nm,则熔点FeO___(填“<”、“>”或“=”)NiO,原因是_____________。磷化硼是一种超硬耐磨的涂层材料,其晶胞如图2所示。P原子与B原子的最近距离为acm,则磷化硼晶胞的边长为________cm(用含a的代数式表示)。
题目解答
答案
 ,
, ,
, );②
);② ③由于GaF3是离子晶体,GaCl3是分子晶体,所以离子晶体GaF3的熔沸点高(2)金属;①3:1;②
③由于GaF3是离子晶体,GaCl3是分子晶体,所以离子晶体GaF3的熔沸点高(2)金属;①3:1;②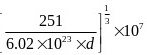 ③阳离子半径越小对氧的吸引力越大,夺取氧的能力越强(3)原子晶体;共价键
③阳离子半径越小对氧的吸引力越大,夺取氧的能力越强(3)原子晶体;共价键 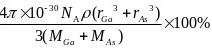 ;4甲烷分子间靠分子间作用力结合,所以甲烷晶体为分子晶体,而分子晶体熔沸点在常压下很低,且甲烷的相对分子质量很小,分子间作用力很小(4)3mol (5)1∶3 (6) c(7)③④①②⑥⑤
;4甲烷分子间靠分子间作用力结合,所以甲烷晶体为分子晶体,而分子晶体熔沸点在常压下很低,且甲烷的相对分子质量很小,分子间作用力很小(4)3mol (5)1∶3 (6) c(7)③④①②⑥⑤(8)①3∶1②结构相似的分子晶体的相对分子质量越大,分子间作用力(或范德华力)越强,熔化所需的能量越多,故熔点:Si60>N60>C60;而破坏分子需断开化学键,元素电负性越强其形成的化学键越稳定,断键时所需能量越多,故破坏分子需要的能量大小顺序为N60>C60>Si60(9)sp3 共价键 SiC>Si(10)Mg Mg2+半径比Ca2+小,MgO晶格能大 ①②③④(11)b ×1030(12)< FeO和NiO相比,阴离子相同,阳离子所带电荷相同,但亚铁离子半径大于镍离子,所以FeO晶格能小,熔点低