30.(一)“一氧化碳变换”是化工生产中的重要反应。研究表明,温度和催化剂是CO变换最重要的工艺条件,某工厂采用“一氧化碳中温-低温-低温串联变换法”,其工艺流程如图所示(部分流程省略)。变换气-|||-1-|||-原料气-|||-2-|||-3-|||-工艺流程图已知:①变换反应:H2O(g)+CO(g)变换气-|||-1-|||-原料气-|||-2-|||-3-|||-工艺流程图CO2(g)+H2(g) △H=-41.2kJ·mol-1(反应Ⅰ)可能发生的副反应:CO(g)+H2(g)变换气-|||-1-|||-原料气-|||-2-|||-3-|||-工艺流程图C(s)+H2O(g)CO(g)+3H2(g)变换气-|||-1-|||-原料气-|||-2-|||-3-|||-工艺流程图CH4(g)+ H2O(g)CO2(g)+4H2(g)变换气-|||-1-|||-原料气-|||-2-|||-3-|||-工艺流程图CH4(g)+ 2H2O(g)②“汽气比”(H2O/CO)指通入变换炉原料气中水蒸气与一氧化碳的体积比。③工艺流程图中的“1,2,3”为采用不同温度和催化剂的变换炉,变换炉之间为间壁式换热器。催化机理:水分子首先被催化剂表面吸附并分解为氢气及吸附态的氧原子,当一氧化碳分子撞击到氧原子吸附层时被氧化为二氧化碳离开吸附剂表面。请回答:(1)利于提高CO平衡转化率的条件有_________。A.低温 B.高温 C.低压 D.高压 E.催化剂(2)维持体系总压强p恒定,体积为V,在温度T时,通入总物质的量为n、汽气比为3的水蒸气和一氧化碳混合气体发生反应I。已知一氧化碳的平衡转化率为α,则在该温度下反应I的平衡常数K=_____。(用α等符号表示)(3)实际生产中变换炉1中常用工艺条件为:使用铁基催化剂,控制温度在300℃~400℃,汽气比3~5。下图 是实际生产中,在一定温度和不同汽气比条件下(其他条件一定)的一氧化碳转化率曲线。变换气-|||-1-|||-原料气-|||-2-|||-3-|||-工艺流程图变换气-|||-1-|||-原料气-|||-2-|||-3-|||-工艺流程图①分析说明当汽气比过大时,CO转化率下降的原因为_____。②在图 中画出300℃时的CO平衡转化率曲线(不考虑副反应的影响)_____________________。③关于一氧化碳变换工艺的下列理解,正确的是_________。A.反应Ⅰ受压强影响小,是因为该反应的△S=0B.工业上可采用稍高于常压的条件,以加快反应速率C.催化剂分段加装是为了增大接触面积,加快化学反应速率D.可以研究适合更低温条件的催化剂,能降低能耗并提高一氧化碳转化率E.适当增大汽气比有利于减少积炭(二)工业上含氰(CN-)废水可以在碱性条件下,用次氯酸钠等氧化剂除去;也可在碱性条件下用电解法去除其毒性,这两种方法都分为两步进行,中间产物均为CNO-,最终都将中间产物转化为无毒稳定的无机物,试分别写出氧化法第二步反应和电解法第二步反应的离子方程式:_____;
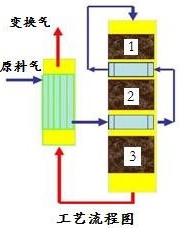
30.(一)“一氧化碳变换”是化工生产中的重要反应。研究表明,温度和催化剂是CO变换最重要的工艺条件,某工厂采用“一氧化碳中温-低温-低温串联变换法”,其工艺流程如图所示(部分流程省略)。
已知:①变换反应:H2O(g)+CO(g)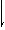 CO2(g)+H2(g) △H=-41.2kJ·mol-1(反应Ⅰ)可能发生的副反应:
CO2(g)+H2(g) △H=-41.2kJ·mol-1(反应Ⅰ)可能发生的副反应:
CO(g)+H2(g)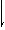 C(s)+H2O(g)
C(s)+H2O(g)
CO(g)+3H2(g)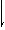 CH4(g)+ H2O(g)
CH4(g)+ H2O(g)
CO2(g)+4H2(g) CH4(g)+ 2H2O(g)
CH4(g)+ 2H2O(g)
②“汽气比”(H2O/CO)指通入变换炉原料气中水蒸气与一氧化碳的体积比。
③工艺流程图中的“1,2,3”为采用不同温度和催化剂的变换炉,变换炉之间为间壁式换热器。催化机理:水分子首先被催化剂表面吸附并分解为氢气及吸附态的氧原子,当一氧化碳分子撞击到氧原子吸附层时被氧化为二氧化碳离开吸附剂表面。
请回答:
(1)利于提高CO平衡转化率的条件有_________。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)维持体系总压强p恒定,体积为V,在温度T时,通入总物质的量为n、汽气比为3的水蒸气和一氧化碳混合气体发生反应I。已知一氧化碳的平衡转化率为α,则在该温度下反应I的平衡常数K=_____。(用α等符号表示)
(3)实际生产中变换炉1中常用工艺条件为:使用铁基催化剂,控制温度在300℃~400℃,汽气比3~5。下图 是实际生产中,在一定温度和不同汽气比条件下(其他条件一定)的一氧化碳转化率曲线。
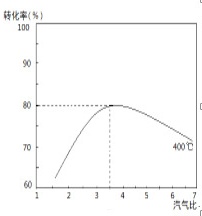
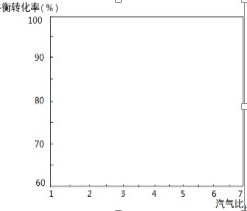
①分析说明当汽气比过大时,CO转化率下降的原因为_____。
②在图 中画出300℃时的CO平衡转化率曲线(不考虑副反应的影响)_____________________。
③关于一氧化碳变换工艺的下列理解,正确的是_________。
A.反应Ⅰ受压强影响小,是因为该反应的△S=0
B.工业上可采用稍高于常压的条件,以加快反应速率
C.催化剂分段加装是为了增大接触面积,加快化学反应速率
D.可以研究适合更低温条件的催化剂,能降低能耗并提高一氧化碳转化率
E.适当增大汽气比有利于减少积炭
(二)工业上含氰(CN-)废水可以在碱性条件下,用次氯酸钠等氧化剂除去;也可在碱性条件下用电解法去除其毒性,这两种方法都分为两步进行,中间产物均为CNO-,最终都将中间产物转化为无毒稳定的无机物,试分别写出氧化法第二步反应和电解法第二步反应的离子方程式:_____;
题目解答
答案
【答案】 (1). A (2). α2/(1-α)(3-α) (3). 蒸汽量太大,气体与催化剂的接触时间减少 (4). 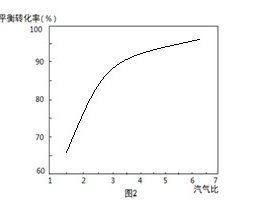 (5). BDE (6). 2CNO-+3ClO-+2OH-=2CO32-+N2+3Cl-+H2O ,2CNO-+8OH--6e-=2CO32-+N2+4H2O
(5). BDE (6). 2CNO-+3ClO-+2OH-=2CO32-+N2+3Cl-+H2O ,2CNO-+8OH--6e-=2CO32-+N2+4H2O
【解析】
【分析】
本题从影响化学平衡移动因素角度分析,注意结合题给信息分析工业流程中化学处理方法,在书写氧化还原反应方程式时,根据化合价高低找准题中氧化剂和还原剂进而分析。
【详解】(一)(1)该反应正向为放热反应,降低温度平衡正向移动,可提高CO平衡转化率;反应前后气体分子数不变,压强变化对平衡无影响,使用催化剂对平衡无影响,均不改变转化率,故本题选A;
(2)由三段式计算有:
H2O(g) + CO(g) 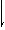 CO2(g) + H2(g)
CO2(g) + H2(g)
起始量(mol):3n/4 n/4 0 0
变化量(mol):nα/4 nα/4 nα/4 nα/4
平衡量(mol):(3-α)n/4 (1-α)n/4 nα/4 nα/4
则平衡常数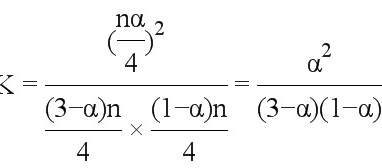 ;
;
(3)①蒸汽量过大时,气体与催化剂的接触时间减少,CO转化率下降;
②参照400℃时图像,降低温度可增大CO转化率,故图像为 ;
;
③该反应反应前后气体分子数不变,故压强变化对平衡无影响,但不能因此确定△S=0,故A错误;增大压强可加快反应速率,在考虑成本情况下可适当增大压强,故B正确;催化剂分段加装是为了保持其催化活性,故C错误;降低温度,能降低能耗并提高一氧化碳转化率,故D正确;由催化机理可知,适当增大汽气比可加快CO撞击到氧原子吸附层得速率,减少积炭,故E正确。本题答案BDE;
(二)CNO-有还原性,故氧化法第二步反应为2CNO-+3ClO-+2OH-=2CO32-+N2+3Cl-+H2O,电解法第二步反应为2CNO-+8OH--6e-=2CO32-+N2+4H2O。