合成氨工业和硫酸工业的生产工艺流程大致为:H2、N2-|||-原 压 合成塔 一 冷凝器 氨分离器H2 循环压缩机-|||-液氨-|||-SO2、O2-|||-浓硫酸-|||-硫铁矿 →沸 炉气 SO2、O2 热 SO2、O2 吸收塔 尾气 尾 气-|||-SO-|||-空气 处理器-|||-硫酸产品-|||-副产品上述合成塔和接触室中的反应分别为:N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ/mol;2SO2(g)+O2(g)⇌2SO3(g)△H=-196.6kJ/mol(1)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是.(2)采用循环操作可以提高原料的利用率,下列工业生产中,采用循环操作的是(填写序号).①硫酸工业②合成氨工业③硝酸工业④氯碱工业(3)根据化学平衡移动原理来确定的条件或措施有(填写序号).①合成氨工业在高压下进行;②硫酸工业的催化氧化在常压下进行;③合成氨工业及时将氨液化分离;④硫酸工业净化后的炉气中含有过量空气;⑤硫铁矿石加入沸腾炉之前先粉碎;⑥吸收塔中用98.3%的浓硫酸吸收SO3⑦合成氨工业和硫酸工业都使用催化剂;⑧合成氨工业和硫酸工业都用适宜的温度(4)硫酸工业尾气直接排放到空气中会造成环境污染,其后果主要是.处理硫酸工业尾气的一种常用方法是“氨-酸”法,写出这种尾气处理方法的化学方程式.有人研究用Na2SO3作为治理SO2污染的一种新方法,该方法的第一步是用Na2SO3水溶液吸收SO2,第二步是加热吸收溶液,使之重新生成Na2SO3,同时得到含高浓度SO2的水蒸气副产品.这种尾气处理方法与“氨一酸”相比的优点是.(5)若经净化、干燥处理后进入接触室的气体体积组成是:SO27%,O211%,N282%,从接触室出来的气体中SO3的体积分数为7%,则SO2的转化率为(保留三位有效数字)..
合成氨工业和硫酸工业的生产工艺流程大致为: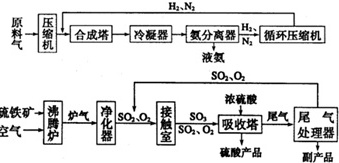
上述合成塔和接触室中的反应分别为:
N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ/mol;
2SO2(g)+O2(g)⇌2SO3(g)△H=-196.6kJ/mol
(1)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是.
(2)采用循环操作可以提高原料的利用率,下列工业生产中,采用循环操作的是(填写序号).
①硫酸工业②合成氨工业③硝酸工业④氯碱工业
(3)根据化学平衡移动原理来确定的条件或措施有(填写序号).
①合成氨工业在高压下进行;
②硫酸工业的催化氧化在常压下进行;
③合成氨工业及时将氨液化分离;
④硫酸工业净化后的炉气中含有过量空气;
⑤硫铁矿石加入沸腾炉之前先粉碎;
⑥吸收塔中用98.3%的浓硫酸吸收SO3
⑦合成氨工业和硫酸工业都使用催化剂;
⑧合成氨工业和硫酸工业都用适宜的温度
(4)硫酸工业尾气直接排放到空气中会造成环境污染,其后果主要是.处理硫酸工业尾气的一种常用方法是“氨-酸”法,写出这种尾气处理方法的化学方程式.有人研究用Na2SO3作为治理SO2污染的一种新方法,该方法的第一步是用Na2SO3水溶液吸收SO2,第二步是加热吸收溶液,使之重新生成Na2SO3,同时得到含高浓度SO2的水蒸气副产品.这种尾气处理方法与“氨一酸”相比的优点是.
(5)若经净化、干燥处理后进入接触室的气体体积组成是:SO27%,O211%,N282%,从接触室出来的气体中SO3的体积分数为7%,则SO2的转化率为(保留三位有效数字).
题目解答
答案
充分利用反应中放出的热量加热反应气 ①②③ ①③④ 形成酸雨 SO2+2NH3•H2O═(NH4)2SO3,(NH4)2SO3+H2SO4═(NH4)2SO4+SO2↑+H2O Na2SO3可循环使用 96.6%
.