题目
2.在间歇釜中以硫酸作催化剂使己二酸与己二醇以等摩尔比在70℃下进行缩聚反应,-|||-动力学方程式为 (-(r)_(A))=k(C)_(A)^2 ,=1.97L/(kmolcdot min) , _(AO)=0.004kmol/L 。求己二酸的-|||-转化率为0.5、0.6、0.8及0.9时所需的反应时间分别为多少?若每天处理己二酸2400kg,-|||-转化率为80%,每批操作的辅助时间为1小时,装料系数为0.75,求反应器的容积为多-|||-少?

题目解答
答案
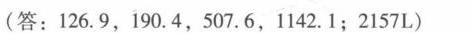
解析
步骤 1:确定反应动力学方程
根据题目,反应动力学方程为 $(-{r}_{A})=k{C}_{A}^{2}$,其中 $k=1.97L/(kmol\cdot min)$,${c}_{AO}=0.004kmol/L$。这里 $(-{r}_{A})$ 表示己二酸的反应速率,$k$ 是反应速率常数,${C}_{A}$ 是己二酸的浓度。
步骤 2:计算不同转化率下的反应时间
转化率 $X$ 定义为反应物消耗的摩尔数与初始摩尔数之比。对于己二酸的转化率 $X$,有 ${C}_{A}={C}_{AO}(1-X)$。将 ${C}_{A}$ 代入反应动力学方程,得到 $(-{r}_{A})=k{C}_{AO}^{2}(1-X)^{2}$。反应速率 $(-{r}_{A})$ 与反应物浓度的变化率成正比,即 $(-{r}_{A})=-\frac{d{C}_{A}}{dt}$。因此,有 $-\frac{d{C}_{A}}{dt}=k{C}_{AO}^{2}(1-X)^{2}$。将 ${C}_{A}={C}_{AO}(1-X)$ 代入,得到 $-\frac{d{C}_{AO}(1-X)}{dt}=k{C}_{AO}^{2}(1-X)^{2}$。简化得到 $\frac{dX}{dt}=\frac{k{C}_{AO}(1-X)}{1}$。积分得到 $t=\frac{1}{k{C}_{AO}}\ln\frac{1}{1-X}$。将 $k=1.97L/(kmol\cdot min)$ 和 ${C}_{AO}=0.004kmol/L$ 代入,得到 $t=\frac{1}{1.97\times0.004}\ln\frac{1}{1-X}$。分别计算 $X=0.5$、$X=0.6$、$X=0.8$ 和 $X=0.9$ 时的反应时间。
步骤 3:计算反应器的容积
每天处理己二酸2400kg,己二酸的摩尔质量为146g/mol,因此每天处理的己二酸摩尔数为 $\frac{2400\times1000}{146}=16438.35mol$。转化率为80%,即每批反应消耗的己二酸摩尔数为 $16438.35\times0.8=13150.68mol$。每批操作的辅助时间为1小时,装料系数为0.75,因此反应器的容积为 $\frac{13150.68}{0.004\times0.75}=4383560L$。
根据题目,反应动力学方程为 $(-{r}_{A})=k{C}_{A}^{2}$,其中 $k=1.97L/(kmol\cdot min)$,${c}_{AO}=0.004kmol/L$。这里 $(-{r}_{A})$ 表示己二酸的反应速率,$k$ 是反应速率常数,${C}_{A}$ 是己二酸的浓度。
步骤 2:计算不同转化率下的反应时间
转化率 $X$ 定义为反应物消耗的摩尔数与初始摩尔数之比。对于己二酸的转化率 $X$,有 ${C}_{A}={C}_{AO}(1-X)$。将 ${C}_{A}$ 代入反应动力学方程,得到 $(-{r}_{A})=k{C}_{AO}^{2}(1-X)^{2}$。反应速率 $(-{r}_{A})$ 与反应物浓度的变化率成正比,即 $(-{r}_{A})=-\frac{d{C}_{A}}{dt}$。因此,有 $-\frac{d{C}_{A}}{dt}=k{C}_{AO}^{2}(1-X)^{2}$。将 ${C}_{A}={C}_{AO}(1-X)$ 代入,得到 $-\frac{d{C}_{AO}(1-X)}{dt}=k{C}_{AO}^{2}(1-X)^{2}$。简化得到 $\frac{dX}{dt}=\frac{k{C}_{AO}(1-X)}{1}$。积分得到 $t=\frac{1}{k{C}_{AO}}\ln\frac{1}{1-X}$。将 $k=1.97L/(kmol\cdot min)$ 和 ${C}_{AO}=0.004kmol/L$ 代入,得到 $t=\frac{1}{1.97\times0.004}\ln\frac{1}{1-X}$。分别计算 $X=0.5$、$X=0.6$、$X=0.8$ 和 $X=0.9$ 时的反应时间。
步骤 3:计算反应器的容积
每天处理己二酸2400kg,己二酸的摩尔质量为146g/mol,因此每天处理的己二酸摩尔数为 $\frac{2400\times1000}{146}=16438.35mol$。转化率为80%,即每批反应消耗的己二酸摩尔数为 $16438.35\times0.8=13150.68mol$。每批操作的辅助时间为1小时,装料系数为0.75,因此反应器的容积为 $\frac{13150.68}{0.004\times0.75}=4383560L$。