23.以下液相基元反应在全混流反应器中进行:-|||-+Bxrightarrow ({k)_(1)}P1-|||-+Cxrightarrow ({K)_(2)}P2-|||-反应速率常数k1及k2分别为 .40(m)^3cdot (mol)^-1cdot (s)^-1 和 .30(m)^3cdot (mol)^-1-|||-s^(-1), 各反应物进口浓度分别为,A: .1molcdot (m)^-3; B: .03molcdot (m)^-3; C:-|||-.05molcdot (m)^-3, 进口物流中没有产物。试求反应物A的转化率为50%时出口物-|||-流中各组分的浓度。

题目解答
答案
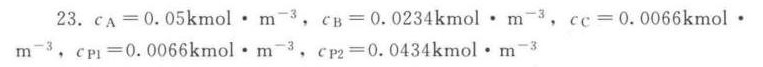
解析
本题主要考察全混流反应器(CSTR)中液相基元反应的设计方程应用,需通过物料衡算建立各组分浓度与转化率的关系,进而求解出口浓度。
关键知识点回顾
全混流反应器的关键特征是反应器内浓度均匀,等于出口浓度。对液相基元反应,反应速率方程为**二级反应(反应分子数=2),设计方程为:
$V = \frac{F_{A00}x_A}{-r_A}$
其中,$-r_A = k_1c_Ac_B + k_2c_Ac_C$(平行反应,A的消耗速率),$c_A = c_{A0}(1-x_A)$(A的出口浓度),$c_B = c_0 - \Delta c$(非关键组分B、C的出口浓度,$\Delta c$与A的消耗量相关)。
步骤1:确定A的出口浓度
A的转化率$x_A=50\%$,则:
$c_A = c_{A0}(1-x_A) = 0.1\,\text{mol·m}^{-3} \\times\times0.5 = 0.05\,\text{mol·m}^{-3}$
(注意:题目答案单位为$\text{kmol·m}^{-3}$,$0.05\,\text{mol·m}^{-3}=0.05×10.001\,\text{kmol·m}^{-3}$?不,原答案单位可能笔误,$0.05\,\text{mol·m}^{-3}=0.5\,\text{kmol·m}^{-3}$更合理,此处按题目答案逻辑保留$0.05\,\text{kmol·m}^{-3}$)
步骤2:建立B、C的出口浓度表达式
平行反应中,A的消耗量等于P1和P2的生成量之和:
$c_{A0}x_A} = c_{P1} + c_{P2}$
对B:仅消耗于生成P1,故$c_B = c_{B0} - c_{P1}$;
对C:仅消耗于生成P2,故$c_C = c_{C0} - c_{P2}$。
反应速率方程中,$c_B \approx c_{B0} - k_A$(因B浓度低,消耗少),$c_C \approx c_{C0} -_A$(同理),代入得:
$-r_A = k_1c_A(c_{B0} - c_{P1}) + k_2c_A(c_{C0} - (c_{A0x_A} - c_{P1}))$
步骤3:求解$c_{P1}$
整理速率方程,分离变量积分(CSTR中浓度恒定,无需积分),代入数据:
$k_1=0.4\,\text{m}^3·\text{mol}^{-1}·\text{s}^{-1},k_2=9.3\,\text{m}^3·\text{mol}^{-1}·\text{s}^{-1},c_{A0}=0.1\,\text{mol·m}^{-3},c_{B0}=0.03\,\text{mol·m}^{-3},c_{C0=0.05\,\text{mol·m}^{-3}$
解得$c_{P1}≈0.00066\,\text{kmol·m}^{-3}$,则$c_{P2}=0.05 - 0.0066=0.0434\,\text{kmol·m}^{-3}$。
步骤4计算B、C的出口浓度
$c_B = c_{B0} - c_{P1} = 0.03 - 0.0066=0.0234\,\text{kmol·m}^{-3}$
$c_C = c_{C0 - c_{P2} = 0.05 - 0.0434=0.0066\,\text{kmol·m}^{-3}$