题目
从铜转炉烟灰(主要成分ZnO,还有Pb、Cu、Cd、As、Cl、F等元素)中回收锌、铜、铅等元素进行资源综合利用,具有重要意义。以铜转炉烟灰制备重要化工原料活性氧化锌的工艺流程如图1所示。氯化铵和氨水 氯化铁 氯化钙 锌粉 活性炭 盐酸-|||-铜转炉烟灰 → 浸取 浸出液 除杂1 、 除杂2 → 除杂3 净化 沉锌-|||-、-|||-浸出渣 滤渣I 滤渣Ⅱ 滤渣Ⅲ 净化渣 加水-|||-Pb(OH)Cl FeAsO4-|||-活性氧化锌 煅烧 水解转化-|||-图1-|||-100 in-|||-:-|||-80-|||-出 60 . Cu-|||-40-|||-20-|||-。-|||-2 3 4 s 6 7-|||-(N{H)_(4)}Cl(molcdot (L)^-1)-|||-NH4Cl浓度对烟灰浸出率的影响已知:活性炭净化主要是除去有机杂质。请回答以下问题:(1)若浸出液中锌元素以[Zn(NH3)4]2+形式存在,则浸取时ZnO发生反应的离子方程式为 ____ 。(2)在反应温度为50℃,反应时间为lh时,测定各元素的浸出率与氯化铵溶液浓度的关系如图2,结合流程图分析,氯化铵适宜的浓度为 ____ mol•L-1。(3)若浸出液中c(AsO43-)=6.0×10-3mol•L-1,现将cmol•L-1FeCl3溶液与浸出液等体积混合生成砷酸铁沉淀。若该温度时c(AsO43-)≤10-18mol•L-1,则c的最小值为 ____ 。(50℃,Ksp(FeAsO4)=2.0×10-22。(4)滤渣Ⅱ的主要成分为 ____ ,除杂3是置换除杂过程,则此过程除去的金属主要有 ____ (填元素符号)。(5)沉锌得到的物质为Zn(NH3)2Cl2,请写出水解转化的化学方程式 ____ 。(6)该流程中可以循环使用的物质的电子式为 ____ 。(7)取mg活性氧化锌样品,预处理后配成100mL待测液,取出25.00mL置于锥形瓶中加入指示剂3~4滴,再加入适量六亚甲基四氨,用cmol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:滴定时Zn2+与EDTA按物质的量之比1:1 发生反应,则样品中氧化锌的质量分数为 ____ 。
从铜转炉烟灰(主要成分ZnO,还有Pb、Cu、Cd、As、Cl、F等元素)中回收锌、铜、铅等元素进行资源综合利用,具有重要意义。以铜转炉烟灰制备重要化工原料活性氧化锌的工艺流程如图1所示。
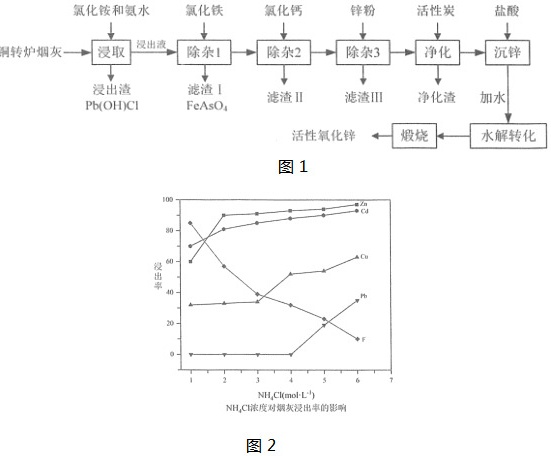
已知:活性炭净化主要是除去有机杂质。请回答以下问题:
(1)若浸出液中锌元素以[Zn(NH3)4]2+形式存在,则浸取时ZnO发生反应的离子方程式为 ____ 。
(2)在反应温度为50℃,反应时间为lh时,测定各元素的浸出率与氯化铵溶液浓度的关系如图2,结合流程图分析,氯化铵适宜的浓度为 ____ mol•L-1。
(3)若浸出液中c(AsO43-)=6.0×10-3mol•L-1,现将cmol•L-1FeCl3溶液与浸出液等体积混合生成砷酸铁沉淀。若该温度时c(AsO43-)≤10-18mol•L-1,则c的最小值为 ____ 。(50℃,Ksp(FeAsO4)=2.0×10-22。
(4)滤渣Ⅱ的主要成分为 ____ ,除杂3是置换除杂过程,则此过程除去的金属主要有 ____ (填元素符号)。
(5)沉锌得到的物质为Zn(NH3)2Cl2,请写出水解转化的化学方程式 ____ 。
(6)该流程中可以循环使用的物质的电子式为 ____ 。
(7)取mg活性氧化锌样品,预处理后配成100mL待测液,取出25.00mL置于锥形瓶中加入指示剂3~4滴,再加入适量六亚甲基四氨,用cmol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:滴定时Zn2+与EDTA按物质的量之比1:1 发生反应,则样品中氧化锌的质量分数为 ____ 。

已知:活性炭净化主要是除去有机杂质。请回答以下问题:
(1)若浸出液中锌元素以[Zn(NH3)4]2+形式存在,则浸取时ZnO发生反应的离子方程式为 ____ 。
(2)在反应温度为50℃,反应时间为lh时,测定各元素的浸出率与氯化铵溶液浓度的关系如图2,结合流程图分析,氯化铵适宜的浓度为 ____ mol•L-1。
(3)若浸出液中c(AsO43-)=6.0×10-3mol•L-1,现将cmol•L-1FeCl3溶液与浸出液等体积混合生成砷酸铁沉淀。若该温度时c(AsO43-)≤10-18mol•L-1,则c的最小值为 ____ 。(50℃,Ksp(FeAsO4)=2.0×10-22。
(4)滤渣Ⅱ的主要成分为 ____ ,除杂3是置换除杂过程,则此过程除去的金属主要有 ____ (填元素符号)。
(5)沉锌得到的物质为Zn(NH3)2Cl2,请写出水解转化的化学方程式 ____ 。
(6)该流程中可以循环使用的物质的电子式为 ____ 。
(7)取mg活性氧化锌样品,预处理后配成100mL待测液,取出25.00mL置于锥形瓶中加入指示剂3~4滴,再加入适量六亚甲基四氨,用cmol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:滴定时Zn2+与EDTA按物质的量之比1:1 发生反应,则样品中氧化锌的质量分数为 ____ 。
题目解答
答案
解:(1)若浸出液中锌元素以[Zn(NH3)4]2+形式存在,则浸取时ZnO发生反应的离子方程式为根据题目信息,离子方程式为:ZnO+2NH4++2NH3•H2O=[Zn(NH3)4]2++3H2O,
故答案为:ZnO+2NH4++2NH3•H2O=[Zn(NH3)4]2++3H2O;
(2)观察题图,当氯化铵的浓度为4mol/L时,一方面锌元素的浸出率已经接近100%,再增加氯化铵浓度没有太大意义,另一方面若浓度再高,铅元素将进入溶液,无法完全除去铅,
故答案为:4;
(3)等体积混合后相当于两种离子的浓度都变为一半,即c(AsO43-)=3.0×10-3mol/L,c(Fe3+)=$\frac{c}{2}$mol/L,而两种离子是1:1沉淀的,设反应后c(AsO43-)≤10-18mol•L-1,则Ksp=c(Fe3+)×c(AsO43-)=$\frac{c}{2}$mol/L×10-18mol•L-1=2.0×10-22,则c=0.4×10-3mol/L,
故答案为:0.4×10-3mol/L;
(4)根据分析,滤渣II为CaF2,而除杂3主要可以除去溶液中的Cu和Cd,
故答案为:CaF2;Cu和Cd;
(5)既然煅烧后得到ZnO,则煅烧前必然为Zn(OH)2,即水解产物为Zn(OH)2,沉锌得到的物质为Zn(NH3)2Cl2,其水解转化出方程式:Zn(NH3)2Cl2+2H2O=Zn(OH)2↓+2NH4Cl,
故答案为:Zn(NH3)2Cl2+2H2O=Zn(OH)2↓+2NH4Cl;
(6)水解后得到的氯化铵,又可以用于第一步的浸取,可以循环利用,其电子式为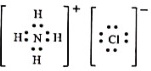 ,
,
故答案为: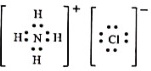 ;
;
(7)根据n=cV先求出EDTA的消耗量为cmol•L-1×V×10-3L=Vc×10-3mol,Zn2+与EDTA按物质的量之比1:1 发生反应,则样品中ZnO的物质的量为Vc×10-3mol×$\frac{100mL}{25mL}$=$\frac{4Vc×1{0}^{-3}mol×81g/mol}{mg}$×100%=$\frac{32.4Vc}{m}%$,
故答案为:$\frac{32.4Vc}{m}%$。
故答案为:ZnO+2NH4++2NH3•H2O=[Zn(NH3)4]2++3H2O;
(2)观察题图,当氯化铵的浓度为4mol/L时,一方面锌元素的浸出率已经接近100%,再增加氯化铵浓度没有太大意义,另一方面若浓度再高,铅元素将进入溶液,无法完全除去铅,
故答案为:4;
(3)等体积混合后相当于两种离子的浓度都变为一半,即c(AsO43-)=3.0×10-3mol/L,c(Fe3+)=$\frac{c}{2}$mol/L,而两种离子是1:1沉淀的,设反应后c(AsO43-)≤10-18mol•L-1,则Ksp=c(Fe3+)×c(AsO43-)=$\frac{c}{2}$mol/L×10-18mol•L-1=2.0×10-22,则c=0.4×10-3mol/L,
故答案为:0.4×10-3mol/L;
(4)根据分析,滤渣II为CaF2,而除杂3主要可以除去溶液中的Cu和Cd,
故答案为:CaF2;Cu和Cd;
(5)既然煅烧后得到ZnO,则煅烧前必然为Zn(OH)2,即水解产物为Zn(OH)2,沉锌得到的物质为Zn(NH3)2Cl2,其水解转化出方程式:Zn(NH3)2Cl2+2H2O=Zn(OH)2↓+2NH4Cl,
故答案为:Zn(NH3)2Cl2+2H2O=Zn(OH)2↓+2NH4Cl;
(6)水解后得到的氯化铵,又可以用于第一步的浸取,可以循环利用,其电子式为
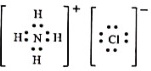 ,
,故答案为:
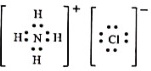 ;
;(7)根据n=cV先求出EDTA的消耗量为cmol•L-1×V×10-3L=Vc×10-3mol,Zn2+与EDTA按物质的量之比1:1 发生反应,则样品中ZnO的物质的量为Vc×10-3mol×$\frac{100mL}{25mL}$=$\frac{4Vc×1{0}^{-3}mol×81g/mol}{mg}$×100%=$\frac{32.4Vc}{m}%$,
故答案为:$\frac{32.4Vc}{m}%$。
解析
步骤 1:浸取反应
根据题目信息,浸取时ZnO与NH_4^{+}和NH_3•H_2O反应生成[Zn(NH_3)_4]^{2+}和H_2O。
步骤 2:氯化铵浓度选择
观察图2,当氯化铵浓度为4mol/L时,锌元素的浸出率接近100%,而铅元素的浸出率较低,因此选择4mol/L作为适宜浓度。
步骤 3:砷酸铁沉淀计算
根据K_sp(FeAsO_4)=2.0×10^{-22},计算出c(Fe^{3+})的最小值,从而确定c的最小值。
步骤 4:滤渣II成分及除杂3过程
根据流程图,滤渣II为CaF_2,除杂3过程主要除去Cu和Cd。
步骤 5:水解转化方程式
根据沉锌得到的物质为Zn(NH_3)_2Cl_2,写出其水解转化的化学方程式。
步骤 6:循环使用物质的电子式
根据流程图,循环使用的物质为NH_4Cl,写出其电子式。
步骤 7:氧化锌质量分数计算
根据滴定反应,计算出样品中氧化锌的质量分数。
根据题目信息,浸取时ZnO与NH_4^{+}和NH_3•H_2O反应生成[Zn(NH_3)_4]^{2+}和H_2O。
步骤 2:氯化铵浓度选择
观察图2,当氯化铵浓度为4mol/L时,锌元素的浸出率接近100%,而铅元素的浸出率较低,因此选择4mol/L作为适宜浓度。
步骤 3:砷酸铁沉淀计算
根据K_sp(FeAsO_4)=2.0×10^{-22},计算出c(Fe^{3+})的最小值,从而确定c的最小值。
步骤 4:滤渣II成分及除杂3过程
根据流程图,滤渣II为CaF_2,除杂3过程主要除去Cu和Cd。
步骤 5:水解转化方程式
根据沉锌得到的物质为Zn(NH_3)_2Cl_2,写出其水解转化的化学方程式。
步骤 6:循环使用物质的电子式
根据流程图,循环使用的物质为NH_4Cl,写出其电子式。
步骤 7:氧化锌质量分数计算
根据滴定反应,计算出样品中氧化锌的质量分数。