题目
我国在应对气候变化工作中取得显著成效,并向国际社会承诺2030年实现“碳达峰”,2060年实现“碳中和”。因此将CO2转化为高附加值化学品成为科学家研究的重要课题。Ⅰ.已知利用CO2合成甲醇过程中主要发生以下反应:主反应Ⅰ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH1副反应Ⅱ:C(O)_(2)(g)+(H)_(2)(g)⇌CO(g)+(H)_(2)O(g)Δ(H)_(2)=+41.2kJ•mo(l)^-1(1)已知:CO(g)+2(H)_(2)(g)⇌C(H)_(3)OH(g)Δ(H)_(3)=-90.6kJ•mo(l)^-1,则ΔH1为 ____ 。(2)在恒温恒压(1.8MPa,400℃)下,CO2和H2按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得相关数据如下表所示。 反应器 CO2平衡转化率 甲醇的选择性 达到平衡时间/s 普通反应器(A) 25.0% 80.0% 10.0 分子筛膜催化反应器(B) α>25.0% 100.0% 8.0 已知:ⅰ.分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能;i.CH3OH的选择性=(n((C{H)_(3)OH)}_(生成))/(n((C{O)_{2))}_(消耗)}×100%。①在普通反应器(A)中,下列能作为反应(主反应和副反应)达到平衡状态的判据是 ____ (填标号)。A.体系压强不再变化B.气体的密度不再改变C.v正(CO2)=3v逆(H2)D.各物质浓度比不再改变②在分子筛膜催化反应器(B)中,CO2的平衡转化率明显高于普通反应器(A),可能的原因是 ____ 。③若普通反应器(A)中初始时n(CO2)=1mol,则平衡时CO与H2O的物质的量之比为 ____ 。(3)不同条件下,按照n(CO2):n(H2)=1:3投料,CO2的平衡转化率如图所示。85-|||-80-|||-75-|||-70-|||-65-|||-60 →p1-|||-→P2 (500,60)-|||-55-|||-△P3-|||-0 100 200 300 400 500600 700 800 900 1000-|||-^circ C①在p1压强下,200~550℃时反应以 ____ (填“Ⅰ”或“Ⅱ”)为主,压强p1、p2、p3由大到小的顺序是 ____ 。②压强为p2时,温度高于660℃之后,随着温度升高CO2平衡转化率增大的原因是 ____ 。Ⅱ.近年来,有研究人员用CO2通过电催化生成多种燃料如乙烯、甲醇等,实现CO2的回收利用。(4)酸性电解质溶液中乙烯燃料电池的负极反应方程式为 ____ 。
我国在应对气候变化工作中取得显著成效,并向国际社会承诺2030年实现“碳达峰”,2060年实现“碳中和”。因此将CO2转化为高附加值化学品成为科学家研究的重要课题。
Ⅰ.已知利用CO2合成甲醇过程中主要发生以下反应:
主反应Ⅰ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH1
副反应Ⅱ:$C{O}_{2}(g)+{H}_{2}(g)⇌CO(g)+{H}_{2}O(g)Δ{H}_{2}=+41.2kJ•mo{l}^{-1}$
(1)已知:$CO(g)+2{H}_{2}(g)⇌C{H}_{3}OH(g)Δ{H}_{3}=-90.6kJ•mo{l}^{-1}$,则ΔH1为 ____ 。
(2)在恒温恒压(1.8MPa,400℃)下,CO2和H2按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得相关数据如下表所示。
已知:ⅰ.分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能;
i.CH3OH的选择性=$\frac{n{(C{H}_{3}OH)}_{生成}}{n{(C{O}_{2})}_{消耗}}×100%$。
①在普通反应器(A)中,下列能作为反应(主反应和副反应)达到平衡状态的判据是 ____ (填标号)。
A.体系压强不再变化
B.气体的密度不再改变
C.v正(CO2)=3v逆(H2)
D.各物质浓度比不再改变
②在分子筛膜催化反应器(B)中,CO2的平衡转化率明显高于普通反应器(A),可能的原因是 ____ 。
③若普通反应器(A)中初始时n(CO2)=1mol,则平衡时CO与H2O的物质的量之比为 ____ 。
(3)不同条件下,按照n(CO2):n(H2)=1:3投料,CO2的平衡转化率如图所示。
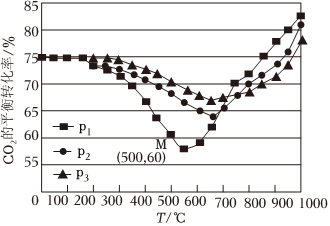
①在p1压强下,200~550℃时反应以 ____ (填“Ⅰ”或“Ⅱ”)为主,压强p1、p2、p3由大到小的顺序是 ____ 。
②压强为p2时,温度高于660℃之后,随着温度升高CO2平衡转化率增大的原因是 ____ 。
Ⅱ.近年来,有研究人员用CO2通过电催化生成多种燃料如乙烯、甲醇等,实现CO2的回收利用。
(4)酸性电解质溶液中乙烯燃料电池的负极反应方程式为 ____ 。
Ⅰ.已知利用CO2合成甲醇过程中主要发生以下反应:
主反应Ⅰ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH1
副反应Ⅱ:$C{O}_{2}(g)+{H}_{2}(g)⇌CO(g)+{H}_{2}O(g)Δ{H}_{2}=+41.2kJ•mo{l}^{-1}$
(1)已知:$CO(g)+2{H}_{2}(g)⇌C{H}_{3}OH(g)Δ{H}_{3}=-90.6kJ•mo{l}^{-1}$,则ΔH1为 ____ 。
(2)在恒温恒压(1.8MPa,400℃)下,CO2和H2按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得相关数据如下表所示。
| 反应器 | CO2平衡转化率 | 甲醇的选择性 | 达到平衡时间/s |
| 普通反应器(A) | 25.0% | 80.0% | 10.0 |
| 分子筛膜催化反应器(B) | α>25.0% | 100.0% | 8.0 |
i.CH3OH的选择性=$\frac{n{(C{H}_{3}OH)}_{生成}}{n{(C{O}_{2})}_{消耗}}×100%$。
①在普通反应器(A)中,下列能作为反应(主反应和副反应)达到平衡状态的判据是 ____ (填标号)。
A.体系压强不再变化
B.气体的密度不再改变
C.v正(CO2)=3v逆(H2)
D.各物质浓度比不再改变
②在分子筛膜催化反应器(B)中,CO2的平衡转化率明显高于普通反应器(A),可能的原因是 ____ 。
③若普通反应器(A)中初始时n(CO2)=1mol,则平衡时CO与H2O的物质的量之比为 ____ 。
(3)不同条件下,按照n(CO2):n(H2)=1:3投料,CO2的平衡转化率如图所示。

①在p1压强下,200~550℃时反应以 ____ (填“Ⅰ”或“Ⅱ”)为主,压强p1、p2、p3由大到小的顺序是 ____ 。
②压强为p2时,温度高于660℃之后,随着温度升高CO2平衡转化率增大的原因是 ____ 。
Ⅱ.近年来,有研究人员用CO2通过电催化生成多种燃料如乙烯、甲醇等,实现CO2的回收利用。
(4)酸性电解质溶液中乙烯燃料电池的负极反应方程式为 ____ 。
题目解答
答案
解:(1)由盖斯定律,副反应Ⅱ+已知反应可得主反应Ⅰ:ΔH1=+41.2kJ/mol-90.6kJ/mol=-49.4kJ/mol,
故答案为:-49.4kJ/mol;
(2)①A.在恒温恒压下进行反应,则混合气体的压强一直保持不变,不能说明反应达到平衡状态,故A错误;
B.在恒温恒压下进行反应,气体体积为变量,而气体质量不变,则气体的密度为变量,当气体的密度不再改变,达到平衡状态,故B正确;
C.反应速率比等于系数比,v正(CO2)=3v逆(H2)不能说明正逆反应速率相等,不能判断达到平衡状态,故C错误;
D.各物质浓度比是一变量,当其不再改变时说明反应达到平衡状态,故D正确;
故答案为:BD;
②分子筛膜具有分离部分H2O的功能,c(H2O)减小,根据勒夏特列原理,平衡正向移动,导致在反应器(B)中的平衡转化率明显高于反应器(A),
故答案为:分子筛膜具有分离出部分H2O(g)的功能,c(H2O)减小,根据勒夏特列原理,平衡正向移动;
③恒温恒压下,体积之比等于物质的量之比,按体积比1:3投料,反应器(A)中初始时,二氧化碳为1mol,则氢气为3mol,由表知,二氧化碳平衡转化率为25.0%,则反应二氧化碳0.25mol,甲醇的选择性为80.0%,则生成甲醇0.25mol×80%=0.2mol,列三段式:
$\begin{array}{c}\end{array}$
$\begin{array}{c}\end{array}$ CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
起始量/mol 1 3 0 0
转化量/mol 0.2 0.6 0.2 0.2
平衡量/mol 0.2
CO2(g)+H2(g)⇌CO(g)+H2O(g)
起始量/mol 0 0
转化量/mol 0.25-0.2 0.05 0.05 0.05
平衡量/mol 0.75 2.35 0.05 0.25
平衡时CO与H2O的物质的量之比为0.05:0.25=1:5,
故答案为:1:5;
(3)①在p1压强下,反应Ⅰ是放热反应,反应Ⅱ是吸热反应,升高温度,反应Ⅰ的平衡向逆反应方向移动,200~550℃时CO2的平衡转化率减小,说明反应由逆向移动,即反应以I为主;反应Ⅰ为气体体积减小的反应、反应Ⅱ为气体体积不变的反应,增大压强,反应Ⅰ向正反应方向移动、反应Ⅱ不移动,二氧化碳的转化率增大,由图可知,温度低于550℃时,压强为P3、P2、P1对应二氧化碳的转化率依次减小,则P3>P2>P1,
故答案为:I;p3>p2>p1;
②压强为p2时,温度高于660℃之后,随着温度升高CO2平衡转化率增大的原因是:反应Ⅰ是放热反应,反应Ⅱ是吸热反应,温度高于660℃之后,温度对反应Ⅱ的影响大于对反应Ⅰ的影响,反应转化率主要由反应Ⅱ决定,
故答案为:反应Ⅰ是放热反应,反应Ⅱ是吸热反应,温度高于660℃之后,温度对反应Ⅱ的影响大于对反应Ⅰ的影响,反应转化率主要由反应Ⅱ决定;
(4)酸性电解质溶液中乙烯燃料电池的负极上乙烯失电子生成二氧化碳,1mol乙烯转移12mol电子,由电荷守恒可知生成物还有12mol H+,负极的反应方程式为C2H4+4H2O-12e-=2CO2+12H+,
故答案为:C2H4+4H2O-12e-=2CO2+12H+。
故答案为:-49.4kJ/mol;
(2)①A.在恒温恒压下进行反应,则混合气体的压强一直保持不变,不能说明反应达到平衡状态,故A错误;
B.在恒温恒压下进行反应,气体体积为变量,而气体质量不变,则气体的密度为变量,当气体的密度不再改变,达到平衡状态,故B正确;
C.反应速率比等于系数比,v正(CO2)=3v逆(H2)不能说明正逆反应速率相等,不能判断达到平衡状态,故C错误;
D.各物质浓度比是一变量,当其不再改变时说明反应达到平衡状态,故D正确;
故答案为:BD;
②分子筛膜具有分离部分H2O的功能,c(H2O)减小,根据勒夏特列原理,平衡正向移动,导致在反应器(B)中的平衡转化率明显高于反应器(A),
故答案为:分子筛膜具有分离出部分H2O(g)的功能,c(H2O)减小,根据勒夏特列原理,平衡正向移动;
③恒温恒压下,体积之比等于物质的量之比,按体积比1:3投料,反应器(A)中初始时,二氧化碳为1mol,则氢气为3mol,由表知,二氧化碳平衡转化率为25.0%,则反应二氧化碳0.25mol,甲醇的选择性为80.0%,则生成甲醇0.25mol×80%=0.2mol,列三段式:
$\begin{array}{c}\end{array}$
$\begin{array}{c}\end{array}$ CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
起始量/mol 1 3 0 0
转化量/mol 0.2 0.6 0.2 0.2
平衡量/mol 0.2
CO2(g)+H2(g)⇌CO(g)+H2O(g)
起始量/mol 0 0
转化量/mol 0.25-0.2 0.05 0.05 0.05
平衡量/mol 0.75 2.35 0.05 0.25
平衡时CO与H2O的物质的量之比为0.05:0.25=1:5,
故答案为:1:5;
(3)①在p1压强下,反应Ⅰ是放热反应,反应Ⅱ是吸热反应,升高温度,反应Ⅰ的平衡向逆反应方向移动,200~550℃时CO2的平衡转化率减小,说明反应由逆向移动,即反应以I为主;反应Ⅰ为气体体积减小的反应、反应Ⅱ为气体体积不变的反应,增大压强,反应Ⅰ向正反应方向移动、反应Ⅱ不移动,二氧化碳的转化率增大,由图可知,温度低于550℃时,压强为P3、P2、P1对应二氧化碳的转化率依次减小,则P3>P2>P1,
故答案为:I;p3>p2>p1;
②压强为p2时,温度高于660℃之后,随着温度升高CO2平衡转化率增大的原因是:反应Ⅰ是放热反应,反应Ⅱ是吸热反应,温度高于660℃之后,温度对反应Ⅱ的影响大于对反应Ⅰ的影响,反应转化率主要由反应Ⅱ决定,
故答案为:反应Ⅰ是放热反应,反应Ⅱ是吸热反应,温度高于660℃之后,温度对反应Ⅱ的影响大于对反应Ⅰ的影响,反应转化率主要由反应Ⅱ决定;
(4)酸性电解质溶液中乙烯燃料电池的负极上乙烯失电子生成二氧化碳,1mol乙烯转移12mol电子,由电荷守恒可知生成物还有12mol H+,负极的反应方程式为C2H4+4H2O-12e-=2CO2+12H+,
故答案为:C2H4+4H2O-12e-=2CO2+12H+。