题目
在连续精馏塔中分离由二硫化碳和四氯化碳所组成的混合液。已知原料液流量为14000kg/h,组成wF为0.3(二硫化碳的质量分数,下同)。若要求釜液组成wW不大于0.05,馏出液回收率为90%。试求馏出液的流量和组成,分别以摩尔流量和摩尔分数表示。
在连续精馏塔中分离由二硫化碳和四氯化碳所组成的混合液。已知原料液流量为14000kg/h,组成wF为0.3(二硫化碳的质量分数,下同)。若要求釜液组成wW不大于0.05,馏出液回收率为90%。试求馏出液的流量和组成,分别以摩尔流量和摩尔分数表示。
题目解答
答案
解:
因为 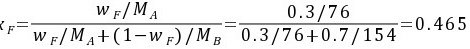
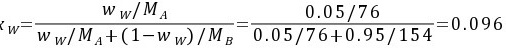
原料液平均摩尔质量
MF=0.465×76+(1-0.465)×154=117.7kg/kmol
所以 F=14000 / 117.7=118.95 kmol/h
馏出液回收率 DxD / FxF =90%
DxD=0.9×118.95×0.465=49.78
由全塔物料衡算
F=D+W 118.95=D+W
FxF=DxD+WxW 118.95×0.465=0.9×118.95×0.465+0.096W
解之 D=61.33kmol/h
故 xD=49.78 / 61.33=0.81
解析
步骤 1:计算原料液的平均摩尔质量
原料液由二硫化碳(CS₂)和四氯化碳(CCl₄)组成,其摩尔质量分别为76 kg/kmol和154 kg/kmol。原料液中二硫化碳的质量分数为0.3,四氯化碳的质量分数为0.7。因此,原料液的平均摩尔质量MF为:
$$
MF = 0.3 \times 76 + 0.7 \times 154 = 123.2 \text{ kg/kmol}
$$
步骤 2:计算原料液的摩尔流量
原料液流量为14000 kg/h,因此原料液的摩尔流量F为:
$$
F = \frac{14000}{123.2} = 113.62 \text{ kmol/h}
$$
步骤 3:计算馏出液的摩尔流量
馏出液回收率为90%,即馏出液中二硫化碳的摩尔流量为原料液中二硫化碳摩尔流量的90%。原料液中二硫化碳的摩尔流量为:
$$
F_{CS₂} = 113.62 \times 0.3 = 34.09 \text{ kmol/h}
$$
因此,馏出液中二硫化碳的摩尔流量为:
$$
D_{CS₂} = 0.9 \times 34.09 = 30.68 \text{ kmol/h}
$$
步骤 4:计算釜液的摩尔流量
根据全塔物料衡算,原料液的摩尔流量等于馏出液和釜液的摩尔流量之和,即:
$$
F = D + W
$$
其中,W为釜液的摩尔流量。根据全塔物料衡算,原料液中二硫化碳的摩尔流量等于馏出液和釜液中二硫化碳的摩尔流量之和,即:
$$
F_{CS₂} = D_{CS₂} + W_{CS₂}
$$
其中,W_{CS₂}为釜液中二硫化碳的摩尔流量。由于要求釜液中二硫化碳的质量分数不大于0.05,因此:
$$
W_{CS₂} = 0.05 \times W
$$
将上述方程联立求解,得到:
$$
113.62 = D + W
$$
$$
34.09 = 30.68 + 0.05 \times W
$$
解得:
$$
D = 61.33 \text{ kmol/h}
$$
$$
W = 52.29 \text{ kmol/h}
$$
步骤 5:计算馏出液的组成
馏出液中二硫化碳的摩尔分数为:
$$
x_{D} = \frac{D_{CS₂}}{D} = \frac{30.68}{61.33} = 0.50
$$
原料液由二硫化碳(CS₂)和四氯化碳(CCl₄)组成,其摩尔质量分别为76 kg/kmol和154 kg/kmol。原料液中二硫化碳的质量分数为0.3,四氯化碳的质量分数为0.7。因此,原料液的平均摩尔质量MF为:
$$
MF = 0.3 \times 76 + 0.7 \times 154 = 123.2 \text{ kg/kmol}
$$
步骤 2:计算原料液的摩尔流量
原料液流量为14000 kg/h,因此原料液的摩尔流量F为:
$$
F = \frac{14000}{123.2} = 113.62 \text{ kmol/h}
$$
步骤 3:计算馏出液的摩尔流量
馏出液回收率为90%,即馏出液中二硫化碳的摩尔流量为原料液中二硫化碳摩尔流量的90%。原料液中二硫化碳的摩尔流量为:
$$
F_{CS₂} = 113.62 \times 0.3 = 34.09 \text{ kmol/h}
$$
因此,馏出液中二硫化碳的摩尔流量为:
$$
D_{CS₂} = 0.9 \times 34.09 = 30.68 \text{ kmol/h}
$$
步骤 4:计算釜液的摩尔流量
根据全塔物料衡算,原料液的摩尔流量等于馏出液和釜液的摩尔流量之和,即:
$$
F = D + W
$$
其中,W为釜液的摩尔流量。根据全塔物料衡算,原料液中二硫化碳的摩尔流量等于馏出液和釜液中二硫化碳的摩尔流量之和,即:
$$
F_{CS₂} = D_{CS₂} + W_{CS₂}
$$
其中,W_{CS₂}为釜液中二硫化碳的摩尔流量。由于要求釜液中二硫化碳的质量分数不大于0.05,因此:
$$
W_{CS₂} = 0.05 \times W
$$
将上述方程联立求解,得到:
$$
113.62 = D + W
$$
$$
34.09 = 30.68 + 0.05 \times W
$$
解得:
$$
D = 61.33 \text{ kmol/h}
$$
$$
W = 52.29 \text{ kmol/h}
$$
步骤 5:计算馏出液的组成
馏出液中二硫化碳的摩尔分数为:
$$
x_{D} = \frac{D_{CS₂}}{D} = \frac{30.68}{61.33} = 0.50
$$