题目
6.在室温下,某盛氧气钢筒内氧气压力为537.02kPa,若提用160dm^3(在101.325kPa下占的体-|||-积)的氧气后,简内压力降为131.72kPa,设温度不变,试用理想气体状态方程估计钢筒的体积。

题目解答
答案
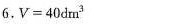
解析
步骤 1:确定理想气体状态方程
理想气体状态方程为:$PV=nRT$,其中$P$为气体压力,$V$为气体体积,$n$为气体物质的量,$R$为理想气体常数,$T$为气体温度。由于题目中温度不变,可以使用$P_1V_1=P_2V_2$来简化计算,其中$P_1$和$V_1$是初始状态的压力和体积,$P_2$和$V_2$是最终状态的压力和体积。
步骤 2:计算使用氧气后的体积变化
题目中提到,使用了160dm^3的氧气,这个体积是在101.325kPa下的体积。由于压力变化,我们需要计算这个体积在初始压力537.02kPa下的体积。使用理想气体状态方程$P_1V_1=P_2V_2$,其中$P_1=101.325kPa$,$V_1=160dm^3$,$P_2=537.02kPa$,解得$V_2$。
步骤 3:计算钢筒的体积
使用理想气体状态方程$P_1V_1=P_2V_2$,其中$P_1=537.02kPa$,$P_2=131.72kPa$,$V_2$为使用氧气后的体积,解得$V_1$,即钢筒的体积。
理想气体状态方程为:$PV=nRT$,其中$P$为气体压力,$V$为气体体积,$n$为气体物质的量,$R$为理想气体常数,$T$为气体温度。由于题目中温度不变,可以使用$P_1V_1=P_2V_2$来简化计算,其中$P_1$和$V_1$是初始状态的压力和体积,$P_2$和$V_2$是最终状态的压力和体积。
步骤 2:计算使用氧气后的体积变化
题目中提到,使用了160dm^3的氧气,这个体积是在101.325kPa下的体积。由于压力变化,我们需要计算这个体积在初始压力537.02kPa下的体积。使用理想气体状态方程$P_1V_1=P_2V_2$,其中$P_1=101.325kPa$,$V_1=160dm^3$,$P_2=537.02kPa$,解得$V_2$。
步骤 3:计算钢筒的体积
使用理想气体状态方程$P_1V_1=P_2V_2$,其中$P_1=537.02kPa$,$P_2=131.72kPa$,$V_2$为使用氧气后的体积,解得$V_1$,即钢筒的体积。