对金属而言,六方晶体结构为最紧密堆积,而体心立方为次紧密堆积,原子间距应该增大。六方密堆积 体心立方假设体系中共包含n个Fe原子,则会形成n/6个六方晶胞,每个晶胞体积为V,Fe原子半径为r,形成n/2个体心立方晶胞,每个晶胞体积为V,每个Fe原子半径为r,则:;其中, ,;对体心立方:,, ;计算:得 也就是说,结构中原子中心间距减小了3.06%;2.14 氯化铯(CsCl)晶体属于立方结构。假设Cs和Cl沿立方对角线接触,且Cs半径为0.170nm,Cl半径为0.181nm,试计算氯化铯晶体结构中离子的堆积密度,并结合紧密堆积结构的堆积密度对其结构特点进行讨论。答:氯化铯是简立方结构且Cs和Cl沿立方体对角线接触,因此,,,氯化铯晶胞中氯原子个数为,铯原子个数为,二者体积为所以离子的堆积密度为。其堆积密度小于最紧密堆积密度74%,这是因为Cs离子半径较大无法填充到Cl离子做最紧密排列形成的八面体间隙中,导致Cl被撑开,由6配位变成8配位,晶体结构也由面心立方变成体心立方。2.15氧化锂(LiO)的晶体结构可看成由O按面心立方密堆,Li占据其四面体空隙中。若Li半径为0.074nm,O半径为0.140nm,试计算:(1)LiO的晶胞常数;(2)LiO晶体质量密度;(3)O密堆积所形成的空隙能容纳阳正离子的最大半径是多少?
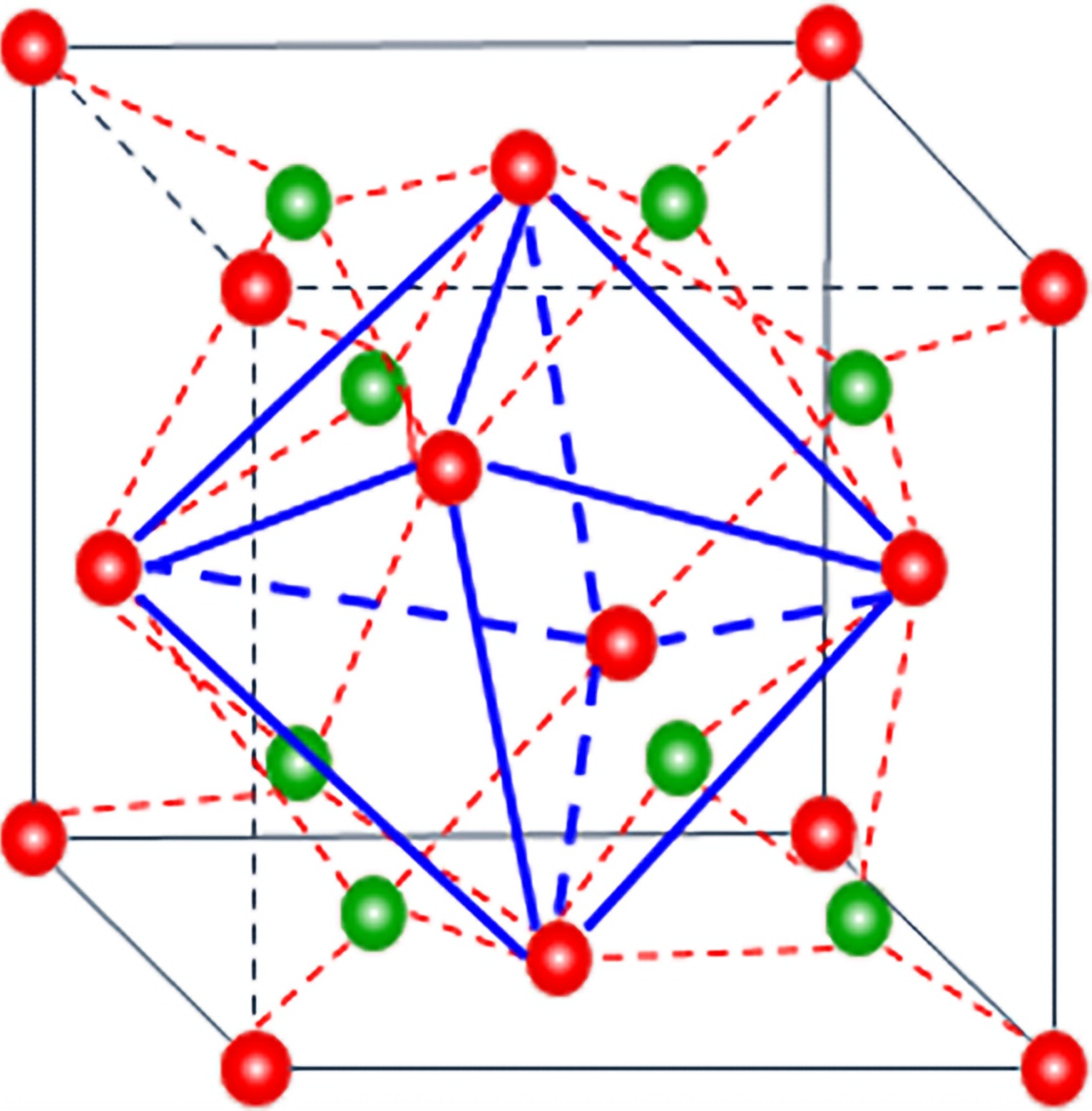
对金属而言,六方晶体结构为最紧密堆积,而体心立方为次紧密堆积,原子间距应该增大。

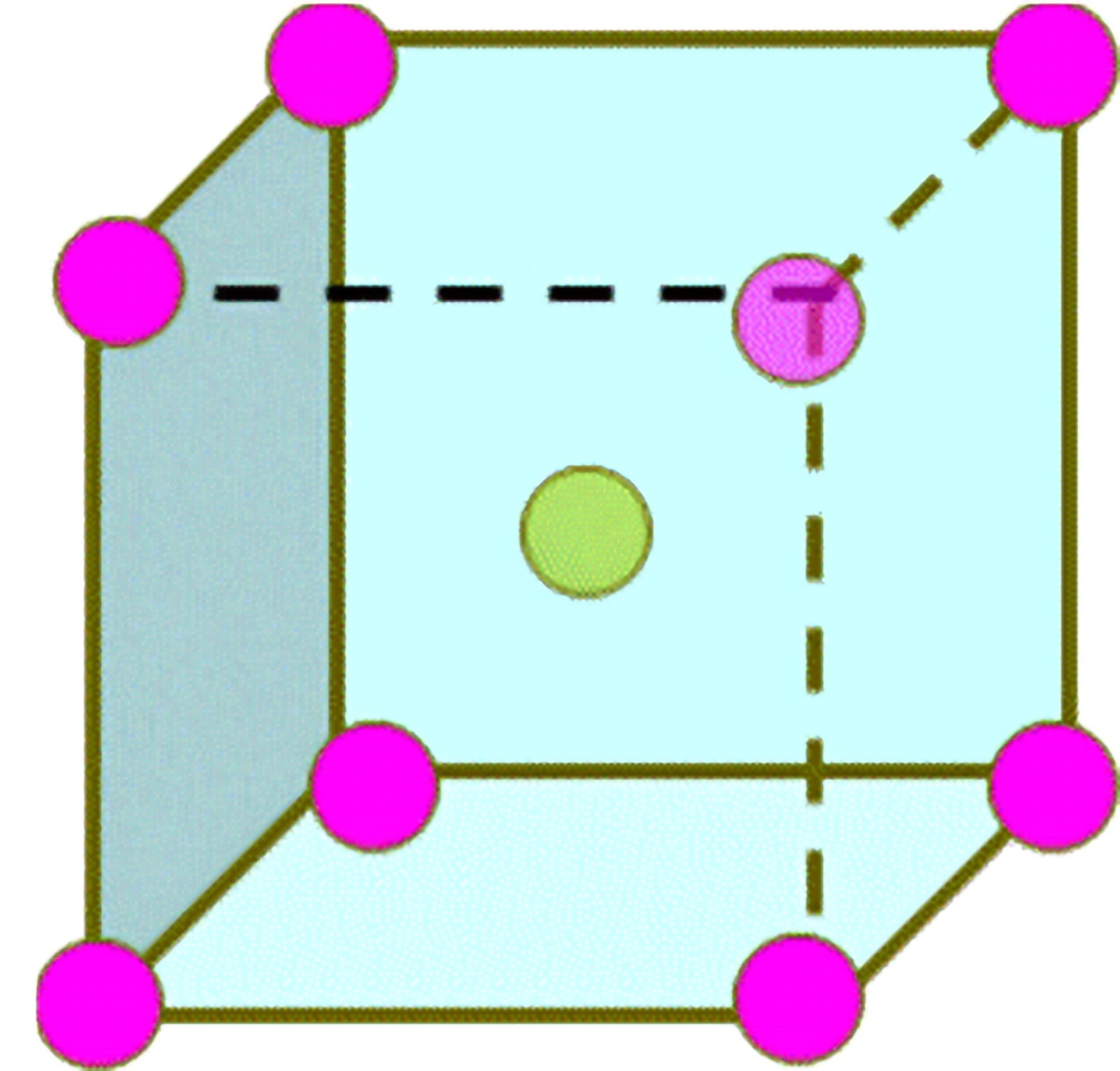
六方密堆积 体心立方
假设体系中共包含n个Fe原子,则会形成n/6个六方晶胞,每个晶胞体积为V,Fe原子半径为r,形成n/2个体心立方晶胞,每个晶胞体积为V,每个Fe原子半径为r,则:
;
其中,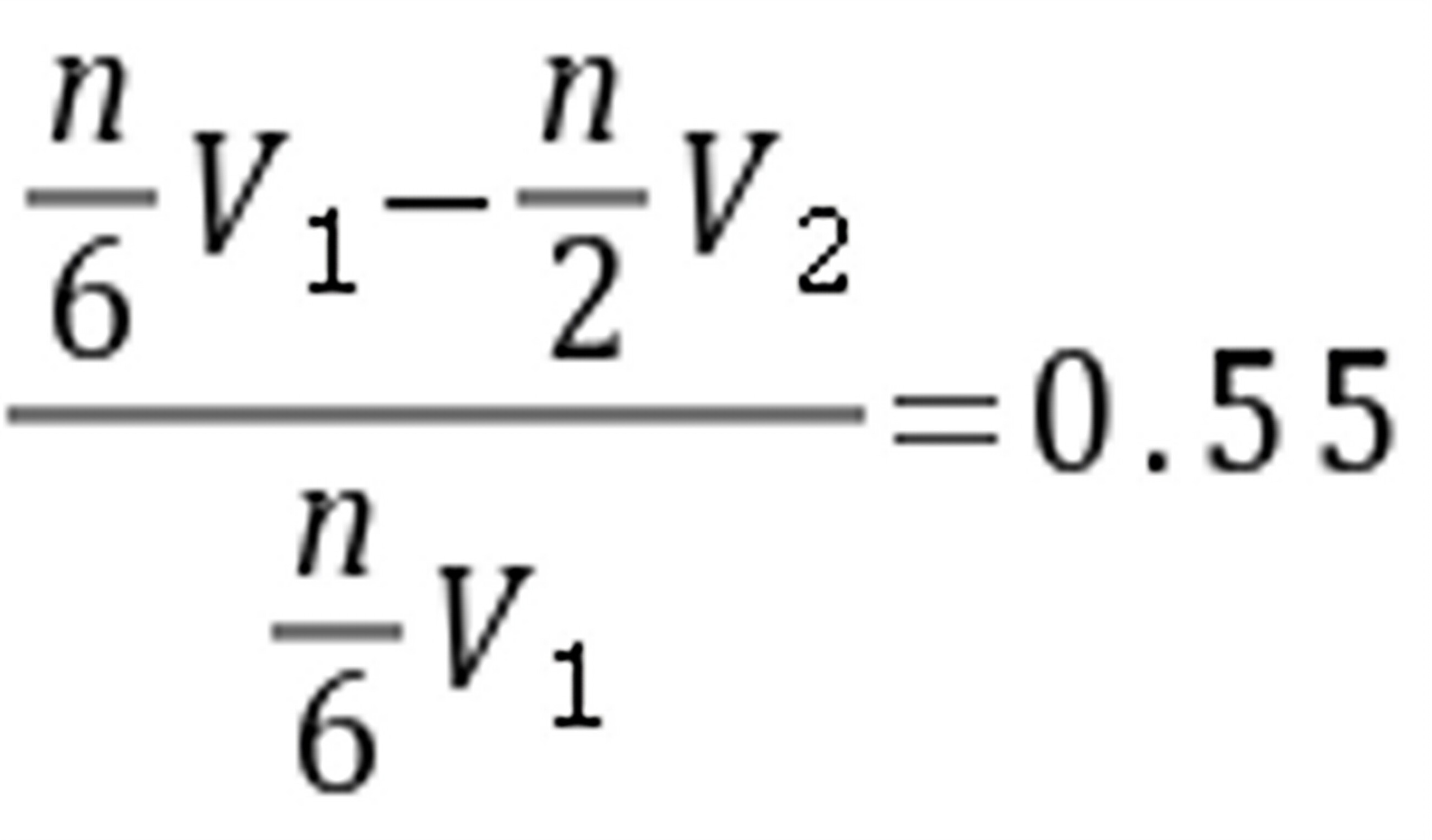 ,;
,;
对体心立方: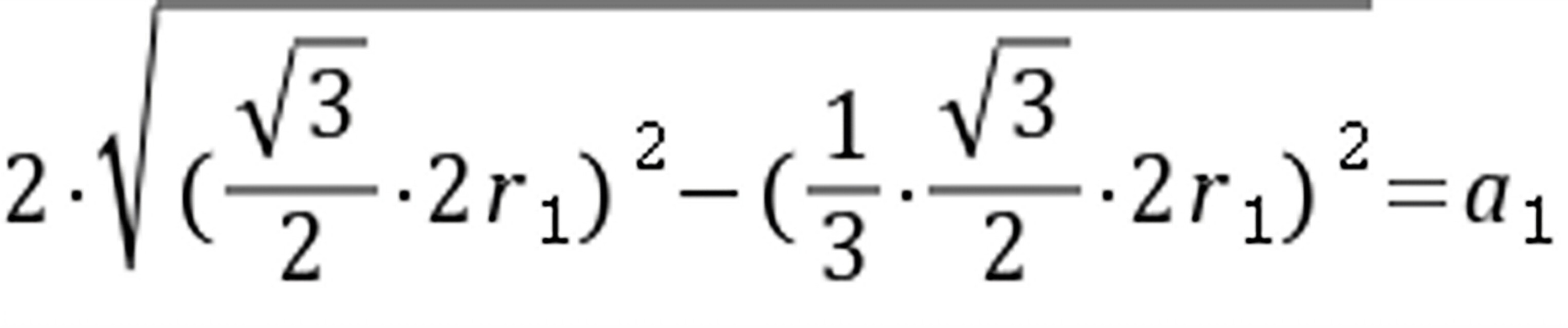 ,
,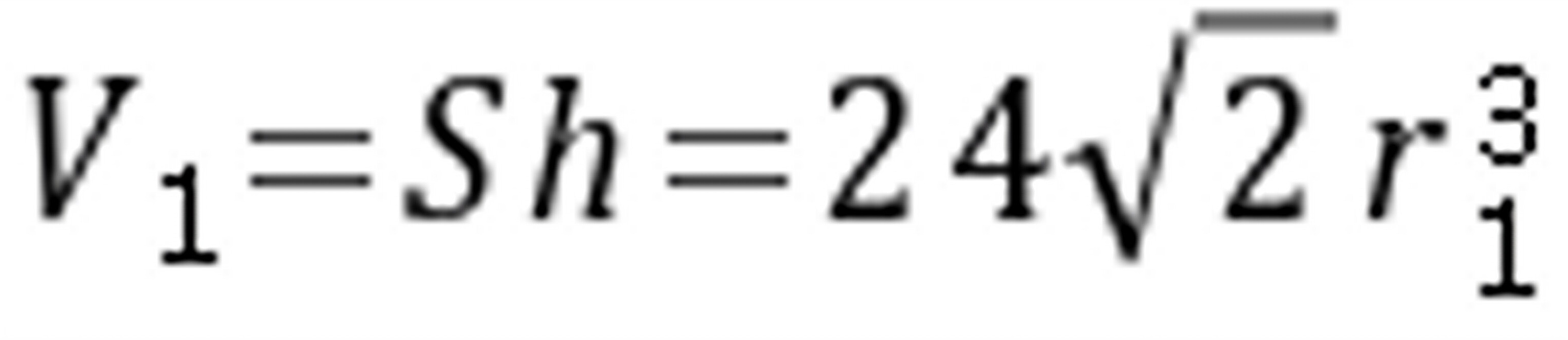 , ;
, ;
计算: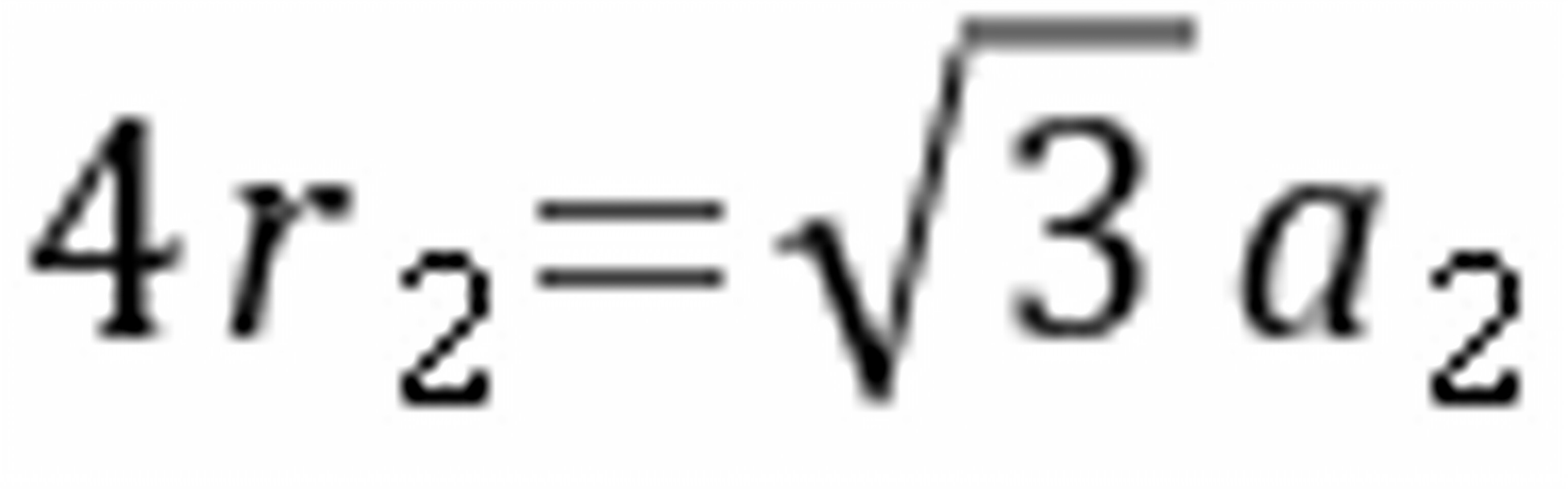
得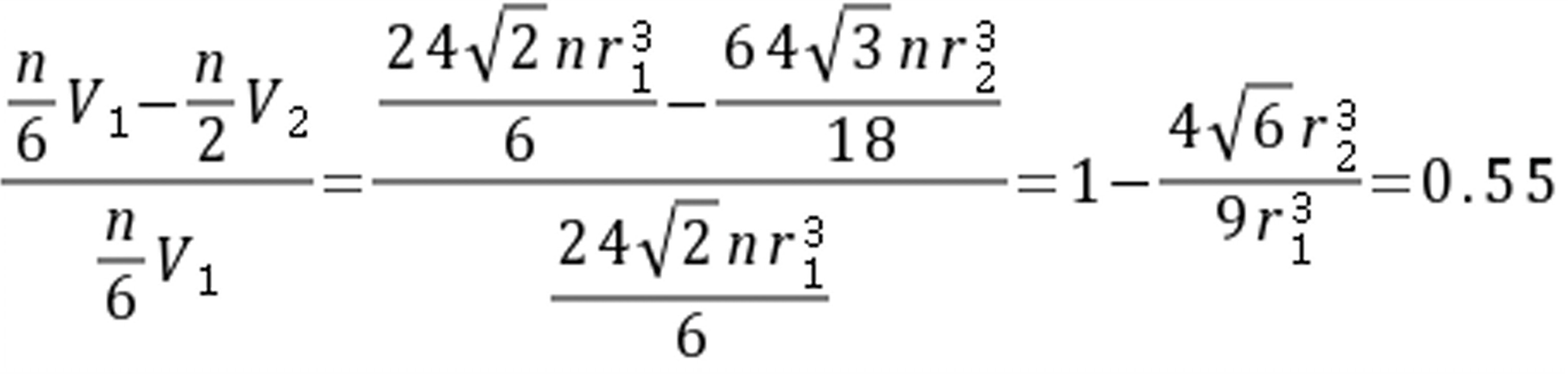 也就是说,结构中原子中心间距减小了3.06%;
也就是说,结构中原子中心间距减小了3.06%;
2.14 氯化铯(CsCl)晶体属于立方结构。假设Cs和Cl沿立方对角线接触,且Cs半径为0.170nm,Cl半径为0.181nm,试计算氯化铯晶体结构中离子的堆积密度,并结合紧密堆积结构的堆积密度对其结构特点进行讨论。
答:
氯化铯是简立方结构且Cs和Cl沿立方体对角线接触,因此,
,,
氯化铯晶胞中氯原子个数为,铯原子个数为,
二者体积为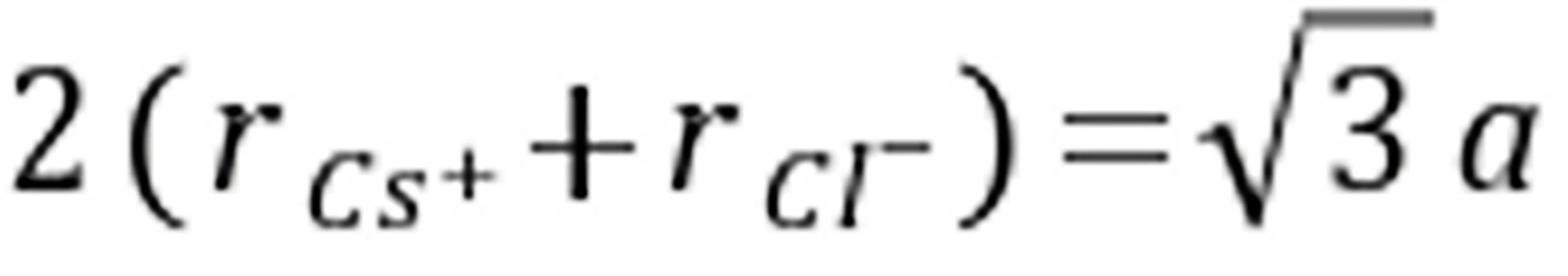
所以离子的堆积密度为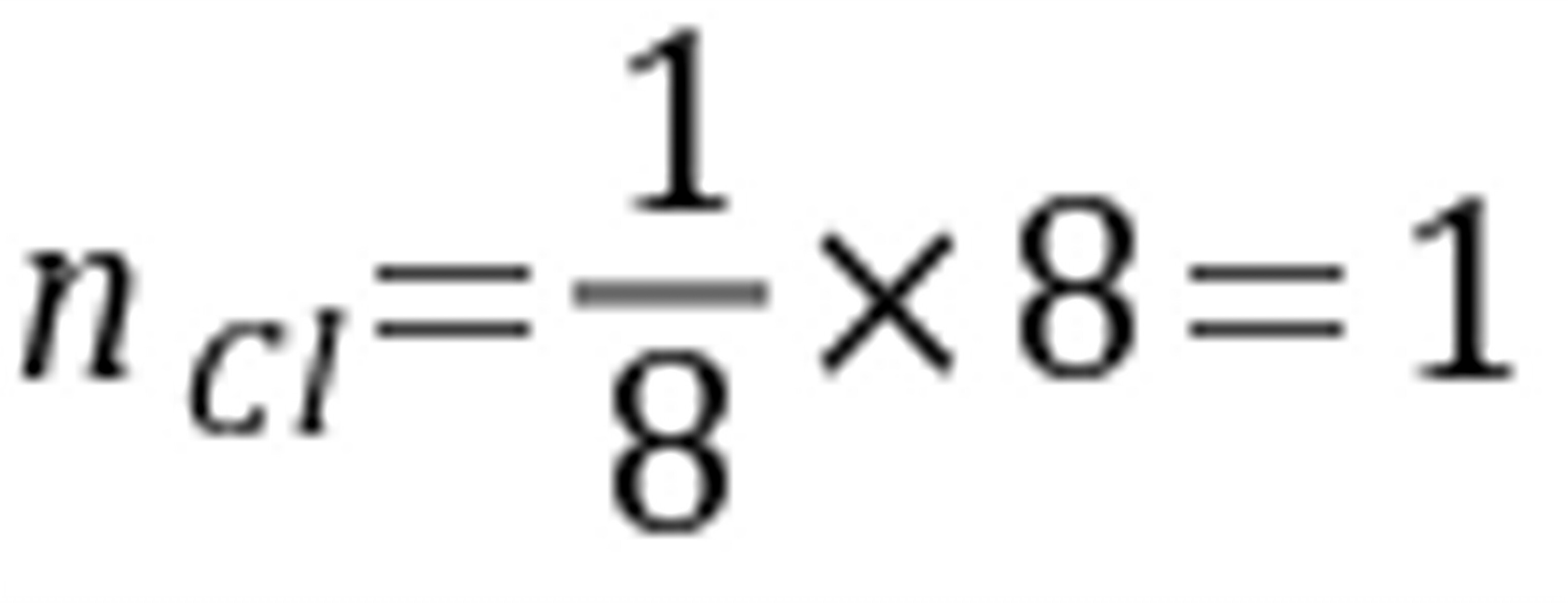 。
。
其堆积密度小于最紧密堆积密度74%,这是因为Cs离子半径较大无法填充到Cl离子做最紧密排列形成的八面体间隙中,导致Cl被撑开,由6配位变成8配位,晶体结构也由面心立方变成体心立方。
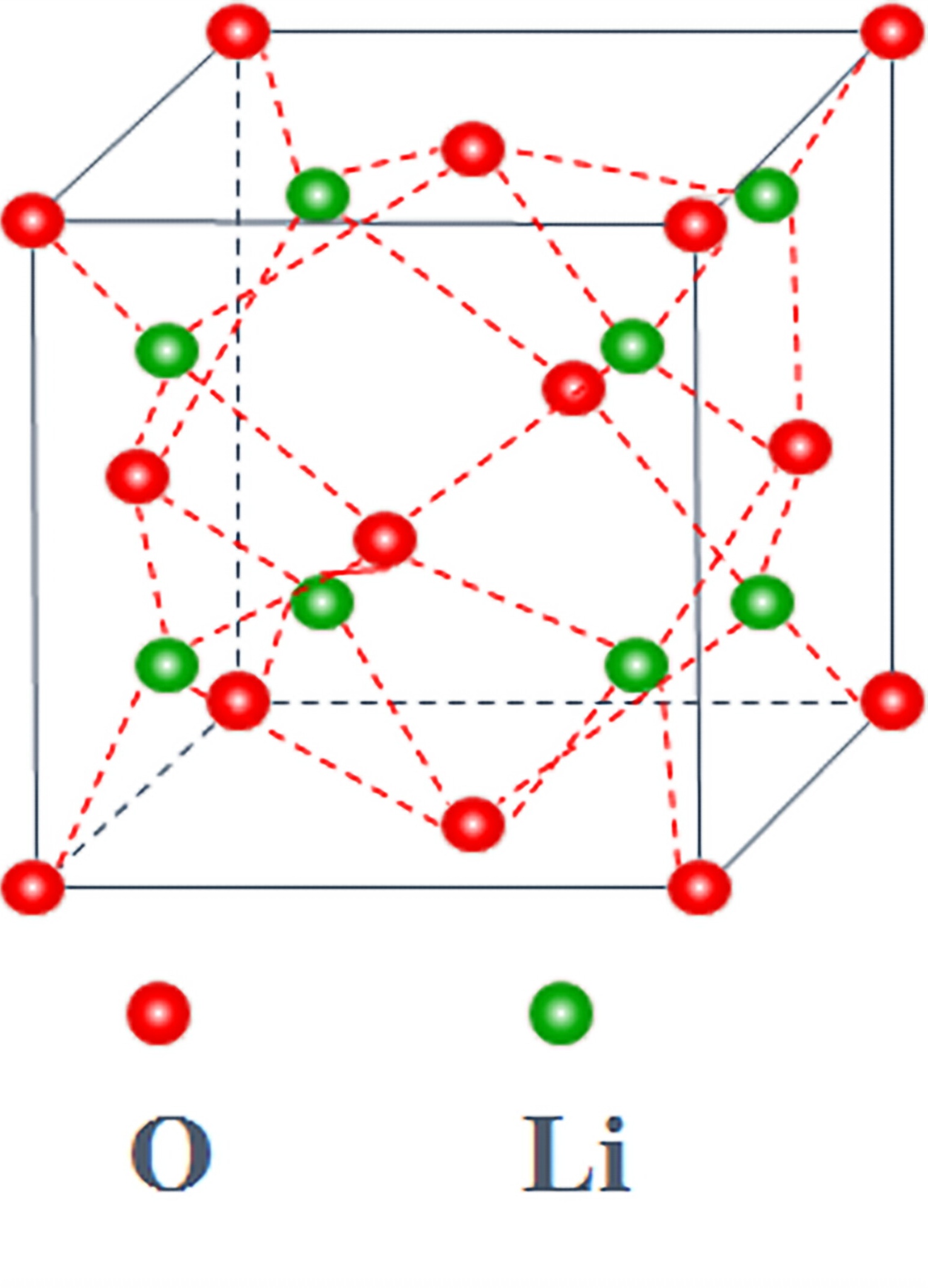
2.15氧化锂(LiO)的晶体结构可看成由O按面心立方密堆,Li占据其四面体空隙中。若Li半径为0.074nm,O半径为0.140nm,试计算:(1)LiO的晶胞常数;(2)LiO晶体质量密度;(3)O密堆积所形成的空隙能容纳阳正离子的最大半径是多少?
题目解答
答案
解:(1)。Li2O 是反萤石结构(萤石结构中阴、阳离子的位置完全互换),由于O2-按面心立方密堆,则单个晶胞中含有4个O,8个Li。O离子的面心立方密堆中四面体空隙全部被Li占据,O离子的配位数为8,位于8个锂离子形成的小立方体体心位置。
则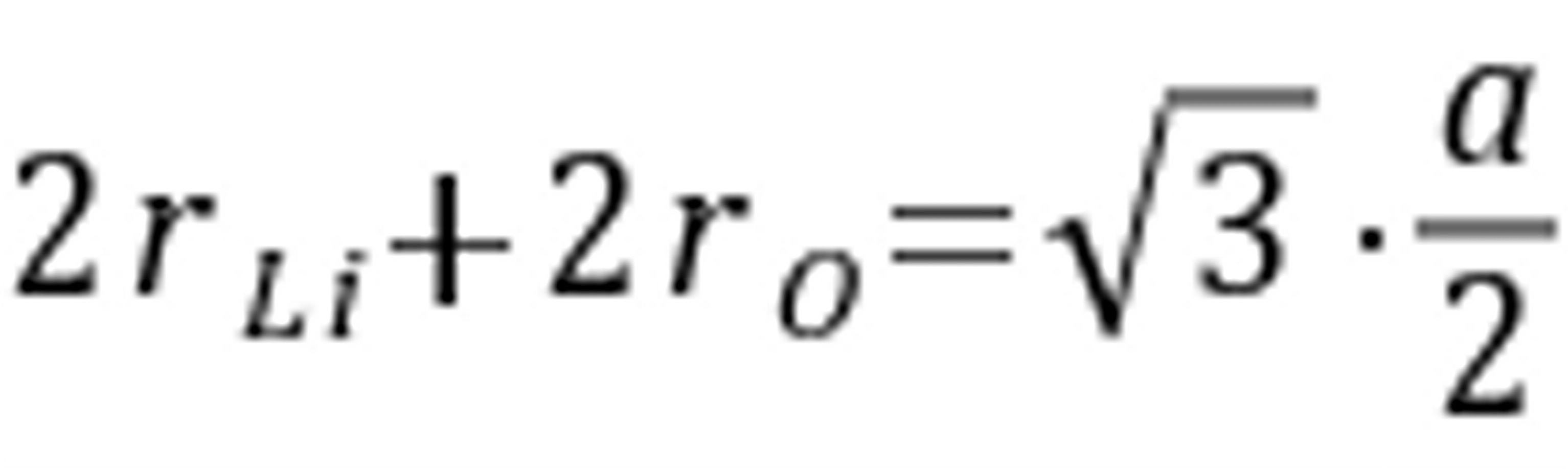 ,
,
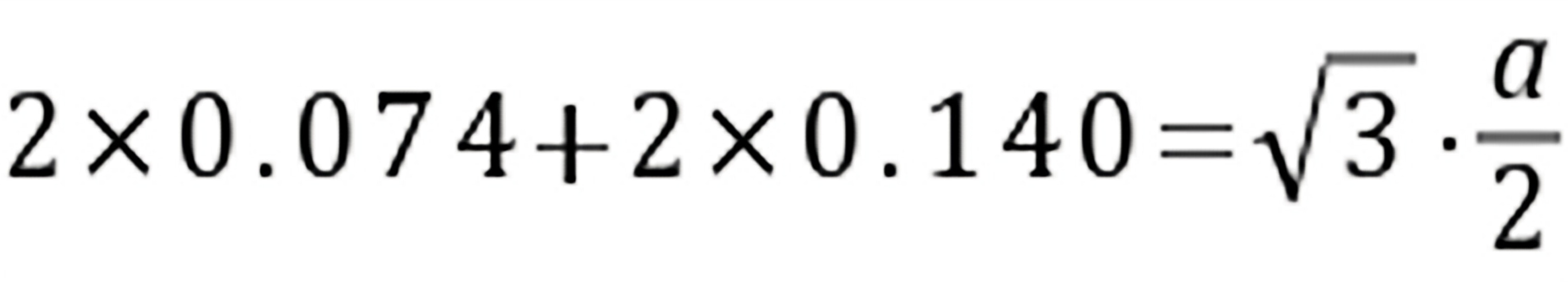 ,
,
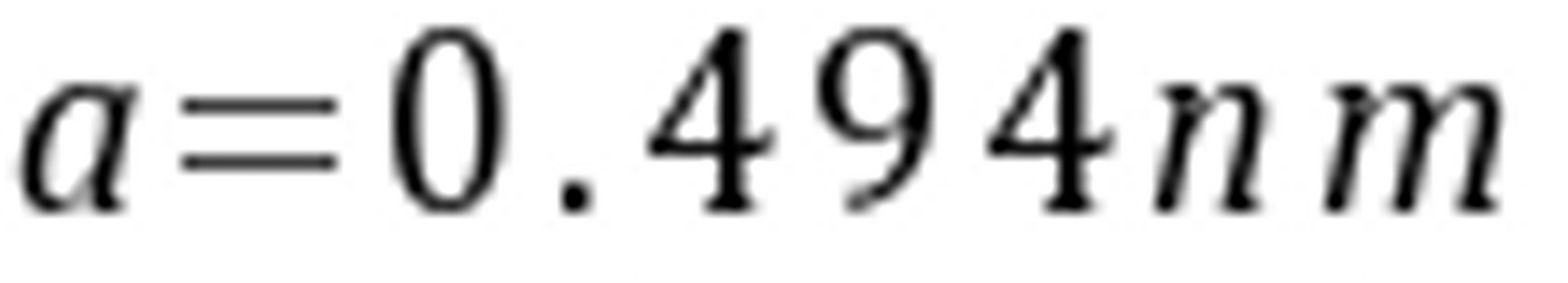
(2)单个晶胞体积为: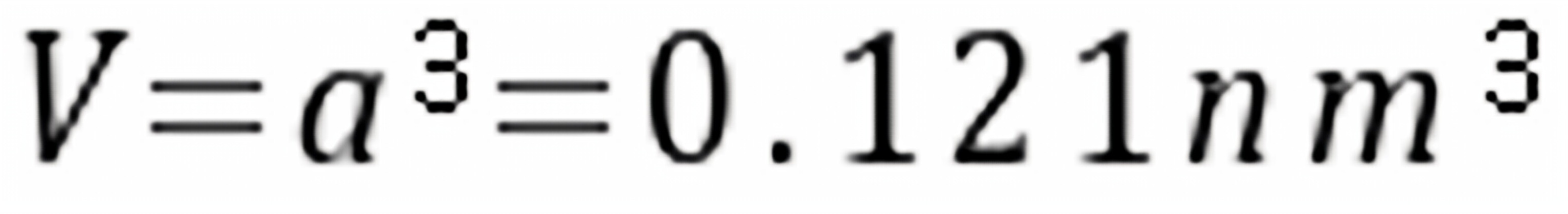 ,
,
晶胞质量为: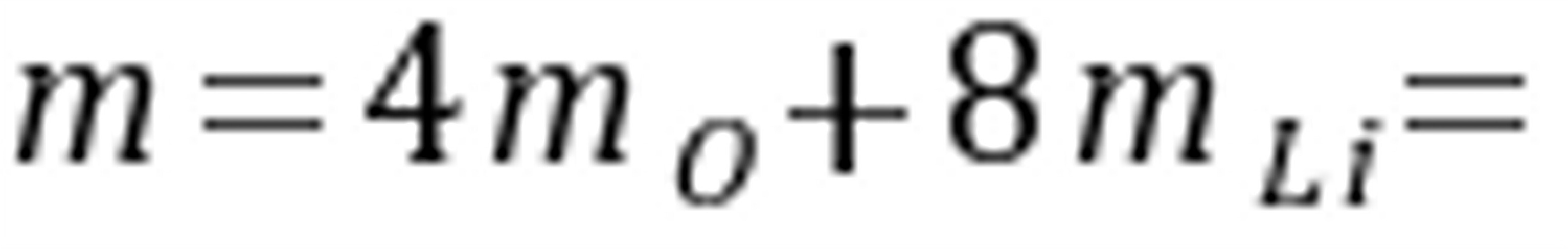
Li2O晶体质量密度为: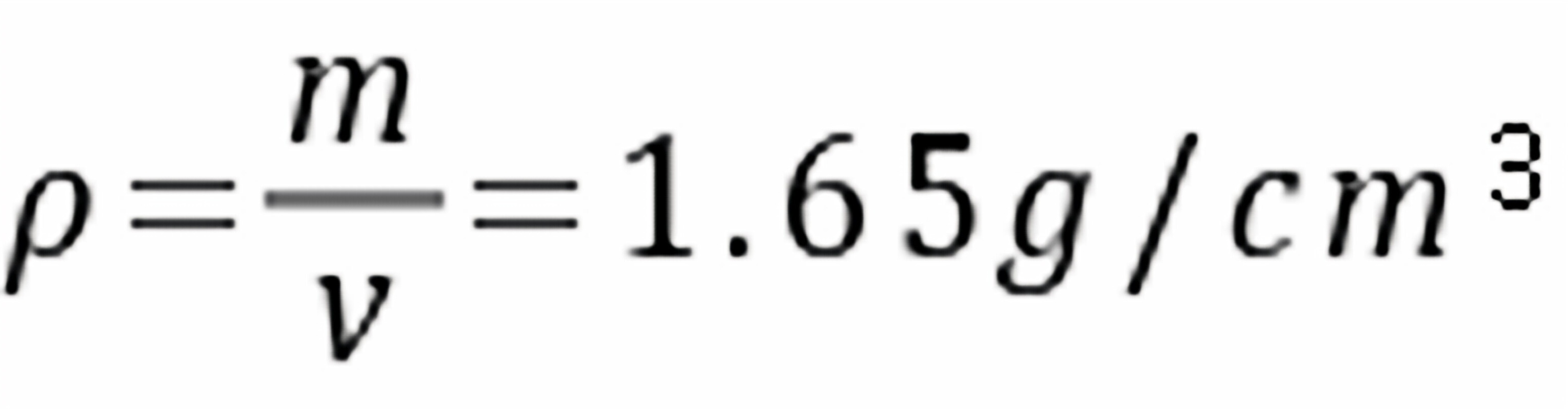
(3)O离子做六方密堆积,可形成四面体空隙和八面体空隙。八面体空隙最大,如果填入的阳离子M的刚好与O离子接触的话,则
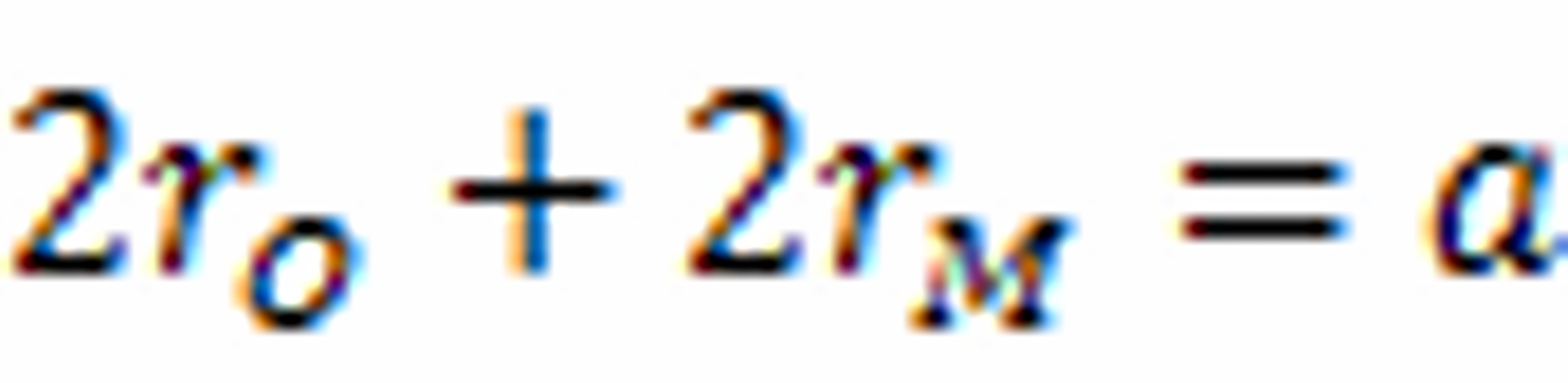
即,
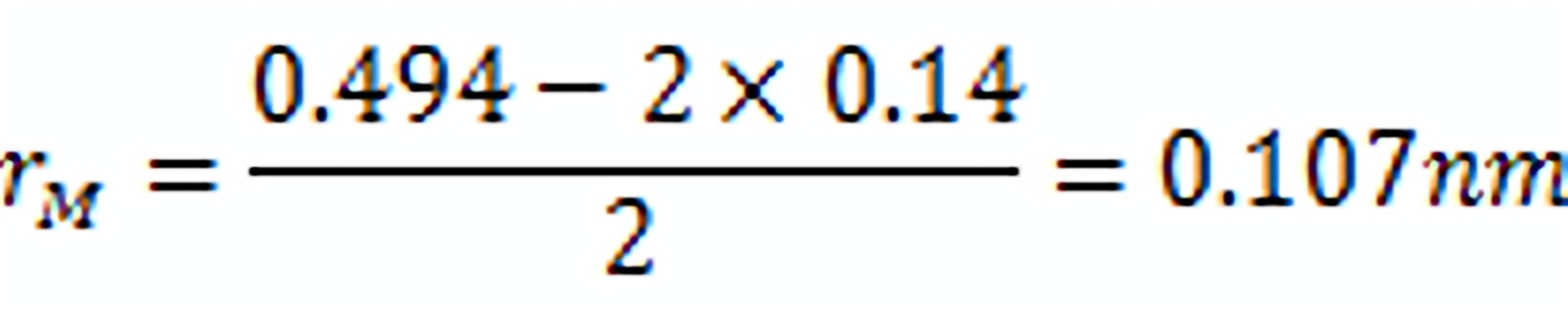
可见,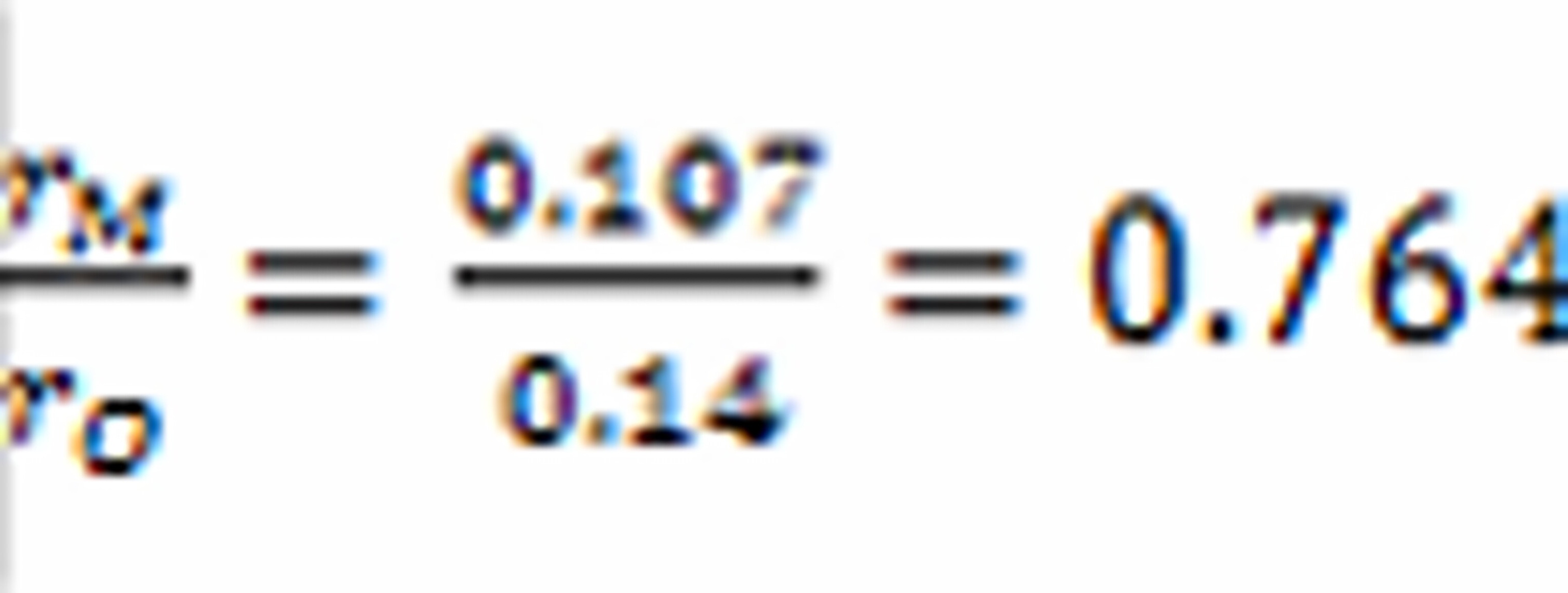 ,符合形成八面体配位的条件。
,符合形成八面体配位的条件。