题目
用清水在塔中逆流吸收混于空气中的二氧化硫。已知混合气中二氧化硫的体积分数为0.,操作条件下物系的相平衡常数为26.7,载气的流量为250 kmol/h。若吸收剂用量为最小用量的1.55倍,要求二氧化硫的回收率为92%。试求水的用量(kg/h)及所需理论级数。
用清水在塔中逆流吸收混于空气中的二氧化硫。已知混合气中二氧化硫的体积分数为0.,操作条件下物系的相平衡常数为26.7,载气的流量为250 kmol/h。若吸收剂用量为最小用量的1.55倍,要求二氧化硫的回收率为92%。试求水的用量(kg/h)及所需理论级数。
题目解答
答案
解: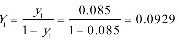
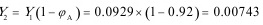
用清水吸收,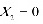
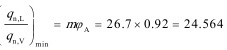
操作液气比为
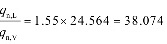
水的用量为
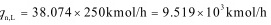
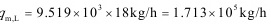
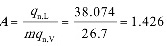
用清水吸收,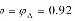
由 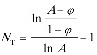
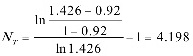
解析
步骤 1:计算混合气中二氧化硫的摩尔分数
混合气中二氧化硫的体积分数为0.085,因此其摩尔分数${y}_{1}$为0.085。
步骤 2:计算吸收后混合气中二氧化硫的摩尔分数
根据题目要求,二氧化硫的回收率为92%,因此吸收后混合气中二氧化硫的摩尔分数${y}_{2}$为${y}_{1}(1-{\varphi }_{A})=0.085\times (1-0.92)=0.00743$。
步骤 3:计算最小液气比
操作条件下物系的相平衡常数为26.7,因此最小液气比${q}_{n}v$为26.7。
步骤 4:计算实际液气比
题目中给出吸收剂用量为最小用量的1.55倍,因此实际液气比${q}_{m}$为$1.55\times 26.7=41.385$。
步骤 5:计算水的用量
水的用量为${q}_{m}\times {T}_{n}=41.385\times 250kmol/h=10.346\times {10}^{3}kmoln$,换算成质量为$10.346\times {10}^{3}\times 18kg/h=1.862\times {10}^{5}kg/h$。
步骤 6:计算所需理论级数
根据公式${N}_{r}=\dfrac {\ln \dfrac {1.426-0.92}{1.029}}{\ln 1.426}-1$,计算出所需理论级数${N}_{r}$为4.198。
混合气中二氧化硫的体积分数为0.085,因此其摩尔分数${y}_{1}$为0.085。
步骤 2:计算吸收后混合气中二氧化硫的摩尔分数
根据题目要求,二氧化硫的回收率为92%,因此吸收后混合气中二氧化硫的摩尔分数${y}_{2}$为${y}_{1}(1-{\varphi }_{A})=0.085\times (1-0.92)=0.00743$。
步骤 3:计算最小液气比
操作条件下物系的相平衡常数为26.7,因此最小液气比${q}_{n}v$为26.7。
步骤 4:计算实际液气比
题目中给出吸收剂用量为最小用量的1.55倍,因此实际液气比${q}_{m}$为$1.55\times 26.7=41.385$。
步骤 5:计算水的用量
水的用量为${q}_{m}\times {T}_{n}=41.385\times 250kmol/h=10.346\times {10}^{3}kmoln$,换算成质量为$10.346\times {10}^{3}\times 18kg/h=1.862\times {10}^{5}kg/h$。
步骤 6:计算所需理论级数
根据公式${N}_{r}=\dfrac {\ln \dfrac {1.426-0.92}{1.029}}{\ln 1.426}-1$,计算出所需理论级数${N}_{r}$为4.198。