草酸作为一种重要的化工原料,某学习小组的同学拟以甘蔗渣为原料用水解一氧化一水解技术制取草酸。 滴入一定浓度的硝酸-|||-粉碎的甘蔗渣50g → 硫酸浸泡 → ..... 在反应器中搅拌,控制温度-|||-① ②-|||-草酸水合物 ← 粗品 抽滤 .← 升温到t℃,保温数小时得到草酸-|||-⑤ ④ Ⅰ、步骤④是减压抽滤(见下图),其优点是:__________________________________________, 当抽滤完毕或中途停止抽滤时,为了防止自来水倒吸入B装置,最佳的操作是___________。 滴入一定浓度的硝酸-|||-粉碎的甘蔗渣50g → 硫酸浸泡 → ..... 在反应器中搅拌,控制温度-|||-① ②-|||-草酸水合物 ← 粗品 抽滤 .← 升温到t℃,保温数小时得到草酸-|||-⑤ ④ Ⅱ、该小组同学为了确定产品H 2 C 2 O 4 ·xH 2 O中的的x值,进行下列实验: ①取w g产品配成100mL水溶液; ②量取25.00mL草酸溶液置于锥形瓶中,加入适量稀H 2 SO 4 后,用浓度为c mol·L -1 KMnO 4 溶液滴定。 请回答下列问题: (1)实验①中,需要用到的玻璃仪器有:玻璃棒、烧杯、胶头滴管和___________。 (2)写出草酸溶液与酸性高锰酸钾溶液反应的离子方程式:_____________________________。 (3)若滴定时,前后两次读数分别为a mL和b mL,由此计算出该草酸晶体的x值是__________ Ⅲ、该小组同学在做实验Ⅱ②时发现向草酸溶液中逐滴加入高锰酸钾溶液时,溶液褪色总是先慢后快,即反应速率由小变大。为此,他们设计了实验进行探究: 【实验用品】 仪器:试管(若干个并编号①,②,③…)、胶头滴管(若干支)、秒表 试剂:0.1 mol/L H 2 C 2 O 4 溶液、0.1 mol/L KMnO 4 溶液、稀硫酸、MnSO 4 固体 【实验内容】 实验(1):在①号和②号试管中分别先加入5m1 0.1mol/L H 2 C 2 O 4 溶液,然后各加10滴稀硫酸,且在②号试管中加入少量硫酸锰固体。再在两支试管中各加入5滴0.1mol/LKMnO 4 溶液。现象如下(表1) 编号 ①号试管 ②号试管 褪色时间 90s 5 s 实验现象 均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 实验(2):在①号和②号试管中分别加入5m1 0.1mol/L H 2 C 2 O 4 溶液,在②号试管中再滴加l0滴稀硫酸,然后在两支试管中各加入5滴0.1 mol/L 的高锰酸钾溶液。现象如下(表2) 编号 ①号试管 ②号试管 褪色时间 100 s 90 s 实验现象 均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 实验(3):在①号、②号和③号试管中分别加入5m1 0.1mol/L H 2 C 2 O 4 溶液,然后在①、②、③号试管中依次加入10滴、l mL、2 mL稀硫酸溶液,然后各加入5滴0.1 mol/L的高锰酸钾溶液,然后置于温度为65℃的水浴中加热。观察现象如下(表3)。 编号 ①号试管 ②号试管 ③号试管 褪色时间 88 s 100 s 120 s 实验现象 均有气泡产生;①号试管的溶液褪色比②、③号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 (1)设计实验(1)对应的假设是_________________________________________________。 实验(1)得出的结论是____________________________________________________。 (2)由实验(2)和实验(3)得出的结论是_________________________________________m___。
草酸作为一种重要的化工原料,某学习小组的同学拟以甘蔗渣为原料用水解一氧化一水解技术制取草酸。
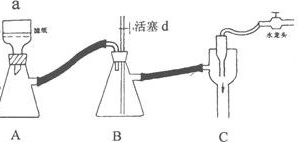
Ⅰ、步骤④是减压抽滤(见下图),其优点是:__________________________________________, 当抽滤完毕或中途停止抽滤时,为了防止自来水倒吸入B装置,最佳的操作是___________。
Ⅱ、该小组同学为了确定产品H 2 C 2 O 4 ·xH 2 O中的的x值,进行下列实验:
①取w g产品配成100mL水溶液;
②量取25.00mL草酸溶液置于锥形瓶中,加入适量稀H 2 SO 4 后,用浓度为c mol·L -1 KMnO 4 溶液滴定。 请回答下列问题:
(1)实验①中,需要用到的玻璃仪器有:玻璃棒、烧杯、胶头滴管和___________。
(2)写出草酸溶液与酸性高锰酸钾溶液反应的离子方程式:_____________________________。
(3)若滴定时,前后两次读数分别为a mL和b mL,由此计算出该草酸晶体的x值是__________
Ⅲ、该小组同学在做实验Ⅱ②时发现向草酸溶液中逐滴加入高锰酸钾溶液时,溶液褪色总是先慢后快,即反应速率由小变大。为此,他们设计了实验进行探究:
【实验用品】 仪器:试管(若干个并编号①,②,③…)、胶头滴管(若干支)、秒表
试剂:0.1 mol/L H 2 C 2 O 4 溶液、0.1 mol/L KMnO 4 溶液、稀硫酸、MnSO 4 固体
【实验内容】
实验(1):在①号和②号试管中分别先加入5m1 0.1mol/L H 2 C 2 O 4 溶液,然后各加10滴稀硫酸,且在②号试管中加入少量硫酸锰固体。再在两支试管中各加入5滴0.1mol/LKMnO 4 溶液。现象如下(表1)
| 编号 |
①号试管 |
②号试管 |
| 褪色时间 |
90s |
5 s |
| 实验现象 |
均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
|
| 编号 |
①号试管 |
②号试管 |
| 褪色时间 |
100 s |
90 s |
| 实验现象 |
均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
|
| 编号 |
①号试管 |
②号试管 |
③号试管 |
| 褪色时间 |
88 s |
100 s |
120 s |
| 实验现象 |
均有气泡产生;①号试管的溶液褪色比②、③号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
||
实验(1)得出的结论是____________________________________________________。
(2)由实验(2)和实验(3)得出的结论是_________________________________________m___。
题目解答
答案
(16分)Ⅰ、加快过滤速度、得到较干燥的沉淀;慢慢打开活塞d,然后关闭水龙头; (2分+2分)
Ⅱ、(1)100mL容量瓶(1分) (2)5 H 2 C 2 O 4 +2MnO 4 - +6H + =2Mn 2+ +10CO 2 ↑+8H 2 O(2分) (3) 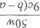 -5 (2分)
-5 (2分)
Ⅲ、(1)假设:反应产物中的Mn 2+ 可能是反应的催化剂;(2分)
结论:Mn 2+ 在反应中起到催化剂的作用,加快了反应速率;假设1成立。(2分)
(2)由表2和表3的实验结果可知:硫酸对草酸和高锰酸钾溶液的反应有影响。加入少量硫酸,可以促进草酸和高锰酸钾溶液的反应,而加入大量硫酸,草酸和高锰酸钾溶液的反应速率开始比较慢,随着反应的进行,褪色速率加快;(2分)温度对该反应速率影响不大。(1分)(其他合理答案也可以酌情给分)
解析