题目
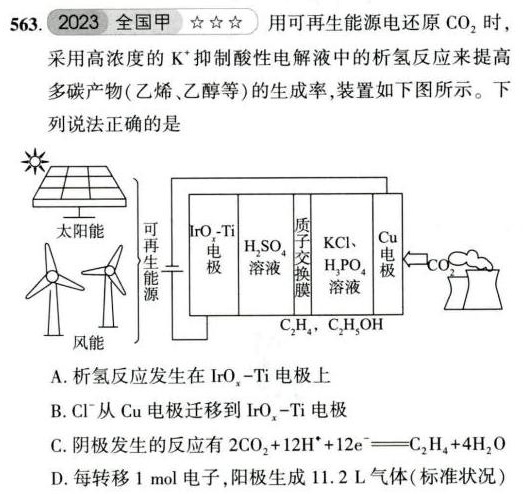
563.2023全国甲 ☆☆☆ 用可再生能源电还原CO2时,-|||-采用高浓度的 +3 抑制酸性电解液中的析氢反应来提高-|||-多碳产物(乙烯、乙醇等)的生成率,装置如下图所示。下-|||-列说法正确的是-|||-太阳能 可 T rO-Til H2SO4 周 KCl、 极-|||-溶液 H3PO4-|||-溶液-|||-C2H4 C 2H5OH-|||-风能-|||-A.析氢反应发生在 _(r)(O)_(x)-(I)_(1) 电极上-|||-B. (H)^- 从Cu电极迁移到 _(r)(O)_(x)-Ii 电极-|||-C.阴极发生的反应有 (O)_(2)+12(H)^++12(e)^-=!=!= (C)_(2)(H)_(4)+4(H)_(2)O-|||-D.每转移1 mol电子,阳极生成11.2L气体(标准状况)
题目解答
答案

解析
考查要点:本题主要考查电解池的工作原理,包括电极判断、离子迁移规律、电极反应式的书写及电子转移与气体体积的关系。
解题核心思路:
- 判断电极类型:根据装置图中材料差异,Cu为阴极,LnxOy-Ti为阳极。
- 析氢反应的位置:析氢反应属于还原反应,必然发生在阴极。
- 离子迁移规律:质子交换膜仅允许H⁺通过,Cl⁻无法跨膜迁移。
- 电极反应式的配平:阴极CO₂转化为C₂H₄,需配平电荷与原子。
- 电子转移与气体体积关系:阳极生成O₂,根据反应式计算气体体积。
破题关键点:
- 阴极反应的还原性:析氢反应和CO₂还原均在阴极发生,但高浓度K⁺抑制析氢反应,优先生成多碳产物。
- 质子交换膜的选择性:Cl⁻无法通过膜,排除B选项。
- 阳极反应的产物:阳极水的氧化生成O₂,而非析氢。
选项A分析
析氢反应(2H⁺ + 2e⁻ → H₂↑)是还原反应,必然发生在阴极(Cu电极),而非阳极(LnxOy-Ti电极)。因此A错误。
选项B分析
装置中质子交换膜仅允许H⁺通过,Cl⁻无法从Cu电极迁移到阳极。因此B错误。
选项C分析
阴极CO₂被还原生成C₂H₄的反应为:
$2\text{CO}_2 + 12\text{H}^+ + 12\text{e}^- \rightarrow \text{C}_2\text{H}_4 + 4\text{H}_2\text{O}$
该反应符合题目中“多碳产物(如乙烯)生成”的描述,C正确。
选项D分析
阳极反应为水的氧化:
$2\text{H}_2\text{O} - 4\text{e}^- \rightarrow \text{O}_2 + 4\text{H}^+$
每转移1 mol电子,生成0.25 mol O₂,对应体积为:
$0.25 \, \text{mol} \times 22.4 \, \text{L/mol} = 5.6 \, \text{L}$
而非11.2 L,因此D错误。