题目
[典型例题]类型一、化学实验基本方法例1.下列实验能达到目的的是( )。A. 在容量瓶中加一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸 B. 用稀硫酸和锌粒反应制氢气 C. 用玻璃棒搅拌漏斗中的液体以加快过滤的速度 D. 加入盐酸以除去硫酸钠中的少量碳酸钠杂质 E. [思路点拨]运用化学实验的基本方法逐项分析各选项的说法是否正确,特别是要注意对实验操作的描述是否准确。 F. [总结升华] 此类题型宜采用逐项分析法。 G. 举一反三: [变式1]下列实验操作与安全事故处理错误的是( ) A.使用温度计测量烧杯中的水浴温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶,残破的温度计插入装有硫粉的广口瓶中 B.用试管夹从试管底由下往上夹住距离管口约dfrac (1)(3)处,手持试管夹长柄末端,进行加热 C.将浓硫酸放入容量瓶中,然后加水稀释制取稀硫酸 D.把玻管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻管插入端,缓慢旋进塞孔中 类型二、混合物分离和提纯的常用方法 a2+、Mg2+、Fe3+、SO42―杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下: dfrac (1)(3) 的名称是____________,所用玻璃仪器是________________________________。 (2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的沉淀,则试剂甲为________溶液。 (3)在第Ⅴ步中,加入试剂丁直到溶液无明显变化时,写出此过程的化学方程式________________。 [总结升华]看似比较大的实验题,往往问题都设在一些小的基本操作,所以做好此类题要注意两点:其一要从宏观把握整个实验方案,其二是准确规范地表述基本操作。 举一反三: [变式1]关于粗盐提纯的下列说法正确的是( ) A.溶解粗盐时,应尽量使溶液稀些,防止食盐不完全溶解 B.滤去不溶性杂质后,将滤液移至坩埚内加热浓缩 C.当蒸发到剩有少量液体时,停止加热利用余热将液体蒸干 D.将制得的晶体转移到新制过滤器中用大量水进行洗涤 [变式2] (1)除去NaNO3固体中混有的少量KNO3,所进行的实验操作依次为________、蒸发、结晶、________。 (2)除去KCl溶液中的SO42-,依次加入的溶液为(填溶质的化学式)__________________。 类型三、物质的量——化学计算的桥梁 NA代表阿伏加德罗常数,下列叙述错误的是( )。 10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% 在H2O2+Cl2==2HCl+O2反应中,每生成32 g氧气,则消耗NA个Cl2分子 标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g 一定温度下,1 L 0.50 mol·L-1 NaCl溶液与2 L 0.25 mol·L-1 Na2CO3溶液含Na+的物质的量不同 [思路点拨]逐选项分析该选项中涉及到的物理量之间的关系,计算时要留心有关细节的说法是否正确。 [总结升华]正误判断题是化学高考命题的热点之一,常见的命题设错角度有:(1)概念的内涵、外延有漏洞;(2)问题叙述忽略特例,如有“都是”“一定”“全部”等较绝对的词;(3)在概念或物理量的“单位”上设错,如“摩尔质量”的单位设作“g”;(4)推论错误;(5)不考虑条件,如“标准状况”“常温”;(6)计算错误;(7)违背有关定律。如“质量守恒定律”、“电荷守恒”、“阿伏加德罗定律”等;(8)概念的运用错误。在分析判断时要关注以上各点。 举一反三: [变式1]下列叙述错误的是( ) A.0.012 kg的12C所含的原子数为6.02×1023 B.1 mol H2O中含有2 mol H和1 mol O C.2 mol NaOH溶于1 L水中配成溶液的浓度为2 mol·L―1 D.1 L 2 mol·L―1 NaOH溶液中含有NaOH 2 mol 类型四、阿伏加德罗定律及其应用 例4.在两个密闭容器中,分别充有质量相等的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )。 甲的分子数比乙的分子数多 甲的物质的量比乙的物质的量少 甲的摩尔体积比乙的摩尔体积小 甲的相对分子质量比乙的相对分子质量小 [思路点拨]两容器的温度和压强均相同,且气体质量相等,而甲的密度大于乙的密度,由dfrac (1)(3)可知V2<V2。 [总结升华]在解答关于阿伏加德罗常数的问题时,应正确理解相关概念的内涵和外延,缜密细致地分析每一个问题。 举一反三: [变式1]在下列条件下,两种气体的分子数一定相等的是 A.同温度、同体积的N2和O4 B.同压强、同体积的H2和CH2 C.同质量、不同密度的N2和CO D.同体积、同密度的CO2和N4 类型五、物质的量浓度在化学实验中的应用 L水可溶解700 L氨气,所得氨水密度为0.9 g / mL,求氨水的物质的量浓度。 [思路点拨]求氨水的物质的量浓度需要知道氨气的物质的量和溶液的体积,氨气的物质的量可由标准状况下氨气的体积求得,溶液的体积可由溶液的质量和密度求得,溶液的质量为溶剂的质量和溶质的质量之和,这样来逐步分析,解析过程就变得非常明了。 [总结升华]本题考查气体溶于水后物质的量浓度的计算。首先求气体溶质的物质的量,抓住定义表达式,准确理解各物理量的含义,同时化学计算中一定要带单位运算。 L Al3(SO4)2和(NH4)2SO4的混合溶液中加入b mol aCl2,恰好使溶液中的SO-33+完全沉淀;如加入足量强碱并加热可得到c mol NH2+气体,则原溶液中的Al4浓度(mol/L)为( )。 [思路点拨]Ba+ SO= BaSO↓,NH+OH NH↑+HO,根据方程式中的数量关系,再运用电荷守恒计算。 [总结升华]本题的立足点是有关物质的量浓度的计算,要注意反应中的定量关系和电荷守恒的应用。
[典型例题]
类型一、化学实验基本方法
例1.下列实验能达到目的的是( )。
A. 在容量瓶中加一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸B. 用稀硫酸和锌粒反应制氢气
C. 用玻璃棒搅拌漏斗中的液体以加快过滤的速度
D. 加入盐酸以除去硫酸钠中的少量碳酸钠杂质
E. [思路点拨]运用化学实验的基本方法逐项分析各选项的说法是否正确,特别是要注意对实验操作的描述是否准确。
F. [总结升华] 此类题型宜采用逐项分析法。
G. 举一反三:
[变式1]下列实验操作与安全事故处理错误的是( ) A.使用温度计测量烧杯中的水浴温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶,残破的温度计插入装有硫粉的广口瓶中 B.用试管夹从试管底由下往上夹住距离管口约
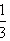 处,手持试管夹长柄末端,进行加热 C.将浓硫酸放入容量瓶中,然后加水稀释制取稀硫酸 D.把玻管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻管插入端,缓慢旋进塞孔中
处,手持试管夹长柄末端,进行加热 C.将浓硫酸放入容量瓶中,然后加水稀释制取稀硫酸 D.把玻管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻管插入端,缓慢旋进塞孔中类型二、混合物分离和提纯的常用方法
a2+、Mg2+、Fe3+、SO42―杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下:
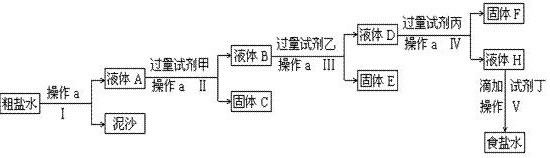
的名称是____________,所用玻璃仪器是________________________________。 (2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的沉淀,则试剂甲为________溶液。 (3)在第Ⅴ步中,加入试剂丁直到溶液无明显变化时,写出此过程的化学方程式________________。
[总结升华]看似比较大的实验题,往往问题都设在一些小的基本操作,所以做好此类题要注意两点:其一要从宏观把握整个实验方案,其二是准确规范地表述基本操作。
举一反三:
[变式1]关于粗盐提纯的下列说法正确的是( ) A.溶解粗盐时,应尽量使溶液稀些,防止食盐不完全溶解 B.滤去不溶性杂质后,将滤液移至坩埚内加热浓缩 C.当蒸发到剩有少量液体时,停止加热利用余热将液体蒸干 D.将制得的晶体转移到新制过滤器中用大量水进行洗涤 [变式2] (1)除去NaNO3固体中混有的少量KNO3,所进行的实验操作依次为________、蒸发、结晶、________。 (2)除去KCl溶液中的SO42-,依次加入的溶液为(填溶质的化学式)__________________。
类型三、物质的量——化学计算的桥梁
NA代表阿伏加德罗常数,下列叙述错误的是( )。
10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8%
在H2O2+Cl2==2HCl+O2反应中,每生成32 g氧气,则消耗NA个Cl2分子
标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
一定温度下,1 L 0.50 mol·L-1 NaCl溶液与2 L 0.25 mol·L-1 Na2CO3溶液含Na+的物质的量不同
[思路点拨]逐选项分析该选项中涉及到的物理量之间的关系,计算时要留心有关细节的说法是否正确。
[总结升华]正误判断题是化学高考命题的热点之一,常见的命题设错角度有:(1)概念的内涵、外延有漏洞;(2)问题叙述忽略特例,如有“都是”“一定”“全部”等较绝对的词;(3)在概念或物理量的“单位”上设错,如“摩尔质量”的单位设作“g”;(4)推论错误;(5)不考虑条件,如“标准状况”“常温”;(6)计算错误;(7)违背有关定律。如“质量守恒定律”、“电荷守恒”、“阿伏加德罗定律”等;(8)概念的运用错误。在分析判断时要关注以上各点。
举一反三:
[变式1]下列叙述错误的是( ) A.0.012 kg的12C所含的原子数为6.02×1023 B.1 mol H2O中含有2 mol H和1 mol O C.2 mol NaOH溶于1 L水中配成溶液的浓度为2 mol·L―1 D.1 L 2 mol·L―1 NaOH溶液中含有NaOH 2 mol 类型四、阿伏加德罗定律及其应用
例4.在两个密闭容器中,分别充有质量相等的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )。
甲的分子数比乙的分子数多
甲的物质的量比乙的物质的量少
甲的摩尔体积比乙的摩尔体积小
甲的相对分子质量比乙的相对分子质量小
[思路点拨]两容器的温度和压强均相同,且气体质量相等,而甲的密度大于乙的密度,由
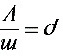 可知V2<V2。
可知V2<V2。[总结升华]在解答关于阿伏加德罗常数的问题时,应正确理解相关概念的内涵和外延,缜密细致地分析每一个问题。
举一反三:
[变式1]在下列条件下,两种气体的分子数一定相等的是 A.同温度、同体积的N2和O4 B.同压强、同体积的H2和CH2 C.同质量、不同密度的N2和CO D.同体积、同密度的CO2和N4 类型五、物质的量浓度在化学实验中的应用
L水可溶解700 L氨气,所得氨水密度为0.9 g / mL,求氨水的物质的量浓度。
[思路点拨]求氨水的物质的量浓度需要知道氨气的物质的量和溶液的体积,氨气的物质的量可由标准状况下氨气的体积求得,溶液的体积可由溶液的质量和密度求得,溶液的质量为溶剂的质量和溶质的质量之和,这样来逐步分析,解析过程就变得非常明了。
[总结升华]本题考查气体溶于水后物质的量浓度的计算。首先求气体溶质的物质的量,抓住定义表达式,准确理解各物理量的含义,同时化学计算中一定要带单位运算。
L Al3(SO4)2和(NH4)2SO4的混合溶液中加入b mol
aCl2,恰好使溶液中的SO-33+完全沉淀;如加入足量强碱并加热可得到c mol NH2+气体,则原溶液中的Al4浓度(mol/L)为( )。
[思路点拨]Ba+ SO= BaSO↓,NH+OH NH↑+HO,根据方程式中的数量关系,再运用电荷守恒计算。
[总结升华]本题的立足点是有关物质的量浓度的计算,要注意反应中的定量关系和电荷守恒的应用。
题目解答
答案
举一反三: 类型二、 混合物分离和提纯的常用方法 举一反三: 类型三、 物质的量 —— 化学计算的桥梁 举一反三: 类型四、 阿伏加德罗定律及其应用 举一反三: 类型五、 物质的量浓度在化学实验中的应用 类型六、 有关物质的量浓度的计算