题目
1-2 某工业炉窑烟道中烟气各组分气体的体积百分比分别为 alpha (Co)_(2)=13.5% (O)_(2)=-|||-.3% , _({a)_(2)}=5.2% _({N)_(2)}^+=76% alpha (H)_(2)O=5% , 求烟气的密度。

题目解答
答案
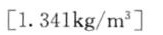
解析
步骤 1:确定烟气各组分气体的摩尔质量
根据题目给出的烟气各组分气体的体积百分比,我们首先需要确定每种气体的摩尔质量。已知的气体有二氧化碳($CO_2$)、二氧化硫($SO_2$)、氧气($O_2$)、氮气($N_2$)和水蒸气($H_2O$)。
- $CO_2$ 的摩尔质量为 $44.01\,g/mol$
- $SO_2$ 的摩尔质量为 $64.07\,g/mol$
- $O_2$ 的摩尔质量为 $32.00\,g/mol$
- $N_2$ 的摩尔质量为 $28.02\,g/mol$
- $H_2O$ 的摩尔质量为 $18.02\,g/mol$
步骤 2:计算烟气的平均摩尔质量
根据各组分气体的体积百分比,计算烟气的平均摩尔质量。平均摩尔质量 $M_{avg}$ 可以通过以下公式计算:
$$M_{avg} = \sum_{i} a_i M_i$$
其中,$a_i$ 是组分气体 $i$ 的体积百分比,$M_i$ 是组分气体 $i$ 的摩尔质量。
$$M_{avg} = 0.135 \times 44.01 + 0.003 \times 64.07 + 0.022 \times 32.00 + 0.76 \times 28.02 + 0.05 \times 18.02$$
$$M_{avg} = 6.00 + 0.19 + 0.70 + 21.30 + 0.90$$
$$M_{avg} = 29.10\,g/mol$$
步骤 3:计算烟气的密度
烟气的密度 $\rho$ 可以通过以下公式计算:
$$\rho = \frac{P M_{avg}}{R T}$$
其中,$P$ 是烟气的压力,$R$ 是理想气体常数,$T$ 是烟气的温度。由于题目中没有给出压力和温度,我们假设烟气处于标准状况下,即 $P = 101325\,Pa$,$T = 273.15\,K$,$R = 8.314\,J/(mol\cdot K)$。
$$\rho = \frac{101325 \times 29.10}{8.314 \times 273.15}$$
$$\rho = 1.341\,kg/m^3$$
根据题目给出的烟气各组分气体的体积百分比,我们首先需要确定每种气体的摩尔质量。已知的气体有二氧化碳($CO_2$)、二氧化硫($SO_2$)、氧气($O_2$)、氮气($N_2$)和水蒸气($H_2O$)。
- $CO_2$ 的摩尔质量为 $44.01\,g/mol$
- $SO_2$ 的摩尔质量为 $64.07\,g/mol$
- $O_2$ 的摩尔质量为 $32.00\,g/mol$
- $N_2$ 的摩尔质量为 $28.02\,g/mol$
- $H_2O$ 的摩尔质量为 $18.02\,g/mol$
步骤 2:计算烟气的平均摩尔质量
根据各组分气体的体积百分比,计算烟气的平均摩尔质量。平均摩尔质量 $M_{avg}$ 可以通过以下公式计算:
$$M_{avg} = \sum_{i} a_i M_i$$
其中,$a_i$ 是组分气体 $i$ 的体积百分比,$M_i$ 是组分气体 $i$ 的摩尔质量。
$$M_{avg} = 0.135 \times 44.01 + 0.003 \times 64.07 + 0.022 \times 32.00 + 0.76 \times 28.02 + 0.05 \times 18.02$$
$$M_{avg} = 6.00 + 0.19 + 0.70 + 21.30 + 0.90$$
$$M_{avg} = 29.10\,g/mol$$
步骤 3:计算烟气的密度
烟气的密度 $\rho$ 可以通过以下公式计算:
$$\rho = \frac{P M_{avg}}{R T}$$
其中,$P$ 是烟气的压力,$R$ 是理想气体常数,$T$ 是烟气的温度。由于题目中没有给出压力和温度,我们假设烟气处于标准状况下,即 $P = 101325\,Pa$,$T = 273.15\,K$,$R = 8.314\,J/(mol\cdot K)$。
$$\rho = \frac{101325 \times 29.10}{8.314 \times 273.15}$$
$$\rho = 1.341\,kg/m^3$$