题目
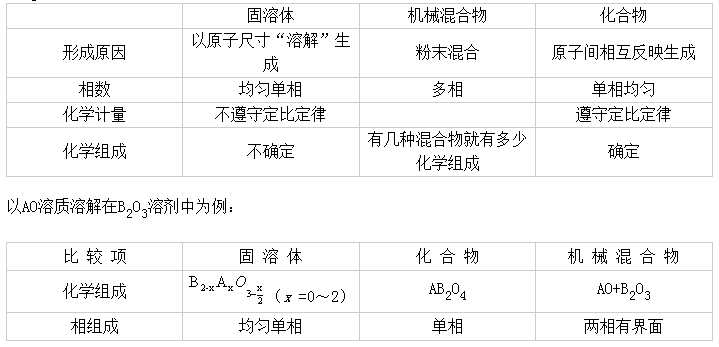
二次再结晶和晶粒生长的异同,防止二次再结晶的措施: 相同点:两者的推动力均为晶界两侧质点的吉布斯自由能之差,进行方式都是通过界面迁移。不同点:前者是个别晶粒异常长大,后者是晶粒尺寸均匀长大;前者气孔被包裹在晶粒内部,后者气孔维持在晶界交汇处。防治措施:合理选择原料的细度,提高粉料粒度的均匀性;控制温度;引入添加剂。相平衡1. 解释名词:凝聚系统:不含气相或气相可以忽略的系统。 介稳平衡:即热力学非平衡态,能量处于较高状态,经常出现于硅酸盐系统中。 低共熔点:是一种无变量点,系统冷却时几种晶相同时从熔液中析出,或加热时同时融化。 双升点:处于交叉位的单转熔点。 双降点:处于共轭位的双转熔点。 马鞍点:三元相图界线上温度最高点,同时又是二元系统温度的最低点。a)晶体与晶体常数:晶体是内部质点在三维空间成周期性重复排列的固体。或晶体是具格子构造的固体。晶体常数:晶轴轴率或轴单位,轴角。b)类质同晶:物质结晶时,其晶体结构中部分原有的离子或原子位置被性质相似的其它离子或原子所占有,共同组成均匀的、呈单一相的晶体,不引起键性和晶体结构变化的现象。 同质多晶:同一化学组成在不同热力学条件下形成结构不同的晶体的现象。c)二八面体型:在层状硅酸盐矿物中,若有三分之二的八面体空隙被阳离子所填充称为二八面体型结构。 三八面体型:在层状硅酸盐矿物中,若全部的八面体空隙被阳离子所填充称为三八面体型结构。 d)同晶取代:杂质离子取代晶体结构中某一结点上的离子而不改变晶体结构类型的现象。 阳离子交换:在粘土矿物中,当结构中的同晶取代主要发生在铝氧层时,一些电价低、半径大的阳离子(如K+、Na+等)将进入晶体结构来平衡多余的负电荷,它们与晶体的结合不很牢固,在一定条件下可以被其它阳离子交换。e)正尖晶石:在AB2.4.晶石型晶体结构中,若A2+分布在四面体空隙、而B3+分布于八面体空隙,称为正尖晶石; 反尖晶石:若A2+分布在八面体空隙、而B3+一半分布于四面体空隙另一半分布于八面体空隙,通式为B(AB)O4,称为反尖晶石。 f)晶胞:任何晶体都对应一种布拉菲格子,因此任何晶体都可划分出与此种布拉菲格子平行六面体相对应的部分,这一部分晶体就称为晶胞。晶胞是能够反映晶体结构特征的最小单位。 表示晶体结构特征的参数(a、b、c,α(b∧c)、β(a∧c)、γ(a∧b))称为晶胞常数,晶胞参数也即晶体常数。 g):配位数:晶体结构中与一个离子直接相邻的异号离子数。配位体:晶体结构中与某一个阳离子直接相邻、形成配位关系的各个阴离子中心连线所构成的多面体。多晶转变:当外界条件改变到一定程度时,各种变体之间发生结构转变,从一种变体转变成为另一种变体的现象。配位场理论:除了考虑到由配位体所引起的纯静电效应以外,还考虑了共价成键的效应的理论。⑵单键强:单键强即为各种化合物分解能与该种化合物配位数的商。⑶分化过程:架状[SiO4]断裂称为熔融石英的分化过程。缩聚过程:分化过程产生的低聚化合物相互发生作用,形成级次较高的聚合物,次过程为缩聚过程。⑷网络形成剂:正离子是网络形成离子,对应氧化物能单独形成玻璃。即凡氧化物的单键能/熔点>0.7.kJ/molk 者称为网络形成剂。网络变性剂:这类氧化物不能形成玻璃,但能改变网络结构,从而使玻璃性质改变,即单键强/熔点<0.125.J/molk者称为网络变形剂。1)当晶体热振动时,一些能量足够大的原子离开平衡位置而挤到晶格点的间隙中,形成间隙原子,而原来位置上形成空位,称为弗伦克尔缺陷。如果正常格点上原子,热起伏后获得能量离开平衡位置,跃迁到晶体的表面,在原正常格点上留下空位,称为肖特基缺陷。2)滑移方向与位错线垂直的位错称为刃型位错。位错线与滑移方向相互平行的位错称为螺型位错。3)非化学计量化合物指偏离正常化学计量的化合物。热缺陷指因热振动而引起的缺陷。 4. SiO2具有很高的熔点,硅酸盐玻璃的熔制温度也很高。现要选择一种氧化物与SiO2在800℃的低温下形成均一的二元氧化物玻璃,请问,选何种氧化物?加入量是多少? 解:根据Na2O-SiO2系统相图可知最低共熔点为799℃。故选择Na2O能与SiO2在800℃的低温下形成均一的二元氧化物玻璃。12.淬冷法的最大优点有哪些?适用的对象是什么?最大优点:准确度高。因为长时间保温较接近平衡状态,淬冷后在室温下又可对试样中平衡共存的相数、各相的组成、形态和数量直接进行测定。适用对象:适用于相变速度慢的系统,如果快则在淬冷时发生相变。14.稳定相与介稳相的区别是什么?1)每一个稳定相有一个稳定存在的温度范围,超过这个范围就变成介稳相。2)在一定温度下,稳定相具有最小蒸汽压。3)介稳相有向稳定相转变的趋势,但从动力学角度讲,转变速度很慢,能长期保持自己的状态。15.在耐火材料硅砖的生产中,为什么鳞石英含量越多越好,而方石英越少越好?石英、鳞石英和方石英三种变体的高低温型转变中,方石英∆V变化最大,石英次之,而鳞石英最小。如果制品中方石英含量大,则在冷却到低温时,由于α-方石英转变成β -方石英有较大的体积收缩而难以获得致密的硅砖制品。16.三元系统组成的表示方法?在三元系统组成中有哪些关系?表示方法:在三元系统中用等边三角形来表示组成。关系:⑴等含量规则;⑵定比例规则;⑶杠杆规则;⑷重心规则;⑸交叉位置规则;⑹共轭位置规则。 17.在三元系统中有哪几条重要规则?它们的用途和定义分别是什么?⑴连线规则:用途:用来判断界线的温度走向。定义:将界线(或延长线)与相应的连线相交,其交点是该界线上的温度最高点;温度走向是背离交点。⑵切线规则:用途:用于判断三元相图上界线的性质。定义:将界线上的某一点所作的切线与相应的组成的连线相交,如交点在连线上,则表示界线上该处具有共熔性质;如交点在连线的延长线上,则表示界线上该处具有转熔性质,远离交点的晶相被回吸。⑶重心规则:用途:用于判断无变量点的性质定义:无变量点处于其相应副三角形的重心位,则为共熔点;无变量点处于其相应副三角形的交叉位,则为单转熔点;无变量点处于其相应副三角形的共轭位,则为双转熔点。⑷三角形规则用途:确定结晶产物和结晶终点。 定义:原始熔体组成点所在三角形的三个顶点表示的物质即为其结晶产物;与这三个物质相应的初晶区所包围的三元无变量点是其结晶终点。晶体及晶体缺陷 2、在氧离子面心立方密堆积结构中,对于获得稳定结构各需何种价离子:1)填满所有的八面体空隙,2价阳离子,MgO;2)填满所有的四面体空隙,1价阳离子,Li2O;(3)填满一半的八面体空隙,4价阳离子,TiO2; (4)填满一半的四面体空隙,2价阳离子,ZnO。 10、简答题 1)试述玻璃和晶体的差别? 2)晶胞与空间格子是何种关系?1)晶体的内部质点在三维空间作有规律的重复排列,兼具短程有序和长程有序的结构。而玻璃的内部质点则呈近程有序而远程无序的无规网络结构或微晶子结构。与非晶体比较晶体具有自限性、均一性、异向性、对称性、最小内能和稳定性。2)晶胞是指能够充分反映整个晶体结构特征的最小结构单位,晶体可看成晶胞的无间隙堆垛而成。晶胞的形状大小与对应的单位平行六面体完全一致,并可用与平行六面体相同的参数来表征晶胞的几何特征。其区别是单位平行六面体是不具任何物理、化学特征的几何点(等同点)构成的。而晶胞则是实在的具体质点构成。 11 以NaCl晶胞为例,试说明面心立方紧密堆积中的八面体和四面体空隙的位置和数量。以NaCl晶胞中(001)面心的一个球(Cl离子)为例,它的正下方有1个八面体空隙(体心位置),与其对称,正上方也有1个八面体空隙;前后左右各有1个八面体空隙(棱心位置)。所以共有6个八面体空隙与其直接相邻,由于每个八面体空隙由6个球构成,所以属于这个球的八面体空隙数为6×1/6=1。 在这个晶胞中,这个球还与另外2个面心、1个顶角上的球构成4个四面体空隙(即1/8小立方体的体心位置);由于对称性,在上面的晶胞中,也有4个四面体空隙由这个参与构成。所以共有8个四面体空隙与其直接相邻,由于每个四面体空隙由4个球构成,所以属于这个球的四面体空隙数为8×1/4=2。16、试述影响置换型固溶体的固溶度的条件。 1)离子尺寸因素 从晶体稳定性考虑,相互替代的离子尺寸愈相近,则固溶体愈稳定。若(r1- r2)< 15%时,形成连续置换型固溶体。若此值在15~30%时,可以形成有限置换型固溶体。而此值>30%时,不能形成固溶体。2)晶体的结构类型 形成连续固溶体的两个组分必须具有完全相同的晶体结构。结构不同最多只能生成有限固溶体。3)离子的电价因素 只有离子价相同或复合替代离子价总和相同时,才可能形成连续置换型固溶体。(4)电负性因素 电负性相近,有利于固溶体的生成。 17、比较项固溶体 化合物 机械混合物
二次再结晶和晶粒生长的异同,防止二次再结晶的措施: 相同点:两者的推动力均为晶界两侧质点的吉布斯自由能之差,进行方式都是通过界面迁移。不同点:前者是个别晶粒异常长大,后者是晶粒尺寸均匀长大;前者气孔被包裹在晶粒内部,后者气孔维持在晶界交汇处。防治措施:合理选择原料的细度,提高粉料粒度的均匀性;控制温度;引入添加剂。相平衡
1. 解释名词:凝聚系统:不含气相或气相可以忽略的系统。 介稳平衡:即热力学非平衡态,能量处于较高状态,经常出现于硅酸盐系统中。 低共熔点:是一种无变量点,系统冷却时几种晶相同时从熔液中析出,或加热时同时融化。 双升点:处于交叉位的单转熔点。 双降点:处于共轭位的双转熔点。 马鞍点:三元相图界线上温度最高点,同时又是二元系统温度的最低点。a)晶体与晶体常数:晶体是内部质点在三维空间成周期性重复排列的固体。或晶体是具格子构造的固体。晶体常数:晶轴轴率或轴单位,轴角。b)类质同晶:物质结晶时,其晶体结构中部分原有的离子或原子位置被性质相似的其它离子或原子所占有,共同组成均匀的、呈单一相的晶体,不引起键性和晶体结构变化的现象。 同质多晶:同一化学组成在不同热力学条件下形成结构不同的晶体的现象。c)二八面体型:在层状硅酸盐矿物中,若有三分之二的八面体空隙被阳离子所填充称为二八面体型结构。 三八面体型:在层状硅酸盐矿物中,若全部的八面体空隙被阳离子所填充称为三八面体型结构。 d)同晶取代:杂质离子取代晶体结构中某一结点上的离子而不改变晶体结构类型的现象。 阳离子交换:在粘土矿物中,当结构中的同晶取代主要发生在铝氧层时,一些电价低、半径大的阳离子(如K+、Na+等)将进入晶体结构来平衡多余的负电荷,它们与晶体的结合不很牢固,在一定条件下可以被其它阳离子交换。e)正尖晶石:在AB
2.
4.晶石型晶体结构中,若A2+分布在四面体空隙、而B3+分布于八面体空隙,称为正尖晶石; 反尖晶石:若A2+分布在八面体空隙、而B3+一半分布于四面体空隙另一半分布于八面体空隙,通式为B(AB)O4,称为反尖晶石。 f)晶胞:任何晶体都对应一种布拉菲格子,因此任何晶体都可划分出与此种布拉菲格子平行六面体相对应的部分,这一部分晶体就称为晶胞。晶胞是能够反映晶体结构特征的最小单位。 表示晶体结构特征的参数(a、b、c,α(b∧c)、β(a∧c)、γ(a∧b))称为晶胞常数,晶胞参数也即晶体常数。 g):配位数:晶体结构中与一个离子直接相邻的异号离子数。配位体:晶体结构中与某一个阳离子直接相邻、形成配位关系的各个阴离子中心连线所构成的多面体。多晶转变:当外界条件改变到一定程度时,各种变体之间发生结构转变,从一种变体转变成为另一种变体的现象。配位场理论:除了考虑到由配位体所引起的纯静电效应以外,还考虑了共价成键的效应的理论。⑵单键强:单键强即为各种化合物分解能与该种化合物配位数的商。⑶分化过程:架状[SiO4]断裂称为熔融石英的分化过程。缩聚过程:分化过程产生的低聚化合物相互发生作用,形成级次较高的聚合物,次过程为缩聚过程。⑷网络形成剂:正离子是网络形成离子,对应氧化物能单独形成玻璃。即凡氧化物的单键能/熔点>
0.
7.kJ/molk 者称为网络形成剂。网络变性剂:这类氧化物不能形成玻璃,但能改变网络结构,从而使玻璃性质改变,即单键强/熔点<0.12
5.J/molk者称为网络变形剂。1)当晶体热振动时,一些能量足够大的原子离开平衡位置而挤到晶格点的间隙中,形成间隙原子,而原来位置上形成空位,称为弗伦克尔缺陷。如果正常格点上原子,热起伏后获得能量离开平衡位置,跃迁到晶体的表面,在原正常格点上留下空位,称为肖特基缺陷。2)滑移方向与位错线垂直的位错称为刃型位错。位错线与滑移方向相互平行的位错称为螺型位错。3)非化学计量化合物指偏离正常化学计量的化合物。热缺陷指因热振动而引起的缺陷。
4. SiO2具有很高的熔点,硅酸盐玻璃的熔制温度也很高。现要选择一种氧化物与SiO2在800℃的低温下形成均一的二元氧化物玻璃,请问,选何种氧化物?加入量是多少? 解:根据Na2O-SiO2系统相图可知最低共熔点为799℃。故选择Na2O能与SiO2在800℃的低温下形成均一的二元氧化物玻璃。12.淬冷法的最大优点有哪些?适用的对象是什么?最大优点:准确度高。因为长时间保温较接近平衡状态,淬冷后在室温下又可对试样中平衡共存的相数、各相的组成、形态和数量直接进行测定。适用对象:适用于相变速度慢的系统,如果快则在淬冷时发生相变。14.稳定相与介稳相的区别是什么?1)每一个稳定相有一个稳定存在的温度范围,超过这个范围就变成介稳相。2)在一定温度下,稳定相具有最小蒸汽压。3)介稳相有向稳定相转变的趋势,但从动力学角度讲,转变速度很慢,能长期保持自己的状态。15.在耐火材料硅砖的生产中,为什么鳞石英含量越多越好,而方石英越少越好?石英、鳞石英和方石英三种变体的高低温型转变中,方石英∆V变化最大,石英次之,而鳞石英最小。如果制品中方石英含量大,则在冷却到低温时,由于α-方石英转变成β -方石英有较大的体积收缩而难以获得致密的硅砖制品。1
6.三元系统组成的表示方法?在三元系统组成中有哪些关系?表示方法:在三元系统中用等边三角形来表示组成。关系:⑴等含量规则;⑵定比例规则;⑶杠杆规则;⑷重心规则;⑸交叉位置规则;⑹共轭位置规则。 17.在三元系统中有哪几条重要规则?它们的用途和定义分别是什么?⑴连线规则:用途:用来判断界线的温度走向。定义:将界线(或延长线)与相应的连线相交,其交点是该界线上的温度最高点;温度走向是背离交点。⑵切线规则:用途:用于判断三元相图上界线的性质。定义:将界线上的某一点所作的切线与相应的组成的连线相交,如交点在连线上,则表示界线上该处具有共熔性质;如交点在连线的延长线上,则表示界线上该处具有转熔性质,远离交点的晶相被回吸。⑶重心规则:用途:用于判断无变量点的性质定义:无变量点处于其相应副三角形的重心位,则为共熔点;无变量点处于其相应副三角形的交叉位,则为单转熔点;无变量点处于其相应副三角形的共轭位,则为双转熔点。⑷三角形规则用途:确定结晶产物和结晶终点。 定义:原始熔体组成点所在三角形的三个顶点表示的物质即为其结晶产物;与这三个物质相应的初晶区所包围的三元无变量点是其结晶终点。晶体及晶体缺陷 2、在氧离子面心立方密堆积结构中,对于获得稳定结构各需何种价离子:1)填满所有的八面体空隙,2价阳离子,MgO;2)填满所有的四面体空隙,1价阳离子,Li2O;(3)填满一半的八面体空隙,4价阳离子,TiO2; (4)填满一半的四面体空隙,2价阳离子,ZnO。 10、简答题 1)试述玻璃和晶体的差别? 2)晶胞与空间格子是何种关系?1)晶体的内部质点在三维空间作有规律的重复排列,兼具短程有序和长程有序的结构。而玻璃的内部质点则呈近程有序而远程无序的无规网络结构或微晶子结构。与非晶体比较晶体具有自限性、均一性、异向性、对称性、最小内能和稳定性。2)晶胞是指能够充分反映整个晶体结构特征的最小结构单位,晶体可看成晶胞的无间隙堆垛而成。晶胞的形状大小与对应的单位平行六面体完全一致,并可用与平行六面体相同的参数来表征晶胞的几何特征。其区别是单位平行六面体是不具任何物理、化学特征的几何点(等同点)构成的。而晶胞则是实在的具体质点构成。 11 以NaCl晶胞为例,试说明面心立方紧密堆积中的八面体和四面体空隙的位置和数量。以NaCl晶胞中(001)面心的一个球(Cl离子)为例,它的正下方有1个八面体空隙(体心位置),与其对称,正上方也有1个八面体空隙;前后左右各有1个八面体空隙(棱心位置)。所以共有6个八面体空隙与其直接相邻,由于每个八面体空隙由6个球构成,所以属于这个球的八面体空隙数为6×1/6=1。 在这个晶胞中,这个球还与另外2个面心、1个顶角上的球构成4个四面体空隙(即1/8小立方体的体心位置);由于对称性,在上面的晶胞中,也有4个四面体空隙由这个参与构成。所以共有8个四面体空隙与其直接相邻,由于每个四面体空隙由4个球构成,所以属于这个球的四面体空隙数为8×1/4=2。16、试述影响置换型固溶体的固溶度的条件。 1)离子尺寸因素 从晶体稳定性考虑,相互替代的离子尺寸愈相近,则固溶体愈稳定。若(r1- r2)< 15%时,形成连续置换型固溶体。若此值在15~30%时,可以形成有限置换型固溶体。而此值>30%时,不能形成固溶体。2)晶体的结构类型 形成连续固溶体的两个组分必须具有完全相同的晶体结构。结构不同最多只能生成有限固溶体。3)离子的电价因素 只有离子价相同或复合替代离子价总和相同时,才可能形成连续置换型固溶体。(4)电负性因素 电负性相近,有利于固溶体的生成。 17、比较项固溶体 化合物 机械混合物
1. 解释名词:凝聚系统:不含气相或气相可以忽略的系统。 介稳平衡:即热力学非平衡态,能量处于较高状态,经常出现于硅酸盐系统中。 低共熔点:是一种无变量点,系统冷却时几种晶相同时从熔液中析出,或加热时同时融化。 双升点:处于交叉位的单转熔点。 双降点:处于共轭位的双转熔点。 马鞍点:三元相图界线上温度最高点,同时又是二元系统温度的最低点。a)晶体与晶体常数:晶体是内部质点在三维空间成周期性重复排列的固体。或晶体是具格子构造的固体。晶体常数:晶轴轴率或轴单位,轴角。b)类质同晶:物质结晶时,其晶体结构中部分原有的离子或原子位置被性质相似的其它离子或原子所占有,共同组成均匀的、呈单一相的晶体,不引起键性和晶体结构变化的现象。 同质多晶:同一化学组成在不同热力学条件下形成结构不同的晶体的现象。c)二八面体型:在层状硅酸盐矿物中,若有三分之二的八面体空隙被阳离子所填充称为二八面体型结构。 三八面体型:在层状硅酸盐矿物中,若全部的八面体空隙被阳离子所填充称为三八面体型结构。 d)同晶取代:杂质离子取代晶体结构中某一结点上的离子而不改变晶体结构类型的现象。 阳离子交换:在粘土矿物中,当结构中的同晶取代主要发生在铝氧层时,一些电价低、半径大的阳离子(如K+、Na+等)将进入晶体结构来平衡多余的负电荷,它们与晶体的结合不很牢固,在一定条件下可以被其它阳离子交换。e)正尖晶石:在AB
2.
4.晶石型晶体结构中,若A2+分布在四面体空隙、而B3+分布于八面体空隙,称为正尖晶石; 反尖晶石:若A2+分布在八面体空隙、而B3+一半分布于四面体空隙另一半分布于八面体空隙,通式为B(AB)O4,称为反尖晶石。 f)晶胞:任何晶体都对应一种布拉菲格子,因此任何晶体都可划分出与此种布拉菲格子平行六面体相对应的部分,这一部分晶体就称为晶胞。晶胞是能够反映晶体结构特征的最小单位。 表示晶体结构特征的参数(a、b、c,α(b∧c)、β(a∧c)、γ(a∧b))称为晶胞常数,晶胞参数也即晶体常数。 g):配位数:晶体结构中与一个离子直接相邻的异号离子数。配位体:晶体结构中与某一个阳离子直接相邻、形成配位关系的各个阴离子中心连线所构成的多面体。多晶转变:当外界条件改变到一定程度时,各种变体之间发生结构转变,从一种变体转变成为另一种变体的现象。配位场理论:除了考虑到由配位体所引起的纯静电效应以外,还考虑了共价成键的效应的理论。⑵单键强:单键强即为各种化合物分解能与该种化合物配位数的商。⑶分化过程:架状[SiO4]断裂称为熔融石英的分化过程。缩聚过程:分化过程产生的低聚化合物相互发生作用,形成级次较高的聚合物,次过程为缩聚过程。⑷网络形成剂:正离子是网络形成离子,对应氧化物能单独形成玻璃。即凡氧化物的单键能/熔点>
0.
7.kJ/molk 者称为网络形成剂。网络变性剂:这类氧化物不能形成玻璃,但能改变网络结构,从而使玻璃性质改变,即单键强/熔点<0.12
5.J/molk者称为网络变形剂。1)当晶体热振动时,一些能量足够大的原子离开平衡位置而挤到晶格点的间隙中,形成间隙原子,而原来位置上形成空位,称为弗伦克尔缺陷。如果正常格点上原子,热起伏后获得能量离开平衡位置,跃迁到晶体的表面,在原正常格点上留下空位,称为肖特基缺陷。2)滑移方向与位错线垂直的位错称为刃型位错。位错线与滑移方向相互平行的位错称为螺型位错。3)非化学计量化合物指偏离正常化学计量的化合物。热缺陷指因热振动而引起的缺陷。
4. SiO2具有很高的熔点,硅酸盐玻璃的熔制温度也很高。现要选择一种氧化物与SiO2在800℃的低温下形成均一的二元氧化物玻璃,请问,选何种氧化物?加入量是多少? 解:根据Na2O-SiO2系统相图可知最低共熔点为799℃。故选择Na2O能与SiO2在800℃的低温下形成均一的二元氧化物玻璃。12.淬冷法的最大优点有哪些?适用的对象是什么?最大优点:准确度高。因为长时间保温较接近平衡状态,淬冷后在室温下又可对试样中平衡共存的相数、各相的组成、形态和数量直接进行测定。适用对象:适用于相变速度慢的系统,如果快则在淬冷时发生相变。14.稳定相与介稳相的区别是什么?1)每一个稳定相有一个稳定存在的温度范围,超过这个范围就变成介稳相。2)在一定温度下,稳定相具有最小蒸汽压。3)介稳相有向稳定相转变的趋势,但从动力学角度讲,转变速度很慢,能长期保持自己的状态。15.在耐火材料硅砖的生产中,为什么鳞石英含量越多越好,而方石英越少越好?石英、鳞石英和方石英三种变体的高低温型转变中,方石英∆V变化最大,石英次之,而鳞石英最小。如果制品中方石英含量大,则在冷却到低温时,由于α-方石英转变成β -方石英有较大的体积收缩而难以获得致密的硅砖制品。1
6.三元系统组成的表示方法?在三元系统组成中有哪些关系?表示方法:在三元系统中用等边三角形来表示组成。关系:⑴等含量规则;⑵定比例规则;⑶杠杆规则;⑷重心规则;⑸交叉位置规则;⑹共轭位置规则。 17.在三元系统中有哪几条重要规则?它们的用途和定义分别是什么?⑴连线规则:用途:用来判断界线的温度走向。定义:将界线(或延长线)与相应的连线相交,其交点是该界线上的温度最高点;温度走向是背离交点。⑵切线规则:用途:用于判断三元相图上界线的性质。定义:将界线上的某一点所作的切线与相应的组成的连线相交,如交点在连线上,则表示界线上该处具有共熔性质;如交点在连线的延长线上,则表示界线上该处具有转熔性质,远离交点的晶相被回吸。⑶重心规则:用途:用于判断无变量点的性质定义:无变量点处于其相应副三角形的重心位,则为共熔点;无变量点处于其相应副三角形的交叉位,则为单转熔点;无变量点处于其相应副三角形的共轭位,则为双转熔点。⑷三角形规则用途:确定结晶产物和结晶终点。 定义:原始熔体组成点所在三角形的三个顶点表示的物质即为其结晶产物;与这三个物质相应的初晶区所包围的三元无变量点是其结晶终点。晶体及晶体缺陷 2、在氧离子面心立方密堆积结构中,对于获得稳定结构各需何种价离子:1)填满所有的八面体空隙,2价阳离子,MgO;2)填满所有的四面体空隙,1价阳离子,Li2O;(3)填满一半的八面体空隙,4价阳离子,TiO2; (4)填满一半的四面体空隙,2价阳离子,ZnO。 10、简答题 1)试述玻璃和晶体的差别? 2)晶胞与空间格子是何种关系?1)晶体的内部质点在三维空间作有规律的重复排列,兼具短程有序和长程有序的结构。而玻璃的内部质点则呈近程有序而远程无序的无规网络结构或微晶子结构。与非晶体比较晶体具有自限性、均一性、异向性、对称性、最小内能和稳定性。2)晶胞是指能够充分反映整个晶体结构特征的最小结构单位,晶体可看成晶胞的无间隙堆垛而成。晶胞的形状大小与对应的单位平行六面体完全一致,并可用与平行六面体相同的参数来表征晶胞的几何特征。其区别是单位平行六面体是不具任何物理、化学特征的几何点(等同点)构成的。而晶胞则是实在的具体质点构成。 11 以NaCl晶胞为例,试说明面心立方紧密堆积中的八面体和四面体空隙的位置和数量。以NaCl晶胞中(001)面心的一个球(Cl离子)为例,它的正下方有1个八面体空隙(体心位置),与其对称,正上方也有1个八面体空隙;前后左右各有1个八面体空隙(棱心位置)。所以共有6个八面体空隙与其直接相邻,由于每个八面体空隙由6个球构成,所以属于这个球的八面体空隙数为6×1/6=1。 在这个晶胞中,这个球还与另外2个面心、1个顶角上的球构成4个四面体空隙(即1/8小立方体的体心位置);由于对称性,在上面的晶胞中,也有4个四面体空隙由这个参与构成。所以共有8个四面体空隙与其直接相邻,由于每个四面体空隙由4个球构成,所以属于这个球的四面体空隙数为8×1/4=2。16、试述影响置换型固溶体的固溶度的条件。 1)离子尺寸因素 从晶体稳定性考虑,相互替代的离子尺寸愈相近,则固溶体愈稳定。若(r1- r2)< 15%时,形成连续置换型固溶体。若此值在15~30%时,可以形成有限置换型固溶体。而此值>30%时,不能形成固溶体。2)晶体的结构类型 形成连续固溶体的两个组分必须具有完全相同的晶体结构。结构不同最多只能生成有限固溶体。3)离子的电价因素 只有离子价相同或复合替代离子价总和相同时,才可能形成连续置换型固溶体。(4)电负性因素 电负性相近,有利于固溶体的生成。 17、比较项固溶体 化合物 机械混合物
题目解答
答案
二次再结晶和晶粒生长的异同,防止二次再结晶的措施: 相同点:两者的推动力均为晶界两侧质点的吉布斯自由能之差,进行方式都是通过界面迁移。不同点:前者是个别晶粒异常长大,后者是晶粒尺寸均匀长大;前者气孔被包裹在晶粒内部,后者气孔维持在晶界交汇处。防治措施:合理选择原料的细度,提高粉料粒度的均匀性;控制温度;引入添加剂。