题目
电镀污泥[主要含Cr( III)、Fe(III)、Cu( II)、Ni(II )等]中铬资源再利用生产红矾钠,该工业流程如图:NH3、NH4HCO3 盐酸 H2O2-|||-污泥 ①烘干研磨 ②氨浸 氨浸渣 ③酸浸 酸浸液 ④氧化-|||-NaOH 净-|||-Na2Cr2O7·2H2O ⑦酸化、结晶 ⑥ 萃取液 ⑤萃取-|||-下-|||-NaOH HCl、 TBP- 煤油已知:(1)相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算) 金属离子 开始沉淀的pH 沉淀完全的pH Fe3+ 1.1 3.2 Ni2+ 6.7 9.5 Cr3+ 4.0 6.8 Cu2+ 6 9 (2)Cr( VI)在酸性和碱性环境下的存在形式分别为Cr2O72-、CrO42-。(1)将污泥烘干、研磨的目的是 ____ 。(2)温度对氨浸浸出率的影响如图所示,氨浸的适宜温度为 ____ 左右,80℃以上铜镍浸出率下降的原因为 ____ 。NH3、NH4HCO3 盐酸 H2O2-|||-污泥 ①烘干研磨 ②氨浸 氨浸渣 ③酸浸 酸浸液 ④氧化-|||-NaOH 净-|||-Na2Cr2O7·2H2O ⑦酸化、结晶 ⑥ 萃取液 ⑤萃取-|||-下-|||-NaOH HCl、 TBP- 煤油(3)氧化步骤中pH应控制的范围为 ____ ,H2O2 发生反应的离子方程式为 ____ 。(4)步骤⑥中加入NaOH的工艺名称为 ____ ,可 循环利用的物质有 ____ (填选项)。A.萃取余液B.盐酸C.NaOHD.结晶后母液(5)若实验取干污泥250g,其中含Cr11.2%,实验所得晶体为59.6g,则Cr回收率为 ____ 。(6)通过电解法也可以将Cr(III)转化为Cr(VI)回收,装置如图,中间为 ____ (填“阳离子”、“阴离子”、“质子”)交换膜,阳极的反应式为 ____ 。NH3、NH4HCO3 盐酸 H2O2-|||-污泥 ①烘干研磨 ②氨浸 氨浸渣 ③酸浸 酸浸液 ④氧化-|||-NaOH 净-|||-Na2Cr2O7·2H2O ⑦酸化、结晶 ⑥ 萃取液 ⑤萃取-|||-下-|||-NaOH HCl、 TBP- 煤油
电镀污泥[主要含Cr( III)、Fe(III)、Cu( II)、Ni(II )等]中铬资源再利用生产红矾钠,该工业流程如图:
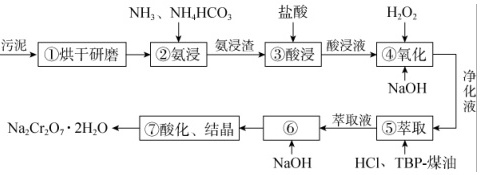
已知:(1)相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算)
(2)Cr( VI)在酸性和碱性环境下的存在形式分别为Cr2O72-、CrO42-。
(1)将污泥烘干、研磨的目的是 ____ 。
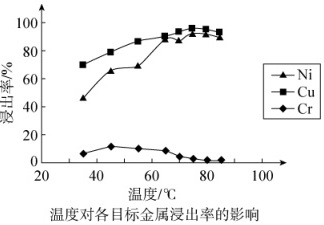
(2)温度对氨浸浸出率的影响如图所示,氨浸的适宜温度为 ____ 左右,80℃以上铜镍浸出率下降的原因为 ____ 。
(3)氧化步骤中pH应控制的范围为 ____ ,H2O2 发生反应的离子方程式为 ____ 。
(4)步骤⑥中加入NaOH的工艺名称为 ____ ,可 循环利用的物质有 ____ (填选项)。
A.萃取余液
B.盐酸
C.NaOH
D.结晶后母液
(5)若实验取干污泥250g,其中含Cr11.2%,实验所得晶体为59.6g,则Cr回收率为 ____ 。
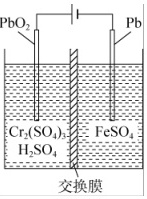
(6)通过电解法也可以将Cr(III)转化为Cr(VI)回收,装置如图,中间为 ____ (填“阳离子”、“阴离子”、“质子”)交换膜,阳极的反应式为 ____ 。

已知:(1)相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算)
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Ni2+ | 6.7 | 9.5 |
| Cr3+ | 4.0 | 6.8 |
| Cu2+ | 6 | 9 |
(1)将污泥烘干、研磨的目的是 ____ 。
(2)温度对氨浸浸出率的影响如图所示,氨浸的适宜温度为 ____ 左右,80℃以上铜镍浸出率下降的原因为 ____ 。

(3)氧化步骤中pH应控制的范围为 ____ ,H2O2 发生反应的离子方程式为 ____ 。
(4)步骤⑥中加入NaOH的工艺名称为 ____ ,可 循环利用的物质有 ____ (填选项)。
A.萃取余液
B.盐酸
C.NaOH
D.结晶后母液
(5)若实验取干污泥250g,其中含Cr11.2%,实验所得晶体为59.6g,则Cr回收率为 ____ 。
(6)通过电解法也可以将Cr(III)转化为Cr(VI)回收,装置如图,中间为 ____ (填“阳离子”、“阴离子”、“质子”)交换膜,阳极的反应式为 ____ 。

题目解答
答案
解:(1)湿污泥中含水多,体积大,有效成分浓度小,工业不易操作,生产成本高。经风干或烘干后,可以减小体积;研磨可以增大与氨浸液的接触面积,提高浸取率,所以将污泥烘干、研磨的目的是富集增大接触面积、提高浸出率,
故答案为:富集增大接触面积、提高浸出率;
(2)根据图像可知,在75°C条件下,Cu(II)、Ni(II)浸出率最高,80°C上铜镍浸出率下降,是由于温度升高,氨气挥发,影响了浸取液成分比例,使效率下降,
故答案为:75℃;温度升高,氨气挥发;
(3)由于酸浸液中还含有Fe(III)、Cu(II)、Ni(II)等杂质,在④除杂步骤中,需都除去,pH应控制为≥9.5;而在pH应控制为≥9.5时Cr(III)也会沉淀,所以H2O2将Cr3+氧化,同时加入NaOH使其转化为CrO42-,离子方程式为2Cr3++3H2O2+10OH-=2CrO42-+8H2O,
故答案为:pH≥9.5;2Cr3++3H2O2+10OH-=2CrO42-+8H2O;
(4)步骤⑤为萃取,提取出CrO42-在有机相中,步骤⑦酸化应在水相进行,所以⑥中加入NaOH的目的是反萃取;流程中由于盐酸和NaOH都在后续步骤中被消耗,能够循环利用的物质有萃取余液、结晶后母液,可以提高原料利用率,AD符合题意,
故答案为:反萃取;AD;
(5)污泥中含Cr为250g×11.2%≈28.0g,实验得晶体为Na2Cr2O7•2H2O质量为59.6g,其中Cr的质量为:$\frac{59.6g}{298g/mol}$×2×52g/mol=20.8g;Cr的回收率为:$\frac{20.8g}{28.0g}$×100%=74.3%,
故答案为:74.3%;
(6)由电解装置图可知,PbO2电极与电源正极相连,为电解池的阳极,Pb电极与电源负极相连,为电解池的阴极,阳极电解液呈酸性,反应式为2Cr3+-6e-+7H2O=Cr2O72-+14H+,为防止Cr3+进入阴极室,应为阴离子膜,
故答案为:阴离子;2Cr3+-6e-+7H2O=Cr2O72-+14H+。
故答案为:富集增大接触面积、提高浸出率;
(2)根据图像可知,在75°C条件下,Cu(II)、Ni(II)浸出率最高,80°C上铜镍浸出率下降,是由于温度升高,氨气挥发,影响了浸取液成分比例,使效率下降,
故答案为:75℃;温度升高,氨气挥发;
(3)由于酸浸液中还含有Fe(III)、Cu(II)、Ni(II)等杂质,在④除杂步骤中,需都除去,pH应控制为≥9.5;而在pH应控制为≥9.5时Cr(III)也会沉淀,所以H2O2将Cr3+氧化,同时加入NaOH使其转化为CrO42-,离子方程式为2Cr3++3H2O2+10OH-=2CrO42-+8H2O,
故答案为:pH≥9.5;2Cr3++3H2O2+10OH-=2CrO42-+8H2O;
(4)步骤⑤为萃取,提取出CrO42-在有机相中,步骤⑦酸化应在水相进行,所以⑥中加入NaOH的目的是反萃取;流程中由于盐酸和NaOH都在后续步骤中被消耗,能够循环利用的物质有萃取余液、结晶后母液,可以提高原料利用率,AD符合题意,
故答案为:反萃取;AD;
(5)污泥中含Cr为250g×11.2%≈28.0g,实验得晶体为Na2Cr2O7•2H2O质量为59.6g,其中Cr的质量为:$\frac{59.6g}{298g/mol}$×2×52g/mol=20.8g;Cr的回收率为:$\frac{20.8g}{28.0g}$×100%=74.3%,
故答案为:74.3%;
(6)由电解装置图可知,PbO2电极与电源正极相连,为电解池的阳极,Pb电极与电源负极相连,为电解池的阴极,阳极电解液呈酸性,反应式为2Cr3+-6e-+7H2O=Cr2O72-+14H+,为防止Cr3+进入阴极室,应为阴离子膜,
故答案为:阴离子;2Cr3+-6e-+7H2O=Cr2O72-+14H+。