题目
在总压为100kPa、温度为30℃时,用清水吸收混合气体中的氨,气相传质系数kg=3.84×10-6 kmol/(m2·s·kPa),液相传质系数kg=1.83×10-4 m/s,假设此操作条件下的平衡关系服从亨利定律,测得液相溶质摩尔分率为0.05,其气相平衡分压为6.7kPa。求当塔内某截面上气、液组成分别为y=0.05,x=0.01时(1)以(kg)、(kg)表示的传质总推动力及相应的传质速率、总传质系数;(2)分析该过程的控制因素。
在总压为100kPa、温度为30℃时,用清水吸收混合气体中的氨,气相传质系数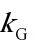 =3.84×10-6 kmol/(m2·s·kPa),液相传质系数
=3.84×10-6 kmol/(m2·s·kPa),液相传质系数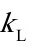 =1.83×10-4 m/s,假设此操作条件下的平衡关系服从亨利定律,测得液相溶质摩尔分率为0.05,其气相平衡分压为6.7kPa。求当塔内某截面上气、液组成分别为y=0.05,x=0.01时
=1.83×10-4 m/s,假设此操作条件下的平衡关系服从亨利定律,测得液相溶质摩尔分率为0.05,其气相平衡分压为6.7kPa。求当塔内某截面上气、液组成分别为y=0.05,x=0.01时
(1)以(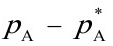 )、(
)、(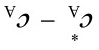 )表示的传质总推动力及相应的传质速率、总传质系数;
)表示的传质总推动力及相应的传质速率、总传质系数;
(2)分析该过程的控制因素。
题目解答
答案
解:(1)根据亨利定律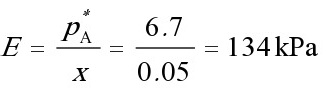
相平衡常数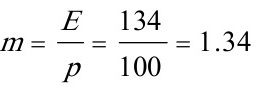
溶解度常数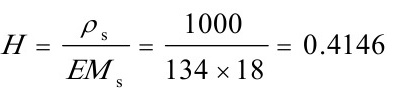
以气相分压差(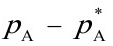 )表示总推动力时:
)表示总推动力时:
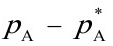 =100×0.05-134×0.01=3.66kPa
=100×0.05-134×0.01=3.66kPa
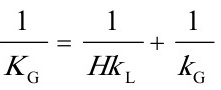 =
=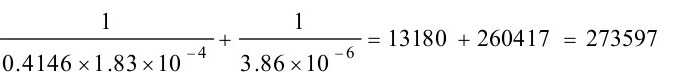
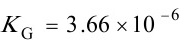 kmol/(m2·s·kPa)
kmol/(m2·s·kPa)
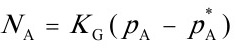 =3.66×10-6×3.66=1.34×10-5 kmol/(m2·s)
=3.66×10-6×3.66=1.34×10-5 kmol/(m2·s)
以(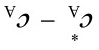 )表示的传质总推动力时:
)表示的传质总推动力时:
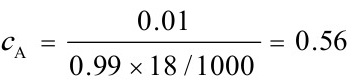 kmol/m3
kmol/m3
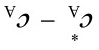 =0.4146×100×0.05-0.56=1.513 kmol/m3
=0.4146×100×0.05-0.56=1.513 kmol/m3
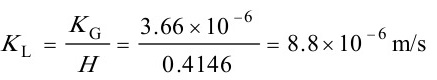
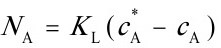 =8.8×10-6×1.513=1.3314×10-5 kmol/(m2·s)
=8.8×10-6×1.513=1.3314×10-5 kmol/(m2·s)
(2)与(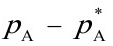 )表示的传质总推动力相应的传质阻力为273597(m2·s·kPa)/ kmol;
)表示的传质总推动力相应的传质阻力为273597(m2·s·kPa)/ kmol;
其中气相阻力为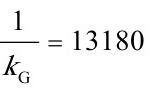 m2·s·kPa/ kmol;
m2·s·kPa/ kmol;
液相阻力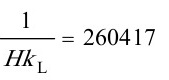 m2·s·kPa/ kmol;
m2·s·kPa/ kmol;
气相阻力占总阻力的百分数为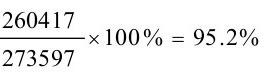 。
。
故该传质过程为气膜控制过程。
解析
步骤 1:计算亨利定律常数E
根据亨利定律,$E=\dfrac{{P}_{A}}{x}=\dfrac{6.7}{0.05}=134kPa$。
步骤 2:计算相平衡常数m
相平衡常数$m=\dfrac{E}{p}=\dfrac{134}{100}=1.34$。
步骤 3:计算溶解度常数H
溶解度常数$H=\dfrac{{P}_{S}}{E{M}_{s}}=\dfrac{1000}{134\times 18}=0.4146$。
步骤 4:以气相分压差(${P}_{A}-{P}_{A}$)表示总推动力
${P}_{A}-{P}_{A}$=100×0.05-134×0.01=3.66kPa。
步骤 5:计算总传质系数${K}_{0}$
$\dfrac{1}{{K}_{0}}=\dfrac{1}{H{K}_{1}}+\dfrac{1}{{K}_{6}}$=$\dfrac{1}{0.4146\times 1.83\times {10}^{-4}}+\dfrac{1}{3.86\times {10}^{-6}}=131800+2614017=2723597$。
步骤 6:计算传质速率${N}_{A}$
${N}_{A}={K}_{G}({P}_{A}-{P}_{A})$=3.66×10-6×3.66=1.34×10-5 kmol/(m2·s)。
步骤 7:以(${C}_{A}-{C}_{A}$)表示的传质总推动力
${c}_{A}=\dfrac{0.01}{0.99\times 18/1000}=0.56$ kmol/m3
${C}_{A}-{C}_{A}$=0.4146×100×0.05-0.56=1.513 kmol/m3。
步骤 8:计算液相传质系数${K}_{L}$
${K}_{L}=\dfrac{{K}_{G}}{H}=\dfrac{3.66\times {10}^{-6}}{0.4146}=8.8\times {10}^{-6}m/s$。
步骤 9:计算传质速率${N}_{A}$
${N}_{A}={K}_{L}({C}_{A}-{c}_{A})$=8.8×10-6×1.513=1.3314×10-5 kmol/(m2·s)。
步骤 10:分析传质过程的控制因素
与(${P}_{A}-{P}_{A}$)表示的传质总推动力相应的传质阻力为273597(m2·s·kPa)/ kmol;
其中气相阻力为$\dfrac{1}{{k}_{0}}=13180$m2·s·kPa/ kmol;
液相阻力$\dfrac{1}{H{K}_{1}}=260417$m2·s·kPa/ kmol;
气相阻力占总阻力的百分数为$\dfrac{260417}{273597}\times 100\% =95.2\% $。
故该传质过程为气膜控制过程。
根据亨利定律,$E=\dfrac{{P}_{A}}{x}=\dfrac{6.7}{0.05}=134kPa$。
步骤 2:计算相平衡常数m
相平衡常数$m=\dfrac{E}{p}=\dfrac{134}{100}=1.34$。
步骤 3:计算溶解度常数H
溶解度常数$H=\dfrac{{P}_{S}}{E{M}_{s}}=\dfrac{1000}{134\times 18}=0.4146$。
步骤 4:以气相分压差(${P}_{A}-{P}_{A}$)表示总推动力
${P}_{A}-{P}_{A}$=100×0.05-134×0.01=3.66kPa。
步骤 5:计算总传质系数${K}_{0}$
$\dfrac{1}{{K}_{0}}=\dfrac{1}{H{K}_{1}}+\dfrac{1}{{K}_{6}}$=$\dfrac{1}{0.4146\times 1.83\times {10}^{-4}}+\dfrac{1}{3.86\times {10}^{-6}}=131800+2614017=2723597$。
步骤 6:计算传质速率${N}_{A}$
${N}_{A}={K}_{G}({P}_{A}-{P}_{A})$=3.66×10-6×3.66=1.34×10-5 kmol/(m2·s)。
步骤 7:以(${C}_{A}-{C}_{A}$)表示的传质总推动力
${c}_{A}=\dfrac{0.01}{0.99\times 18/1000}=0.56$ kmol/m3
${C}_{A}-{C}_{A}$=0.4146×100×0.05-0.56=1.513 kmol/m3。
步骤 8:计算液相传质系数${K}_{L}$
${K}_{L}=\dfrac{{K}_{G}}{H}=\dfrac{3.66\times {10}^{-6}}{0.4146}=8.8\times {10}^{-6}m/s$。
步骤 9:计算传质速率${N}_{A}$
${N}_{A}={K}_{L}({C}_{A}-{c}_{A})$=8.8×10-6×1.513=1.3314×10-5 kmol/(m2·s)。
步骤 10:分析传质过程的控制因素
与(${P}_{A}-{P}_{A}$)表示的传质总推动力相应的传质阻力为273597(m2·s·kPa)/ kmol;
其中气相阻力为$\dfrac{1}{{k}_{0}}=13180$m2·s·kPa/ kmol;
液相阻力$\dfrac{1}{H{K}_{1}}=260417$m2·s·kPa/ kmol;
气相阻力占总阻力的百分数为$\dfrac{260417}{273597}\times 100\% =95.2\% $。
故该传质过程为气膜控制过程。