题目
同学们在学习《燃料及其利用》内容时,进行了以下三个主题的研究。通入气体 a b 接吸收装置-|||-→= 一 数学-|||-红磷-|||-→-|||-图1 图2-|||-精炼煤 +(H)_(2)O ,高温 水煤气 催化剂 甲醇(CH3OH,-|||-粗煤 洗选加工 ② CO和H2) ③ 常温下液态)-|||-①-|||-含硫化合物的洗液,-|||-用作化工原料-|||-图3-|||-一定条件-|||-∞O-|||-∞-|||-图4主题一:燃烧条件及燃料选择(1)探究燃烧条件步骤一 通入N2,点燃酒精灯。步骤二 冷却至室温。步骤三 通入O2,点燃酒精灯。该实验中能说明可燃物燃烧需要O2的现象是 ____ 。从燃烧条件分析,用水灭火主要利用的原理是 ____ 。(2)选择最佳燃料煤、氢气、石油、天然气等物质都可以用做燃料。同学们一致认为氢气是最优质的燃料,原因是 ____ (答出一条原因即可)。主题二:调查家用燃料的变迁(3)20世纪60年代以前,我国城市家庭以“煤球”为燃料,在冬天时有煤气中毒事件发生,其原因是 ____ 。(4)20世纪70年代,“蜂窝煤”取代了“煤球”。 同时,为了减少煤燃烧时对环境的污染,煤气厂将水蒸气通过炽热的煤层制得较洁净的水煤气(主要成分是CO和H2),常常在家用煤气中加入少量有难闻气味的气体,目的是 ____ 。(5)到了80年代,液化石油气和管道气又取代了“蜂窝煤”。煤气中主要成分CO燃烧的化学方程式是 ____ 。(6)21世纪,我国的“西气东输工程”使天然气(主要成分是CH4)成为家庭主要燃料,天然气中主要成分燃烧的化学方程式为 ____ 。主题三:使用燃料与保护环境(7)将煤进行汽化、液化变成清洁能源对环境保护起重要作用。煤气化、液化示意图如图3。Ⅰ.沉淀、过滤和吸附是工业中常用的方法。图中第①步采用的分离方法是 ____ 。Ⅱ.第②步是在高温条件下,将煤与水反应生成CO和H2混合气体,这种气体又称为合成气,该反应的化学方程式为 ____ 。Ⅲ.第③步是将合成气在一定条件下反应,生成甲醇,其反应的微观过程如图4所示。第③步发生的反应属于 ____ (填基本反应类型)。该步骤反应的微观过程示意图中,反应物CO和H2的质量比为 ____ 。同学们在学习《燃料及其利用》内容时,进行了以下三个主题的研究。通入气体 a b 接吸收装置-|||-→= 一 数学-|||-红磷-|||-→-|||-图1 图2-|||-精炼煤 +(H)_(2)O ,高温 水煤气 催化剂 甲醇(CH3OH,-|||-粗煤 洗选加工 ② CO和H2) ③ 常温下液态)-|||-①-|||-含硫化合物的洗液,-|||-用作化工原料-|||-图3-|||-一定条件-|||-∞O-|||-∞-|||-图4主题一:燃烧条件及燃料选择(1)探究燃烧条件步骤一 通入N2,点燃酒精灯。步骤二 冷却至室温。步骤三 通入O2,点燃酒精灯。该实验中能说明可燃物燃烧需要O2的现象是 ____ 。从燃烧条件分析,用水灭火主要利用的原理是 ____ 。(2)选择最佳燃料煤、氢气、石油、天然气等物质都可以用做燃料。同学们一致认为氢气是最优质的燃料,原因是 ____ (答出一条原因即可)。主题二:调查家用燃料的变迁(3)20世纪60年代以前,我国城市家庭以“煤球”为燃料,在冬天时有煤气中毒事件发生,其原因是 ____ 。(4)20世纪70年代,“蜂窝煤”取代了“煤球”。 同时,为了减少煤燃烧时对环境的污染,煤气厂将水蒸气通过炽热的煤层制得较洁净的水煤气(主要成分是CO和H2),常常在家用煤气中加入少量有难闻气味的气体,目的是 ____ 。(5)到了80年代,液化石油气和管道气又取代了“蜂窝煤”。煤气中主要成分CO燃烧的化学方程式是 ____ 。(6)21世纪,我国的“西气东输工程”使天然气(主要成分是CH4)成为家庭主要燃料,天然气中主要成分燃烧的化学方程式为 ____ 。主题三:使用燃料与保护环境(7)将煤进行汽化、液化变成清洁能源对环境保护起重要作用。煤气化、液化示意图如图3。Ⅰ.沉淀、过滤和吸附是工业中常用的方法。图中第①步采用的分离方法是 ____ 。Ⅱ.第②步是在高温条件下,将煤与水反应生成CO和H2混合气体,这种气体又称为合成气,该反应的化学方程式为 ____ 。Ⅲ.第③步是将合成气在一定条件下反应,生成甲醇,其反应的微观过程如图4所示。第③步发生的反应属于 ____ (填基本反应类型)。该步骤反应的微观过程示意图中,反应物CO和H2的质量比为 ____ 。
同学们在学习《燃料及其利用》内容时,进行了以下三个主题的研究。
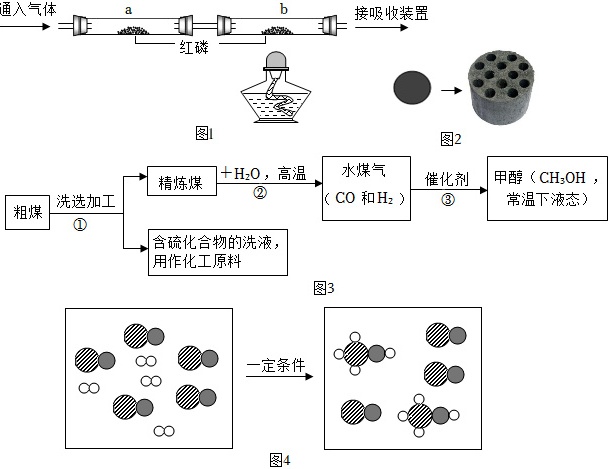
主题一:燃烧条件及燃料选择
(1)探究燃烧条件
步骤一 通入N2,点燃酒精灯。
步骤二 冷却至室温。
步骤三 通入O2,点燃酒精灯。
该实验中能说明可燃物燃烧需要O2的现象是 ____ 。从燃烧条件分析,用水灭火主要利用的原理是 ____ 。
(2)选择最佳燃料
煤、氢气、石油、天然气等物质都可以用做燃料。同学们一致认为氢气是最优质的燃料,原因是 ____ (答出一条原因即可)。
主题二:调查家用燃料的变迁
(3)20世纪60年代以前,我国城市家庭以“煤球”为燃料,在冬天时有煤气中毒事件发生,其原因是 ____ 。
(4)20世纪70年代,“蜂窝煤”取代了“煤球”。
同时,为了减少煤燃烧时对环境的污染,煤气厂将水蒸气通过炽热的煤层制得较洁净的水煤气(主要成分是CO和H2),常常在家用煤气中加入少量有难闻气味的气体,目的是 ____ 。
(5)到了80年代,液化石油气和管道气又取代了“蜂窝煤”。煤气中主要成分CO燃烧的化学方程式是 ____ 。
(6)21世纪,我国的“西气东输工程”使天然气(主要成分是CH4)成为家庭主要燃料,天然气中主要成分燃烧的化学方程式为 ____ 。
主题三:使用燃料与保护环境
(7)将煤进行汽化、液化变成清洁能源对环境保护起重要作用。煤气化、液化示意图如图3。
Ⅰ.沉淀、过滤和吸附是工业中常用的方法。图中第①步采用的分离方法是 ____ 。
Ⅱ.第②步是在高温条件下,将煤与水反应生成CO和H2混合气体,这种气体又称为合成气,该反应的化学方程式为 ____ 。
Ⅲ.第③步是将合成气在一定条件下反应,生成甲醇,其反应的微观过程如图4所示。
第③步发生的反应属于 ____ (填基本反应类型)。该步骤反应的微观过程示意图中,反应物CO和H2的质量比为 ____ 。
同学们在学习《燃料及其利用》内容时,进行了以下三个主题的研究。

主题一:燃烧条件及燃料选择
(1)探究燃烧条件
步骤一 通入N2,点燃酒精灯。
步骤二 冷却至室温。
步骤三 通入O2,点燃酒精灯。
该实验中能说明可燃物燃烧需要O2的现象是 ____ 。从燃烧条件分析,用水灭火主要利用的原理是 ____ 。
(2)选择最佳燃料
煤、氢气、石油、天然气等物质都可以用做燃料。同学们一致认为氢气是最优质的燃料,原因是 ____ (答出一条原因即可)。
主题二:调查家用燃料的变迁
(3)20世纪60年代以前,我国城市家庭以“煤球”为燃料,在冬天时有煤气中毒事件发生,其原因是 ____ 。
(4)20世纪70年代,“蜂窝煤”取代了“煤球”。
同时,为了减少煤燃烧时对环境的污染,煤气厂将水蒸气通过炽热的煤层制得较洁净的水煤气(主要成分是CO和H2),常常在家用煤气中加入少量有难闻气味的气体,目的是 ____ 。
(5)到了80年代,液化石油气和管道气又取代了“蜂窝煤”。煤气中主要成分CO燃烧的化学方程式是 ____ 。
(6)21世纪,我国的“西气东输工程”使天然气(主要成分是CH4)成为家庭主要燃料,天然气中主要成分燃烧的化学方程式为 ____ 。
主题三:使用燃料与保护环境
(7)将煤进行汽化、液化变成清洁能源对环境保护起重要作用。煤气化、液化示意图如图3。
Ⅰ.沉淀、过滤和吸附是工业中常用的方法。图中第①步采用的分离方法是 ____ 。
Ⅱ.第②步是在高温条件下,将煤与水反应生成CO和H2混合气体,这种气体又称为合成气,该反应的化学方程式为 ____ 。
Ⅲ.第③步是将合成气在一定条件下反应,生成甲醇,其反应的微观过程如图4所示。
第③步发生的反应属于 ____ (填基本反应类型)。该步骤反应的微观过程示意图中,反应物CO和H2的质量比为 ____ 。

主题一:燃烧条件及燃料选择
(1)探究燃烧条件
步骤一 通入N2,点燃酒精灯。
步骤二 冷却至室温。
步骤三 通入O2,点燃酒精灯。
该实验中能说明可燃物燃烧需要O2的现象是 ____ 。从燃烧条件分析,用水灭火主要利用的原理是 ____ 。
(2)选择最佳燃料
煤、氢气、石油、天然气等物质都可以用做燃料。同学们一致认为氢气是最优质的燃料,原因是 ____ (答出一条原因即可)。
主题二:调查家用燃料的变迁
(3)20世纪60年代以前,我国城市家庭以“煤球”为燃料,在冬天时有煤气中毒事件发生,其原因是 ____ 。
(4)20世纪70年代,“蜂窝煤”取代了“煤球”。
同时,为了减少煤燃烧时对环境的污染,煤气厂将水蒸气通过炽热的煤层制得较洁净的水煤气(主要成分是CO和H2),常常在家用煤气中加入少量有难闻气味的气体,目的是 ____ 。
(5)到了80年代,液化石油气和管道气又取代了“蜂窝煤”。煤气中主要成分CO燃烧的化学方程式是 ____ 。
(6)21世纪,我国的“西气东输工程”使天然气(主要成分是CH4)成为家庭主要燃料,天然气中主要成分燃烧的化学方程式为 ____ 。
主题三:使用燃料与保护环境
(7)将煤进行汽化、液化变成清洁能源对环境保护起重要作用。煤气化、液化示意图如图3。
Ⅰ.沉淀、过滤和吸附是工业中常用的方法。图中第①步采用的分离方法是 ____ 。
Ⅱ.第②步是在高温条件下,将煤与水反应生成CO和H2混合气体,这种气体又称为合成气,该反应的化学方程式为 ____ 。
Ⅲ.第③步是将合成气在一定条件下反应,生成甲醇,其反应的微观过程如图4所示。
第③步发生的反应属于 ____ (填基本反应类型)。该步骤反应的微观过程示意图中,反应物CO和H2的质量比为 ____ 。
同学们在学习《燃料及其利用》内容时,进行了以下三个主题的研究。

主题一:燃烧条件及燃料选择
(1)探究燃烧条件
步骤一 通入N2,点燃酒精灯。
步骤二 冷却至室温。
步骤三 通入O2,点燃酒精灯。
该实验中能说明可燃物燃烧需要O2的现象是 ____ 。从燃烧条件分析,用水灭火主要利用的原理是 ____ 。
(2)选择最佳燃料
煤、氢气、石油、天然气等物质都可以用做燃料。同学们一致认为氢气是最优质的燃料,原因是 ____ (答出一条原因即可)。
主题二:调查家用燃料的变迁
(3)20世纪60年代以前,我国城市家庭以“煤球”为燃料,在冬天时有煤气中毒事件发生,其原因是 ____ 。
(4)20世纪70年代,“蜂窝煤”取代了“煤球”。
同时,为了减少煤燃烧时对环境的污染,煤气厂将水蒸气通过炽热的煤层制得较洁净的水煤气(主要成分是CO和H2),常常在家用煤气中加入少量有难闻气味的气体,目的是 ____ 。
(5)到了80年代,液化石油气和管道气又取代了“蜂窝煤”。煤气中主要成分CO燃烧的化学方程式是 ____ 。
(6)21世纪,我国的“西气东输工程”使天然气(主要成分是CH4)成为家庭主要燃料,天然气中主要成分燃烧的化学方程式为 ____ 。
主题三:使用燃料与保护环境
(7)将煤进行汽化、液化变成清洁能源对环境保护起重要作用。煤气化、液化示意图如图3。
Ⅰ.沉淀、过滤和吸附是工业中常用的方法。图中第①步采用的分离方法是 ____ 。
Ⅱ.第②步是在高温条件下,将煤与水反应生成CO和H2混合气体,这种气体又称为合成气,该反应的化学方程式为 ____ 。
Ⅲ.第③步是将合成气在一定条件下反应,生成甲醇,其反应的微观过程如图4所示。
第③步发生的反应属于 ____ (填基本反应类型)。该步骤反应的微观过程示意图中,反应物CO和H2的质量比为 ____ 。
题目解答
答案
解:(1)步骤一中,通入N2,N2不支持燃烧,点燃酒精灯,b中加热时红磷不燃烧;步骤三中,通入O2,点燃酒精灯,b中加热时红磷燃烧,说明可燃物燃烧需要氧气;灭火原理:①清除或隔离可燃物,②隔绝氧气或空气,③使温度降到可燃物的着火点以下;由此可知,用水灭火主要利用的原理为利用水汽化吸热的方式使可燃物温度降到可燃物的着火点以下。
(2)煤、氢气、石油、天然气等物质都可以用做燃料。同学们一致认为氢气是最优质的燃料,原因是燃烧放出热量多,生成的水对环境没有污染;
(3)煤的主要成分为碳,碳在氧气中不完全燃烧产生一氧化碳,一氧化碳有毒,因此在冬天时有煤气中毒事件发生;
(4)煤气的主要成分一氧化碳是无色、无味的气体,一旦泄漏,人很难觉察,极易引起中毒事故,煤气厂常在家用水煤气中特意掺入少量有难闻气味的气体,便于人们及时发现煤气泄漏,避免煤气中毒的发生;
(5)煤气中主要成分CO燃烧的化学方程式是 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(6)天然气中主要成分为甲烷,甲烷燃烧的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(7)Ⅰ.把不溶于液体的固体与液体分开的操作为过滤,根据图示信息,图中第①步采用的分离方法是过滤;
Ⅱ.第②步是在高温条件下,将煤与水反应生成CO和H2混合气体,这种气体又称为合成气,该反应的化学方程式为C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2。
Ⅲ.第③步是将合成气在一定条件下反应,生成甲醇,方程式为CO+2H2$\frac{\underline{\;一定条件\;}}{}$CH3OH;该反应符合“多变一”反应特点,为化合反应;根据方程式可知,反应物CO和H2的质量比为28:4=7:1。
故答案为:
(1)步骤一中,b中红磷不燃烧,步骤三中,b中红磷燃烧;降低温度至可燃物的着火点以下;
(2)生成的水对环境没有污染(合理即可);
(3)碳在氧气中不完全燃烧产生一氧化碳,一氧化碳有毒;
(4)便于人们及时发现煤气泄漏,避免煤气中毒的发生;
(5)2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(6)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(7过滤;
Ⅱ.C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2;
Ⅲ.化合反应;7:1。
解:(1)步骤一中,通入N2,N2不支持燃烧,点燃酒精灯,b中加热时红磷不燃烧;步骤三中,通入O2,点燃酒精灯,b中加热时红磷燃烧,说明可燃物燃烧需要氧气;灭火原理:①清除或隔离可燃物,②隔绝氧气或空气,③使温度降到可燃物的着火点以下;由此可知,用水灭火主要利用的原理为利用水汽化吸热的方式使可燃物温度降到可燃物的着火点以下。
(2)煤、氢气、石油、天然气等物质都可以用做燃料。同学们一致认为氢气是最优质的燃料,原因是燃烧放出热量多,生成的水对环境没有污染;
(3)煤的主要成分为碳,碳在氧气中不完全燃烧产生一氧化碳,一氧化碳有毒,因此在冬天时有煤气中毒事件发生;
(4)煤气的主要成分一氧化碳是无色、无味的气体,一旦泄漏,人很难觉察,极易引起中毒事故,煤气厂常在家用水煤气中特意掺入少量有难闻气味的气体,便于人们及时发现煤气泄漏,避免煤气中毒的发生;
(5)煤气中主要成分CO燃烧的化学方程式是 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(6)天然气中主要成分为甲烷,甲烷燃烧的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(7)Ⅰ.把不溶于液体的固体与液体分开的操作为过滤,根据图示信息,图中第①步采用的分离方法是过滤;
Ⅱ.第②步是在高温条件下,将煤与水反应生成CO和H2混合气体,这种气体又称为合成气,该反应的化学方程式为C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2。
Ⅲ.第③步是将合成气在一定条件下反应,生成甲醇,方程式为CO+2H2$\frac{\underline{\;一定条件\;}}{}$CH3OH;该反应符合“多变一”反应特点,为化合反应;根据方程式可知,反应物CO和H2的质量比为28:4=7:1。
故答案为:
(1)步骤一中,b中红磷不燃烧,步骤三中,b中红磷燃烧;降低温度至可燃物的着火点以下;
(2)生成的水对环境没有污染(合理即可);
(3)碳在氧气中不完全燃烧产生一氧化碳,一氧化碳有毒;
(4)便于人们及时发现煤气泄漏,避免煤气中毒的发生;
(5)2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(6)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(7过滤;
Ⅱ.C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2;
Ⅲ.化合反应;7:1。
(2)煤、氢气、石油、天然气等物质都可以用做燃料。同学们一致认为氢气是最优质的燃料,原因是燃烧放出热量多,生成的水对环境没有污染;
(3)煤的主要成分为碳,碳在氧气中不完全燃烧产生一氧化碳,一氧化碳有毒,因此在冬天时有煤气中毒事件发生;
(4)煤气的主要成分一氧化碳是无色、无味的气体,一旦泄漏,人很难觉察,极易引起中毒事故,煤气厂常在家用水煤气中特意掺入少量有难闻气味的气体,便于人们及时发现煤气泄漏,避免煤气中毒的发生;
(5)煤气中主要成分CO燃烧的化学方程式是 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(6)天然气中主要成分为甲烷,甲烷燃烧的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(7)Ⅰ.把不溶于液体的固体与液体分开的操作为过滤,根据图示信息,图中第①步采用的分离方法是过滤;
Ⅱ.第②步是在高温条件下,将煤与水反应生成CO和H2混合气体,这种气体又称为合成气,该反应的化学方程式为C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2。
Ⅲ.第③步是将合成气在一定条件下反应,生成甲醇,方程式为CO+2H2$\frac{\underline{\;一定条件\;}}{}$CH3OH;该反应符合“多变一”反应特点,为化合反应;根据方程式可知,反应物CO和H2的质量比为28:4=7:1。
故答案为:
(1)步骤一中,b中红磷不燃烧,步骤三中,b中红磷燃烧;降低温度至可燃物的着火点以下;
(2)生成的水对环境没有污染(合理即可);
(3)碳在氧气中不完全燃烧产生一氧化碳,一氧化碳有毒;
(4)便于人们及时发现煤气泄漏,避免煤气中毒的发生;
(5)2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(6)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(7过滤;
Ⅱ.C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2;
Ⅲ.化合反应;7:1。
解:(1)步骤一中,通入N2,N2不支持燃烧,点燃酒精灯,b中加热时红磷不燃烧;步骤三中,通入O2,点燃酒精灯,b中加热时红磷燃烧,说明可燃物燃烧需要氧气;灭火原理:①清除或隔离可燃物,②隔绝氧气或空气,③使温度降到可燃物的着火点以下;由此可知,用水灭火主要利用的原理为利用水汽化吸热的方式使可燃物温度降到可燃物的着火点以下。
(2)煤、氢气、石油、天然气等物质都可以用做燃料。同学们一致认为氢气是最优质的燃料,原因是燃烧放出热量多,生成的水对环境没有污染;
(3)煤的主要成分为碳,碳在氧气中不完全燃烧产生一氧化碳,一氧化碳有毒,因此在冬天时有煤气中毒事件发生;
(4)煤气的主要成分一氧化碳是无色、无味的气体,一旦泄漏,人很难觉察,极易引起中毒事故,煤气厂常在家用水煤气中特意掺入少量有难闻气味的气体,便于人们及时发现煤气泄漏,避免煤气中毒的发生;
(5)煤气中主要成分CO燃烧的化学方程式是 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(6)天然气中主要成分为甲烷,甲烷燃烧的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(7)Ⅰ.把不溶于液体的固体与液体分开的操作为过滤,根据图示信息,图中第①步采用的分离方法是过滤;
Ⅱ.第②步是在高温条件下,将煤与水反应生成CO和H2混合气体,这种气体又称为合成气,该反应的化学方程式为C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2。
Ⅲ.第③步是将合成气在一定条件下反应,生成甲醇,方程式为CO+2H2$\frac{\underline{\;一定条件\;}}{}$CH3OH;该反应符合“多变一”反应特点,为化合反应;根据方程式可知,反应物CO和H2的质量比为28:4=7:1。
故答案为:
(1)步骤一中,b中红磷不燃烧,步骤三中,b中红磷燃烧;降低温度至可燃物的着火点以下;
(2)生成的水对环境没有污染(合理即可);
(3)碳在氧气中不完全燃烧产生一氧化碳,一氧化碳有毒;
(4)便于人们及时发现煤气泄漏,避免煤气中毒的发生;
(5)2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(6)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(7过滤;
Ⅱ.C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2;
Ⅲ.化合反应;7:1。