题目
在100 kPa压力下将组成为0.55(易挥发组分的摩尔分数)的两组分理想溶液进行平衡蒸馏和简单蒸馏。原料液处理量为100 kmol,汽化率为0.44。操作范围内的平衡关系可表示为。试求两种情况下易挥发组分的回收率和残液的组成。
在100 kPa压力下将组成为0.55(易挥发组分的摩尔分数)的两组分理想溶液进行平衡蒸馏和简单蒸馏。原料液处理量为100 kmol,汽化率为0.44。操作范围内的平衡关系可表示为。试求两种情况下易挥发组分的回收率和残液的组成。
题目解答
答案
解:(1)平衡蒸馏(闪蒸)
依题给条件 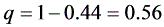
则 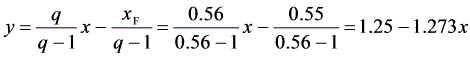
由平衡方程 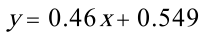
联立两方程,得y = 0.735, x = 0.4045
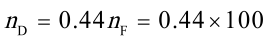 kmol = 44kmol
kmol = 44kmol
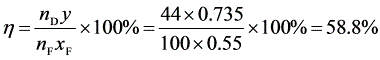
(2)简单蒸馏
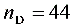 kmol
kmol 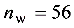 kmol
kmol
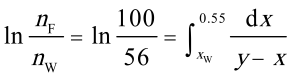
即 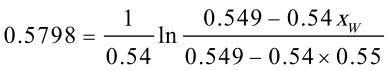
解得 xW = 0.3785
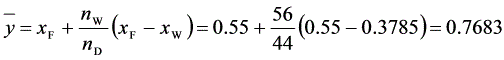
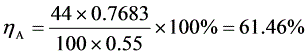
简单蒸馏收率高(61.46%),釜残液组成低(0.3785)
解析
本题主要考查两组分理想溶液的平衡蒸馏(闪蒸)和简单蒸馏的相关计算,解题关键在于利用物料衡算、相平衡关系以及相应的积分公式来求解易挥发组分的回收率和残液组成。
(1)平衡蒸馏(闪蒸)
- 计算进料热状态参数 $q$:
已知汽化率为 $0.44$,根据进料热状态参数 $q$ 的定义 $q = 1 - \frac{V}{F}$(其中 $V$ 为汽化量,$F$ 为进料量),可得 $q = 1 - 0.44 = 0.56$。 - 推导操作线方程:
对于平衡蒸馏,操作线方程为 $y=\frac{q}{q - 1}x-\frac{x_F}{q - 1}$,将 $q = 0.56$,$x_F = 0.55$ 代入可得:
$y=\frac{0.56}{0.56 - 1}x-\frac{0.55}{0.56 - 1}=1.25 - 1.273x$ - 联立方程求解气液组成:
已知平衡方程 $y = 0.46x + 0.549$,联立操作线方程和平衡方程:
$\begin{cases}y = 1.25 - 1.273x\\y = 0.46x + 0.549\end{cases}$
将两式联立可得:
$1.25 - 1.273x = 0.46x + 0.549$
移项可得:
$1.273x + 0.46x = 1.25 - 0.549$
$1.733x = 0.701$
解得 $x = 0.4045$,将 $x = 0.4045$ 代入平衡方程 $y = 0.46x + 0.549$ 可得 $y = 0.46\times0.4045 + 0.549 = 0.735$。 - 计算汽化量 $n_D$:
已知原料液处理量 $n_F = 100$ kmol,汽化率为 $0.44$,则汽化量 $n_D = 0.44n_F = 0.44\times100 = 44$ kmol。 - 计算易挥发组分的回收率 $\eta$:
回收率 $\eta=\frac{n_Dy}{n_Fx_F}\times100\%$,将 $n_D = 44$ kmol,$y = 0.735$,$n_F = 100$ kmol,$x_F = 0.55$ 代入可得:
$\eta=\frac{44\times0.735}{100\times0.55}\times100\% = 58.8\%$
(2)简单蒸馏
- 计算汽化量 $n_D$ 和残液量 $n_W$:
已知原料液处理量 $n_F = 100$ kmol,汽化率为 $0.44$,则汽化量 $n_D = 0.44n_F = 0.44\times100 = 44$ kmol,残液量 $n_W = n_F - n_D = 100 - 44 = 56$ kmol。 - 利用积分公式求解残液组成 $x_W$:
简单蒸馏的积分公式为 $\ln\frac{n_F}{n_W}=\int_{x_W}^{x_F}\frac{dx}{y - x}$,已知平衡方程 $y = 0.46x + 0.549$,则 $y - x = 0.549 - 0.54x$,代入积分公式可得:
$\ln\frac{100}{56}=\int_{x_W}^{0.55}\frac{dx}{0.549 - 0.54x}$
令 $u = 0.549 - 0.54x$,则 $du = -0.54dx$,当 $x = x_W$ 时,$u = 0.549 - 0.54x_W$;当 $x = 0.55$ 时,$u = 0.549 - 0.54\times0.55$。
则积分变为:
$\ln\frac{100}{56}=-\frac{1}{0.54}\int_{0.549 - 0.54x_W}^{0.549 - 0.54\times0.55}\frac{du}{u}$
$\ln\frac{100}{56}=\frac{1}{0.54}\ln\frac{0.549 - 0.54x_W}{0.549 - 0.54\times0.55}$
已知 $\ln\frac{100}{56}=0.5798$,则:
$0.5798=\frac{1}{0.54}\ln\frac{0.549 - 0.54x_W}{0.549 - 0.54\times0.55}$
$\ln\frac{0.549 - 0.54x_W}{0.549 - 0.54\times0.55}=0.5798\times0.54 = 0.3131$
$\frac{0.549 - 0.54x_W}{0.549 - 0.54\times0.55}=e^{0.3131}=1.367$
$0.549 - 0.54x_W = 1.367\times(0.549 - 0.54\times0.55)$
$0.549 - 0.54x_W = 1.367\times0.2515$
$0.549 - 0.54x_W = 0.3438$
$0.54x_W = 0.549 - 0.3438 = 0.2052$
解得 $x_W = 0.3785$。 - 计算平均气相组成 $\overline{y}$:
根据公式 $\overline{y}=x_F+\frac{n_W}{n_D}(x_F - x_W)$,将 $x_F = 0.55$,$n_W = 56$ kmol,$n_D = 44$ kmol,$x_W = 0.3785$ 代入可得:
$\overline{y}=0.55+\frac{56}{44}(0.55 - 0.3785)=0.7683$ - 计算易挥发组分的回收率 $\eta$:
回收率 $\eta=\frac{n_D\overline{y}}{n_Fx_F}\times100\%$,将 $n_D = 44$ kmol,$\overline{y} = 0.7683$,$n_F = 100$ kmol,$x_F = 0.55$ 代入可得:
$\eta=\frac{44\times0.7683}{100\times0.55}\times100\% = 61.46\%$