题目
生产半水煤气时,煤气发生炉在吹风阶段的某种情况下,76%(摩尔分数)的碳生成二氧化碳,其余的生成一氧化碳。试计算: (1)含碳量为81.38%的100kg的焦炭能生成1.1013MPa、303K的吹风气若干立方米? (2)所得吹风气的组成和各气体分压。
生产半水煤气时,煤气发生炉在吹风阶段的某种情况下,76%(摩尔分数)的碳生成二氧化碳,其余的生成一氧化碳。试计算: (1)含碳量为81.38%的100kg的焦炭能生成1.1013MPa、303K的吹风气若干立方米? (2)所得吹风气的组成和各气体分压。
题目解答
答案



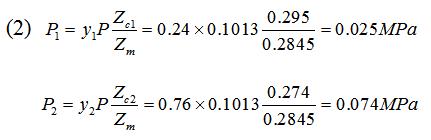
解析
步骤 1:计算焦炭中碳的摩尔数
含碳量为81.38%的100kg焦炭中碳的质量为:$100kg \times 81.38\% = 81.38kg$。碳的摩尔质量为12g/mol,因此焦炭中碳的摩尔数为:$81.38kg \times 1000g/kg \div 12g/mol = 6781.67mol$。
步骤 2:计算生成的气体摩尔数
根据题目,76%的碳生成二氧化碳,24%的碳生成一氧化碳。因此,生成的二氧化碳的摩尔数为:$6781.67mol \times 76\% = 5158.27mol$,生成的一氧化碳的摩尔数为:$6781.67mol \times 24\% = 1623.40mol$。
步骤 3:计算吹风气的体积
根据理想气体状态方程$PV=nRT$,其中$P=1.1013MPa=1.1013\times10^6Pa$,$T=303K$,$R=8.314J/(mol\cdot K)$,$n=5158.27mol+1623.40mol=6781.67mol$。代入公式计算得到吹风气的体积$V$。
步骤 4:计算吹风气的组成和各气体分压
吹风气的组成即为一氧化碳和二氧化碳的摩尔分数,一氧化碳的摩尔分数为$1623.40mol \div 6781.67mol$,二氧化碳的摩尔分数为$5158.27mol \div 6781.67mol$。各气体分压根据分压定律计算,即$P_{CO}=P_{总} \times y_{CO}$,$P_{CO_2}=P_{总} \times y_{CO_2}$。
含碳量为81.38%的100kg焦炭中碳的质量为:$100kg \times 81.38\% = 81.38kg$。碳的摩尔质量为12g/mol,因此焦炭中碳的摩尔数为:$81.38kg \times 1000g/kg \div 12g/mol = 6781.67mol$。
步骤 2:计算生成的气体摩尔数
根据题目,76%的碳生成二氧化碳,24%的碳生成一氧化碳。因此,生成的二氧化碳的摩尔数为:$6781.67mol \times 76\% = 5158.27mol$,生成的一氧化碳的摩尔数为:$6781.67mol \times 24\% = 1623.40mol$。
步骤 3:计算吹风气的体积
根据理想气体状态方程$PV=nRT$,其中$P=1.1013MPa=1.1013\times10^6Pa$,$T=303K$,$R=8.314J/(mol\cdot K)$,$n=5158.27mol+1623.40mol=6781.67mol$。代入公式计算得到吹风气的体积$V$。
步骤 4:计算吹风气的组成和各气体分压
吹风气的组成即为一氧化碳和二氧化碳的摩尔分数,一氧化碳的摩尔分数为$1623.40mol \div 6781.67mol$,二氧化碳的摩尔分数为$5158.27mol \div 6781.67mol$。各气体分压根据分压定律计算,即$P_{CO}=P_{总} \times y_{CO}$,$P_{CO_2}=P_{总} \times y_{CO_2}$。