题目
80 (0,1,80)-|||-60 (pi )_(1)-|||-40 T2-|||-20-|||-1% 0.1 0.2 0.3 0.4 0.50.6 P/MPa异丁烯(C4H8)是一种重要的化工原料,可由异丁烷(C4H10)直接催化脱氢制备:(1)已知:C4H10(g)+(1)/(2)O2(g)═C4H8(g)+H2O(g)△H1=-119kJ•mol-1H2(g)+(1)/(2)O2(g)═H2O(g)△H2=-242kJ•mol-1写出由异丁烷(C4H10)催化脱氢制备异丁烯(C4H8)的热化学方程式。 ____ 。(2)一定条件下,以异丁烷为原料催化脱氢生产异丁烯。温度、压强的改变对异丁烷平衡转化率的影响如图所示。①判断T1、T2的大小关系:T1 ____ T2(填“>”或“<”);能使单位时间内异丁烯的产量提高,又能使异丁烷平衡产率提高,应采取的措施是 ____ (填标号)。a.升高温度 b.降低温度 c.增大压强 d.降低压强 e.使用催化剂②平衡常数的表达式中的平衡浓度可以用平衡时各气体的分压代替(气体a的分压=气体a的物质的量分数×总压强,即p(a)=x(a)×p(总)。求图中的A点状态下的异丁烷脱氢反应的平衡常数Kp= ____ (保留两位有效数字)。(3)温度对催化剂的活性和目标产物的选择性都有一定的影响。表是以V2O5/γ-Al2O3为催化剂,在反应时间相同时,测得的不同温度下的数据。 温度/℃ 550 570 590 610 630 异丁烷转化率/% 13.8 24.5 25.6 30.0 33.3 异丁烯选择性/% 93.9 88.3 95.0 80.4 71.2 异丁烯的产率/% 12.9 21.6 w 24.1 23.7 已知:①选择性=((生成目标产物所消耗的反应物的量))/((参与反应的反应物的量))×100%;②异丁烷高温下裂解生成短碳链烃类化合物。①590℃时异丁烯的产率w= ____ ×100%。②在590℃之前异丁烯的产率随温度升高而增大的原因可能是 ____ 、 ____ 。③590℃之后,异丁烯产率降低的主要原因可能是 ____ 。
 异丁烯(C4H8)是一种重要的化工原料,可由异丁烷(C4H10)直接催化脱氢制备:
异丁烯(C4H8)是一种重要的化工原料,可由异丁烷(C4H10)直接催化脱氢制备:(1)已知:
C4H10(g)+$\frac{1}{2}$O2(g)═C4H8(g)+H2O(g)△H1=-119kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H2=-242kJ•mol-1
写出由异丁烷(C4H10)催化脱氢制备异丁烯(C4H8)的热化学方程式。 ____ 。
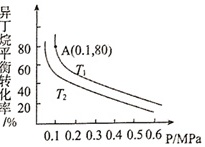
(2)一定条件下,以异丁烷为原料催化脱氢生产异丁烯。温度、压强的改变对异丁烷平衡转化率的影响如图所示。
①判断T1、T2的大小关系:T1 ____ T2(填“>”或“<”);能使单位时间内异丁烯的产量提高,又能使异丁烷平衡产率提高,应采取的措施是 ____ (填标号)。
a.升高温度 b.降低温度 c.增大压强 d.降低压强 e.使用催化剂
②平衡常数的表达式中的平衡浓度可以用平衡时各气体的分压代替(气体a的分压=气体a的物质的量分数×总压强,即p(a)=x(a)×p(总)。求图中的A点状态下的异丁烷脱氢反应的平衡常数Kp= ____ (保留两位有效数字)。
(3)温度对催化剂的活性和目标产物的选择性都有一定的影响。表是以V2O5/γ-Al2O3为催化剂,在反应时间相同时,测得的不同温度下的数据。
| 温度/℃ | 550 | 570 | 590 | 610 | 630 |
| 异丁烷转化率/% | 13.8 | 24.5 | 25.6 | 30.0 | 33.3 |
| 异丁烯选择性/% | 93.9 | 88.3 | 95.0 | 80.4 | 71.2 |
| 异丁烯的产率/% | 12.9 | 21.6 | w | 24.1 | 23.7 |
①590℃时异丁烯的产率w= ____ ×100%。
②在590℃之前异丁烯的产率随温度升高而增大的原因可能是 ____ 、 ____ 。
③590℃之后,异丁烯产率降低的主要原因可能是 ____ 。
题目解答
答案
解:(1)由①C4H10(g)+$\frac{1}{2}$O2(g)=C4H8(g)+H2O(g)△H1=-119kJ/mol,
②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H2=-242kJ/mol,根据盖斯定律可知,①-②得到C4H10(g)=C4H8(g)+H2(g),则△H=(-119kJ/mol)-(-242kJ/mol)=+123kJ/mol,
故答案为:C4H10(g)=C4H8(g)+H2(g)△H=+123kJ/mol;
(2)①由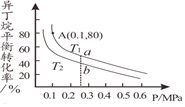 图可知,横坐标是压强,纵坐标是异丁烷的平衡转化率,取相同的压强条件下,作一虚线交T1曲线于a点,交T2曲线于b点,则a点对应的异丁烷的平衡转化率>b点对应的异丁烷的平衡转化率,
图可知,横坐标是压强,纵坐标是异丁烷的平衡转化率,取相同的压强条件下,作一虚线交T1曲线于a点,交T2曲线于b点,则a点对应的异丁烷的平衡转化率>b点对应的异丁烷的平衡转化率,
根据C4H10(g)=C4H8(g)+H2(g)+123△H=+123kJ/mol,△H>0,反应是吸热的,升高温度,平衡向正反应方向移动,异丁烷的平衡转化率才增大,所以温度T1>T2,能使单位时间内异丁烯的产量提高,又能使异丁烷平衡产率提高,由于该反应是一个吸热反应,且是一个气体体积增大的反应,所以应采取的措施为:
a.升高温度,既能增大反应速率,又能使平衡正向移动,故a符合要求;
b.降低温度,反应速率减小,平衡逆向移动,故b不符合要求;
c.增大压强,反应速率增大,平衡逆向移动,故c不符合要求;
d.降低压强,反应速率减小,平衡正向移动,能提高产率,但反应速率减小,单位时间内异丁烯的产量不一定提高,故d不符合要求,
e.使用催化剂,对平衡移动无影响,不会提高异丁烷的平衡转化率,故e不符合要求,
故答案为:>,a。
②平衡常数的表达式中的平衡浓度可以用平衡时各气体的分压代替(气体a的分压=气体a的物质的量分数×总压强,即p(a)=x(a)×p(总)。图中的A点状态下,总压强p=0.1MPa,异丁烷的平衡转化率为80%,设起始状态C4H10物质的量为1mol,根据变化的量=起始的量×转化率可知,达平衡时n(C4H10)=1-1×80%=0.2mol,n(C4H8)=0.8mol,n(H2)=0.8mol,则各分压为p(C4H10)=$\frac{{0.2mol}}{{0.2mol+0.8mol+0.8mol}}$×0.1MPa=$\frac{{0.1}}{9}$MPa,p(C4H8)=$\frac{{0.8mol}}{{0.2mol+0.8mol+0.8mol}}$×0.1MPa=$\frac{{0.4}}{9}$MPa,同理,p(H2)=$\frac{{0.4}}{9}$MPa,平衡常数Kp=$\frac{{p({C_4}{H_8})×p({H_2})}}{{p({C_4}{H_{10}})}}$=$\frac{{\frac{{0.4}}{9}×\frac{{0.4}}{9}}}{{\frac{{0.1}}{9}}}$=0.18,
故答案为:0.18;
(3)①根据异丁烷的转化率=$\frac{{变化的物质的量}}{{起始的物质的量}}$×100%和异丁烯的选择性=$\frac{{生成目标产物所消耗的反应物的量}}{{参与反应的反应物的量}}×100%$,由C4H10(g)=C4H8(g)+H2(g)+123△H=+123kJ/mol方程式可知,消耗异丁烷的物质的量与生成异丁烯的物质的量相等的,所以,根据异丁烷的起始量求出异丁烯的理论产量,根据生成目标产物所消耗的反应物的量可求出异丁烯的实际产量,由异丁烯的产率=$\frac{{实际产量}}{{理论产量}}$×100%,可知在590℃时,异丁烷的转化率为25.6%,异丁烯的选择性为95%,则异丁烯的产率=25.6%×95%=0.243,
故答案为:0.243;
②该反应是吸热反应,升高温度,反应速率加快,平衡正向移动,
故答案为:升高温度,平衡正向移动;升高温度,反应速率加快;
③高于590℃后,异丁烷高温下裂解生成短碳链烃类化合物,有副产物生成,导致异丁烯产率降低,
故答案为:异丁烷高温下裂解生成短碳链烃类化合物,有副产物生成,异丁烯产率降低。
②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H2=-242kJ/mol,根据盖斯定律可知,①-②得到C4H10(g)=C4H8(g)+H2(g),则△H=(-119kJ/mol)-(-242kJ/mol)=+123kJ/mol,
故答案为:C4H10(g)=C4H8(g)+H2(g)△H=+123kJ/mol;
(2)①由
 图可知,横坐标是压强,纵坐标是异丁烷的平衡转化率,取相同的压强条件下,作一虚线交T1曲线于a点,交T2曲线于b点,则a点对应的异丁烷的平衡转化率>b点对应的异丁烷的平衡转化率,
图可知,横坐标是压强,纵坐标是异丁烷的平衡转化率,取相同的压强条件下,作一虚线交T1曲线于a点,交T2曲线于b点,则a点对应的异丁烷的平衡转化率>b点对应的异丁烷的平衡转化率,根据C4H10(g)=C4H8(g)+H2(g)+123△H=+123kJ/mol,△H>0,反应是吸热的,升高温度,平衡向正反应方向移动,异丁烷的平衡转化率才增大,所以温度T1>T2,能使单位时间内异丁烯的产量提高,又能使异丁烷平衡产率提高,由于该反应是一个吸热反应,且是一个气体体积增大的反应,所以应采取的措施为:
a.升高温度,既能增大反应速率,又能使平衡正向移动,故a符合要求;
b.降低温度,反应速率减小,平衡逆向移动,故b不符合要求;
c.增大压强,反应速率增大,平衡逆向移动,故c不符合要求;
d.降低压强,反应速率减小,平衡正向移动,能提高产率,但反应速率减小,单位时间内异丁烯的产量不一定提高,故d不符合要求,
e.使用催化剂,对平衡移动无影响,不会提高异丁烷的平衡转化率,故e不符合要求,
故答案为:>,a。
②平衡常数的表达式中的平衡浓度可以用平衡时各气体的分压代替(气体a的分压=气体a的物质的量分数×总压强,即p(a)=x(a)×p(总)。图中的A点状态下,总压强p=0.1MPa,异丁烷的平衡转化率为80%,设起始状态C4H10物质的量为1mol,根据变化的量=起始的量×转化率可知,达平衡时n(C4H10)=1-1×80%=0.2mol,n(C4H8)=0.8mol,n(H2)=0.8mol,则各分压为p(C4H10)=$\frac{{0.2mol}}{{0.2mol+0.8mol+0.8mol}}$×0.1MPa=$\frac{{0.1}}{9}$MPa,p(C4H8)=$\frac{{0.8mol}}{{0.2mol+0.8mol+0.8mol}}$×0.1MPa=$\frac{{0.4}}{9}$MPa,同理,p(H2)=$\frac{{0.4}}{9}$MPa,平衡常数Kp=$\frac{{p({C_4}{H_8})×p({H_2})}}{{p({C_4}{H_{10}})}}$=$\frac{{\frac{{0.4}}{9}×\frac{{0.4}}{9}}}{{\frac{{0.1}}{9}}}$=0.18,
故答案为:0.18;
(3)①根据异丁烷的转化率=$\frac{{变化的物质的量}}{{起始的物质的量}}$×100%和异丁烯的选择性=$\frac{{生成目标产物所消耗的反应物的量}}{{参与反应的反应物的量}}×100%$,由C4H10(g)=C4H8(g)+H2(g)+123△H=+123kJ/mol方程式可知,消耗异丁烷的物质的量与生成异丁烯的物质的量相等的,所以,根据异丁烷的起始量求出异丁烯的理论产量,根据生成目标产物所消耗的反应物的量可求出异丁烯的实际产量,由异丁烯的产率=$\frac{{实际产量}}{{理论产量}}$×100%,可知在590℃时,异丁烷的转化率为25.6%,异丁烯的选择性为95%,则异丁烯的产率=25.6%×95%=0.243,
故答案为:0.243;
②该反应是吸热反应,升高温度,反应速率加快,平衡正向移动,
故答案为:升高温度,平衡正向移动;升高温度,反应速率加快;
③高于590℃后,异丁烷高温下裂解生成短碳链烃类化合物,有副产物生成,导致异丁烯产率降低,
故答案为:异丁烷高温下裂解生成短碳链烃类化合物,有副产物生成,异丁烯产率降低。