广州一模前大题训练——化工流程题自洁面料就是在普通的面料纤维中加入一层薄薄的纳M二氧化钛。由钛铁矿(主要成分是和的氧化物)制备等产品的一种工艺流程示意如下:钛铁矿 TrO2^+、SO4^(2-) 过滤 滤渣(弃) 滤液 ②冷却 过滤 FeSO4·TH2O TiO^(2+) SO4^2 H TiO3 -|||-浓硫酸 ^3+ ^2+ ①Fe()写出钛铁矿酸浸时,主要成分反应的离子方程式()步骤①加铁的目的是;步骤②冷却的目的是。()上述制备二氧化钛的过程中,可以利用的副产物是;考虑成本和废物综合利用因素,废液中应加入处理。()由金红石制备单质钛,涉及到的步骤为:→己知:①()()()△.·②()()()△一·③()()()()△·则()()2C()()()的△。反应在氩气氛中进行的理由是硫酸亚铁晶体(·)在医药上作补血剂。某课外研究小组测定该补血剂中铁元素的含量,实验步骤如下:请回答下列问题:()证明步骤①滤液中含有的方法是先滴加溶液,再滴加,该过程的现象为:。()步骤②加入过量的目的:。()步骤③中反应的离子方程式:。()步骤④中一系列处理的操作步骤:过滤、、灼烧、、称量。()若实验无损耗,则每片补血剂含铁元素的质量。()该小组有些同学认为用溶液滴定也能进行铁元素含量的测定。(—=)①实验前,首先要精确配制一定物质的量浓度的溶液,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管外,还需。②上述实验中的溶液需要酸化,用于酸化的酸是。.稀硝酸.稀硫酸.稀盐酸.浓硝酸③滴定到终点时的颜色为色。有关钴、镍和铁化合物的性质见下表:氯化钴可用于化学反应催化剂,油漆催干剂,干湿指示剂,啤酒泡沫稳定剂,陶瓷着色剂,制造隐显墨水等。用金属钴板(含少量、)制备氯化钴的工艺流程如下:钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。()“除镍”步骤中,·用量对反应收率的影响,见下表:从表中可知时,除镍效果最好。()“除镍”步骤必须控制在一定的时间内完成,否则沉淀将有部分()生成,试写出反应的化学方程式。()“除铁”步骤中加入双氧水发生反应的离子方程式是.()“除铁”步骤中加入的纯碱作用是。()在“调"步骤中,加盐酸的作用是()已知25℃时,[()].×,则该温度下反应()的平衡常数为。以白云石(化学式表示为·)为原料制备氢氧化镁的工艺流程如下:()根据流程图判断白云石“轻烧”后固体产物的主要成份。则“轻烧”温度应不超过。()流程图中“加热反应”的化学方程式为。()沉淀过程溶液的,此时溶液中()。(已知[()]×)()该工艺中可以循环使用的物质是、(填化学式)。()传统工艺将白云石分解为氧化镁和氧化钙后提取,该工艺采用轻烧白云石的方法,其优点是、。钛铁矿 TrO2^+、SO4^(2-) 过滤 滤渣(弃) 滤液 ②冷却 过滤 FeSO4·TH2O TiO^(2+) SO4^2 H TiO3 -|||-浓硫酸 ^3+ ^2+ ①Fe柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源。液体矿床以钾矿为主,伴生着镁、溴等多种矿产。某研究性学习小组拟取盐湖苦卤的浓缩液(富含、、、、等),来制取较纯净的氯化钾晶体及液溴(),他们设计了如下流程:请根据以上流程,回答相关问题:()操作①的名称是,操作②的所需的主要仪器是()参照右图溶解度曲线,得到的固体的主要成分是(填化学式)。()同学甲提出一些新的方案,对上述操作②后无色溶液进行除杂提纯,其方案如下:、已知试剂是溶液,则溶液的主要成分是(填化学式)。【获取纯净氯化钾】、对溶液加热并不断滴加·一的盐酸溶液,同时用试纸检测溶液,直至时停止加盐酸,得到溶液。该操作的目的是。将溶液倒入蒸发皿中,加热蒸发并用玻璃棒不断搅拌,直到出现较多晶体时,停止加热。【问题讨论】、进行操作⑤中控制溶液可确保除尽,根据提供的数据计算,此时溶液中物质的量浓度为。二氧化氯()是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色的气体,易溶于水。Ⅰ.()可由在存在的条件下与反应制得。则该反应的氧化产物与还原产物的物质的量之比是。Ⅱ.实验室也可用、盐酸、(亚氯酸钠)为原料制备的流程如下:()写出电解时发生反应的化学方程式:;()除去中的可选用的试剂是;(填序号).饱和食盐水.碱石灰.浓硫酸.水()测定(如右图)的过程如下:在锥形瓶中加入足量的碘化钾,用水溶解后,再加硫酸溶液;在玻璃液封管中加入水;将生成的气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用硫代硫酸钠标准溶液滴定(---),共用去硫代硫酸钠溶液。①装置中玻璃液封管的作用是________________②请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式;③滴定终点的现象是:。④测得通入的质量()。(用含、的代数式表示)(已知:的相对分子质量为)红矾钠(重铬酸钠:·)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作辅助剂,在化学工业和制药工业中也和作氧化剂,应用领域十分广泛。实验室中红矾钠可用一种铬铁矿(主要成分:·,还含有少量的氧化物)通过以下过程来制取。铬铁矿等原料溶液产品:·铬渣(含硫酸钠)回答下列问题:()步骤中反应的化学方程式为:·→在常温下该反应速率极慢,下列措施中能使反应速率增大的是。(填字母).将原料粉碎.增加纯碱的用量.升高温度()步骤需将溶液的调至—,并煮沸,其目的是。()步骤中发生反应的离子方程式为。()利用下面的复分解反应,将红矾钠与固体按:物质的量之比混合溶于水后经适当操作可得到晶体。→(已知:温度对氯化钠的溶解度影响很小,对重铬酸钾的溶解度影响较大。)请填写表中空格。硫酸工业中废渣的成分为、、、。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。已知:阳离子以氢氧化物形式完全沉淀时溶液的:一水合氨电离常数×-,其饱和溶液中(-)约为×·。请回答:()写出与氢氟酸反应的化学方程式:。()上述流程中两次使用试剂,推测试剂是(填以下字母编号).水 .氧化铝.氨水.氢氧化钠()溶液到固体过程中需要控制溶液,如果过小,可能导致的后果是。(任写点)()写出的反应离子方程式:。()证明溶液的主要阴离子(-、-除外)的方法是。铬铁矿的主要成分可表示为·,还含有、等杂质,以铬铁矿为原料制备重铬酸钾()的过程如下图所示。已知:①遇水强烈水解。②--请回答:()中元素的化合价是。()煅烧铬铁矿生成和反应的化学方程式是。()滤渣为红褐色的固体,滤渣的成分是(填名称),滤液的成分除、外,还含有(填化学式)。()利用滤渣,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是。()写出由滤液转化为溶液应采取的措施是。()向溶液中加入固体,获得晶体的操作依次是:加热浓缩、、过滤、洗涤、干燥。锆()元素是核反应堆燃料棒的包裹材料,二氧化锆()可以制造耐高温纳M陶瓷。我国有丰富的锆英石(),含、、等杂质,生产锆的流程之一如下:()写出上述流程中高温气化的反应方程式(碳转化成):()写出•在900℃生成的反应方程式()关于二氧化锆纳M陶瓷和锆合金的说法不正确的是(单选).二氧化锆纳M陶瓷是一种新型材料.纳M级二氧化锆是一种胶体.锆合金的硬度比纯锆要高.日本福岛核电站爆炸可能是由锆合金在高温下与水蒸气反应产生的氢气爆炸引起()一种新型燃料电池,一极通入空气,另一极通入甲烷;电解质是掺杂氧化钇()的氧化锆()晶体,在熔融状态下能传导。在熔融电解质中,向(填正负)极移动。电池正极电极反应为:,负极电极反应为:。工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(),其工艺流程如下:已知:.溶解度随温度的升高而增大,适当条件下可结晶析出。.高氯酸是至今为止人们已知酸中的最强酸,沸点90℃。请回答下列问题()反应器Ⅰ中发生反应的化学方程式为,冷却的目的是,能用蒸馏法分离出高氯酸的原因是。()反应器Ⅱ中发生反应的离子方程式为。()通入反应器Ⅱ中的用另一物质代替同样能生成,请简要说明双氧水在反应中能代替的原因是()()、、、等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有请写出工业上用氯气和溶液生产另一种消毒剂的离子方程式()+++(分)将还原为(分);析出或分离、或得到·(分)·(分);石灰或碳酸钙、废碱(分)·(分);防止高温下与空气中的或、作用(分)()氯水(或双氧水等合理氧化剂)(分);溶液由浅绿色变成血红色(分)()将全部氧化成(分)()+-)↓(或·)↓)(分)()洗涤(分);冷却(分)()(分)()容量瓶(分);(分);紫(或紫红)(分)钛铁矿 TrO2^+、SO4^(2-) 过滤 滤渣(弃) 滤液 ②冷却 过滤 FeSO4·TH2O TiO^(2+) SO4^2 H TiO3 -|||-浓硫酸 ^3+ ^2+ ①Fe(分)()、(分)700℃(分)()()↑(分)()×·(分)()()(分)、或·(分)()减少能源消耗(分)、便于分离(分)(其他合理答案也给分,如:减少排放钛铁矿 TrO2^+、SO4^(2-) 过滤 滤渣(弃) 滤液 ②冷却 过滤 FeSO4·TH2O TiO^(2+) SO4^2 H TiO3 -|||-浓硫酸 ^3+ ^2+ ①Fe萃取() ()↑(分)()(分)()①吸收残余的二氧化氯气体,并使锥形瓶内外压强相等(分)②+-+=++-(分)③最后一滴滴下时,溶液由蓝色变为无色,且半分钟内不复原(分)④×-2g(分)()、(分)()除去杂质(分)()→(分)()①过滤(分)②蒸发(分)④冷却,结晶(分)()↑(分)()(分)()镁离子沉淀不完全或氢氧化铝溶解不完全(各分,共分,合理即给分)()-()↓-(分)()取溶液,加入过量()溶液,没有沉淀产生(分,试剂用量不恰当,扣分);再滴加入溶液,有白色沉淀产生,(或再滴加入盐酸,有无色无味气体产生),证明含有-(分)。(合理即给分)()(分)()·(共分,物质正确分,反应条件“高温或煅烧”分,配平分)()氢氧化铁(分);、(共分,每种物质各分)()(熔融)↑(分,物质正确分,反应条件分,配平分)()加稀硫酸酸化(分)()冷却结晶(分)()4C(分)()• ↑↑(分)()(分)()负(分)(分)(分)()+=+++;(分)降低的溶解度,使结晶析出(分)高氯酸的沸点低(分)()++-=-+-+;(分)()有还原性也能把还原为(分)()强氧化性(分)+-=-+-+;(分)
广州一模前大题训练——化工流程题
自洁面料就是在普通的面料纤维中加入一层薄薄的纳M二氧化钛。由钛铁矿(主要成分是和的氧化物)制备等产品的一种工艺流程示意如下:
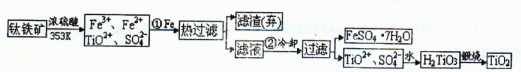
()写出钛铁矿酸浸时,主要成分反应的离子方程式
()步骤①加铁的目的是;步骤②冷却的目的是。
()上述制备二氧化钛的过程中,可以利用的副产物是;考虑成本和废物综合利用因素,废液中应加入处理。
()由金红石制备单质钛,涉及到的步骤为:→
己知:①()()()△.·
②()()()△一·
③()()()()△·
则()()2C()()()的△。
反应在氩气氛中进行的理由是
硫酸亚铁晶体(·)在医药上作补血剂。某课外研究小组测定该补血剂中铁元素的含量,实验步骤如下:
请回答下列问题:
()证明步骤①滤液中含有的方法是先滴加溶液,再滴加,该过程的现象为:。
()步骤②加入过量的目的:。
()步骤③中反应的离子方程式:。
()步骤④中一系列处理的操作步骤:过滤、、灼烧、、称量。
()若实验无损耗,则每片补血剂含铁元素的质量。
()该小组有些同学认为用溶液滴定也能进行铁元素含量的测定。
(—=)
①实验前,首先要精确配制一定物质的量浓度的溶液,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管外,还需。
②上述实验中的溶液需要酸化,用于酸化的酸是。
.稀硝酸.稀硫酸.稀盐酸.浓硝酸
③滴定到终点时的颜色为色。
有关钴、镍和铁化合物的性质见下表:
氯化钴可用于化学反应催化剂,油漆催干剂,干湿指示剂,啤酒泡沫稳定剂,陶瓷着色剂,制造隐显墨水等。用金属钴板(含少量、)制备氯化钴的工艺流程如下:
钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。
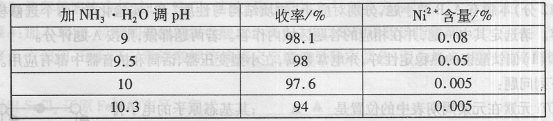
()“除镍”步骤中,·用量对反应收率的影响,见下表:
从表中可知时,除镍效果最好。
()“除镍”步骤必须控制在一定的时间内完成,否则沉淀将有部分()生成,试写出反应的化学方程式。
()“除铁”步骤中加入双氧水发生反应的离子方程式是.
()“除铁”步骤中加入的纯碱作用是。
()在“调"步骤中,加盐酸的作用是
()已知25℃时,[()].×,则该温度下反应()
的平衡常数为。
以白云石(化学式表示为·)为原料制备氢氧化镁的工艺流程如下:
()根据流程图判断白云石“轻烧”后固体产物的主要成份。则“轻烧”温度应不超过。
()流程图中“加热反应”的化学方程式为
。
()沉淀过程溶液的,此时溶液中
()。(已知[()]×)
()该工艺中可以循环使用的物质是、(填化学式)。
()传统工艺将白云石分解为氧化镁和氧化钙后提取,该工艺采用轻烧白云石的方法,其优点是、。
 柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源。液体矿床以钾矿为主,伴生着镁、溴等多种矿产。某研究性学习小组拟取盐湖苦卤的浓缩液(富含、、、、等),来制取较纯净的氯化钾晶体及液溴(),他们设计了如下流程:
柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源。液体矿床以钾矿为主,伴生着镁、溴等多种矿产。某研究性学习小组拟取盐湖苦卤的浓缩液(富含、、、、等),来制取较纯净的氯化钾晶体及液溴(),他们设计了如下流程:
请根据以上流程,回答相关问题:
()操作①的名称是,操作②的所需的主要仪器是
()参照右图溶解度曲线,得到的固体的主要成分是(填化学式)。
()同学甲提出一些新的方案,对上述操作②后无色溶液进行除杂提纯,其方案如下:
、已知试剂是溶液,则溶液的主要成分是(填化学式)。
【获取纯净氯化钾】、对溶液加热并不断滴加·一的盐酸溶液,同时用试纸检测溶液,直至时停止加盐酸,得到溶液。该操作的目的是。将溶液倒入蒸发皿中,加热蒸发并用玻璃棒不断搅拌,直到出现较多晶体时,停止加热。
【问题讨论】、进行操作⑤中控制溶液可确保除尽,根据提供的数据计算,此时溶液中物质的量浓度为。
二氧化氯()是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色的气体,易溶于水。
Ⅰ.()可由在存在的条件下与反应制得。则该反应的氧化产物与还原产物的物质的量之比是。
Ⅱ.实验室也可用、盐酸、(亚氯酸钠)为原料制备的流程如下:
()写出电解时发生反应的化学方程式:;
()除去中的可选用的试剂是;(填序号)
.饱和食盐水.碱石灰.浓硫酸.水
()测定(如右图)的过程如下:在锥形瓶中加入足量的碘化钾,用水溶解后,再加硫酸溶液;在玻璃液封管中加入水;将生成的气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用硫代硫酸钠标准溶液滴定(---),共用去硫代硫酸钠溶液。
①装置中玻璃液封管的作用是________
________
②请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式;
③滴定终点的现象是:。
④测得通入的质量()。(用含、的代数式表示)
(已知:的相对分子质量为)
红矾钠(重铬酸钠:·)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作辅助剂,在化学工业和制药工业中也和作氧化剂,应用领域十分广泛。
实验室中红矾钠可用一种铬铁矿(主要成分:·,还含有少量的氧化物)
通过以下过程来制取。
铬铁矿等原料溶液
产品:·
铬渣(含硫酸钠)
回答下列问题:
()步骤中反应的化学方程式为:·→
在常温下该反应速率极慢,下列措施中能使反应速率增大的是。(填字母)
.将原料粉碎.增加纯碱的用量.升高温度
()步骤需将溶液的调至—,并煮沸,其目的是。
()步骤中发生反应的离子方程式为。
()利用下面的复分解反应,将红矾钠与固体按:物质的量之比混合溶于水后经适当操作可得到晶体。→
(已知:温度对氯化钠的溶解度影响很小,对重铬酸钾的溶解度影响较大。)
请填写表中空格。
硫酸工业中废渣的成分为、、、。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。
已知:阳离子以氢氧化物形式完全沉淀时溶液的:
一水合氨电离常数×-,其饱和溶液中(-)约为×·。
请回答:
()写出与氢氟酸反应的化学方程式:。
()上述流程中两次使用试剂,推测试剂是(填以下字母编号)
.水 .氧化铝.氨水.氢氧化钠
()溶液到固体过程中需要控制溶液,如果过小,可能导致的后果
是。(任写点)
()写出的反应离子方程式:。
()证明溶液的主要阴离子(-、-除外)的方法是
。
铬铁矿的主要成分可表示为·,还含有、等杂质,以铬铁矿为原料制备重铬酸钾()的过程如下图所示。
已知:①遇水强烈水解。②--
请回答:
()中元素的化合价是。
()煅烧铬铁矿生成和反应的化学方程式是
。
()滤渣为红褐色的固体,滤渣的成分是(填名称),滤液的成分除、外,还含有(填化学式)。
()利用滤渣,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是。
()写出由滤液转化为溶液应采取的措施是。
()向溶液中加入固体,获得晶体的操作依次是:
加热浓缩、、过滤、洗涤、干燥。
锆()元素是核反应堆燃料棒的包裹材料,二氧化锆()可以制造耐高温纳M陶瓷。我国有丰富的锆英石(),含、、等杂质,生产锆的流程之一如下:
()写出上述流程中高温气化的反应方程式(碳转化成):
()写出•在900℃生成的反应方程式
()关于二氧化锆纳M陶瓷和锆合金的说法不正确的是(单选)
.二氧化锆纳M陶瓷是一种新型材料.纳M级二氧化锆是一种胶体
.锆合金的硬度比纯锆要高
.日本福岛核电站爆炸可能是由锆合金在高温下与水蒸气反应产生的氢气爆炸引起
()一种新型燃料电池,一极通入空气,另一极通入甲烷;电解质是掺杂氧化钇()的氧化锆()晶体,在熔融状态下能传导。在熔融电解质中,向(填正负)极移动。电池正极电极反应为:,负极电极反应为:。
工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(),其工艺流程如下:
已知:
.溶解度随温度的升高而增大,适当条件下可结晶析出。
.高氯酸是至今为止人们已知酸中的最强酸,沸点90℃。
请回答下列问题
()反应器Ⅰ中发生反应的化学方程式为,冷却的目的是,能用蒸馏法分离出高氯酸的原因是。
()反应器Ⅱ中发生反应的离子方程式为。
()通入反应器Ⅱ中的用另一物质代替同样能生成,请简要说明双氧水在反应中能代替的原因是
()()、、、等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有请写出工业上用氯气和溶液生产另一种消毒剂的离子方程式
()+++(分)
将还原为(分);析出或分离、或得到·(分)
·(分);石灰或碳酸钙、废碱(分)
·(分);防止高温下与空气中的或、作用(分)
()氯水(或双氧水等合理氧化剂)(分);溶液由浅绿色变成血红色(分)
()将全部氧化成(分)
()+-)↓(或·)↓)(分)
()洗涤(分);冷却(分)
()(分)
()容量瓶(分);(分);紫(或紫红)(分)

(分)()、(分)700℃(分)
()()↑(分)
()×·(分)()()(分)、或·(分)
()减少能源消耗(分)、便于分离(分)(其他合理答案也给分,如:减少排放
 萃取
萃取
() ()↑(分)()(分)
()①吸收残余的二氧化氯气体,并使锥形瓶内外压强相等(分)
②+-+=++-(分)
③最后一滴滴下时,溶液由蓝色变为无色,且半分钟内不复原(分)
④×-2g(分)
()、(分)()除去杂质(分)()→(分)
()①过滤(分)②蒸发(分)④冷却,结晶(分)
()↑(分)
()(分)
()镁离子沉淀不完全或氢氧化铝溶解不完全(各分,共分,合理即给分)
()-()↓-(分)
()取溶液,加入过量()溶液,没有沉淀产生(分,试剂用量不恰当,扣分);再滴加入溶液,有白色沉淀产生,(或再滴加入盐酸,有无色无味气体产生),证明含有-(分)。
(合理即给分)
()(分)
()·
(共分,物质正确分,反应条件“高温或煅烧”分,配平分)
()氢氧化铁(分);、(共分,每种物质各分)
()(熔融)↑(分,物质正确分,反应条件分,配平分)
()加稀硫酸酸化(分)()冷却结晶(分)
()4C(分)
()• ↑↑(分)()(分)
()负(分)(分)(分)
()+=+++;(分)
降低的溶解度,使结晶析出(分)高氯酸的沸点低(分)
()++-=-+-+;(分)
()有还原性也能把还原为(分)
()强氧化性(分)+-=-+-+;(分)
题目解答
答案
; .