题目
-8. 在活塞流反应器中进行乙醛分解反应:-|||-(H)_(3)CHOarrow C(H)_(4)+CO-|||-在791K, https:/img.zuoyebang.cc/zyb_edb45fb94979005ac574b74a5cbb9beb.jpg.013times (10)^5Pa, 进料为纯乙醛的条件下,该反应的速率方程为-|||--(r)_(A)=k({C)_(A)}^2 =0.33(m)^3cdot kmolcdot (s)^-1 若乙醛质量流量为 .02kgcdot (s)^-1, 求乙-|||-醛转化率为40%时所需要的反应器有效容积和物料在反应器中的平均停-|||-留时间。

题目解答
答案
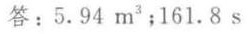
解析
步骤 1:确定反应速率方程和反应物的初始浓度
反应速率方程为 $-{r}_{A}=k{{C}_{A}}^{2}$,其中 $k=0.33{m}^{3}\cdot kmol\cdot {s}^{-1}$。乙醛的质量流量为 $0.02kg\cdot {s}^{-1}$,乙醛的摩尔质量为 $44g/mol$,因此乙醛的摩尔流量为 $0.02/44=0.0004545kmol\cdot {s}^{-1}$。由于进料为纯乙醛,初始浓度 $C_{A0}$ 可以通过摩尔流量和反应器体积 $V$ 来表示,即 $C_{A0} = \frac{0.0004545}{V}$。
步骤 2:计算转化率40%时的浓度
转化率为40%,即 $X=0.4$,则 $C_{A} = C_{A0}(1-X) = C_{A0}(1-0.4) = 0.6C_{A0}$。将 $C_{A0}$ 代入,得到 $C_{A} = 0.6 \times \frac{0.0004545}{V}$。
步骤 3:计算反应器有效容积
根据反应速率方程 $-{r}_{A}=k{{C}_{A}}^{2}$,将 $C_{A}$ 代入,得到 $-{r}_{A}=0.33 \times (0.6 \times \frac{0.0004545}{V})^{2}$。由于 $-{r}_{A} = \frac{0.0004545}{V}$,可以解出 $V$。即 $0.0004545/V = 0.33 \times (0.6 \times \frac{0.0004545}{V})^{2}$,解得 $V = 5.94{m}^{3}$。
步骤 4:计算物料在反应器中的平均停留时间
物料在反应器中的平均停留时间 $\tau$ 可以通过反应器体积 $V$ 除以物料的体积流量 $Q$ 来计算。由于 $Q = \frac{0.02}{44} = 0.0004545kmol\cdot {s}^{-1}$,则 $\tau = \frac{V}{Q} = \frac{5.94}{0.0004545} = 161.8s$。
反应速率方程为 $-{r}_{A}=k{{C}_{A}}^{2}$,其中 $k=0.33{m}^{3}\cdot kmol\cdot {s}^{-1}$。乙醛的质量流量为 $0.02kg\cdot {s}^{-1}$,乙醛的摩尔质量为 $44g/mol$,因此乙醛的摩尔流量为 $0.02/44=0.0004545kmol\cdot {s}^{-1}$。由于进料为纯乙醛,初始浓度 $C_{A0}$ 可以通过摩尔流量和反应器体积 $V$ 来表示,即 $C_{A0} = \frac{0.0004545}{V}$。
步骤 2:计算转化率40%时的浓度
转化率为40%,即 $X=0.4$,则 $C_{A} = C_{A0}(1-X) = C_{A0}(1-0.4) = 0.6C_{A0}$。将 $C_{A0}$ 代入,得到 $C_{A} = 0.6 \times \frac{0.0004545}{V}$。
步骤 3:计算反应器有效容积
根据反应速率方程 $-{r}_{A}=k{{C}_{A}}^{2}$,将 $C_{A}$ 代入,得到 $-{r}_{A}=0.33 \times (0.6 \times \frac{0.0004545}{V})^{2}$。由于 $-{r}_{A} = \frac{0.0004545}{V}$,可以解出 $V$。即 $0.0004545/V = 0.33 \times (0.6 \times \frac{0.0004545}{V})^{2}$,解得 $V = 5.94{m}^{3}$。
步骤 4:计算物料在反应器中的平均停留时间
物料在反应器中的平均停留时间 $\tau$ 可以通过反应器体积 $V$ 除以物料的体积流量 $Q$ 来计算。由于 $Q = \frac{0.02}{44} = 0.0004545kmol\cdot {s}^{-1}$,则 $\tau = \frac{V}{Q} = \frac{5.94}{0.0004545} = 161.8s$。