题目
氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高.(1)根据以上描述,推测氮化硅可能有哪些用途( )(填字母)a.制作坩埚b.用作建筑陶瓷c.制作耐高温轴承d.制作切削刀具(2)请写出氮和硅的原子结构示意图,并根据元素周期律的知识,写出氮化硅的化学式.(3)氮化硅在19世纪已经被化学家合成出来,但直到100多年后才逐渐应用于工业领域。材料的基础研究和实际应用之间存在着一定距离,你认为二者之间的关系是怎样的?请查阅相关资料,与同学交流你的观点.
氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高.
(1)根据以上描述,推测氮化硅可能有哪些用途( )(填字母)
a.制作坩埚
b.用作建筑陶瓷
c.制作耐高温轴承
d.制作切削刀具
(2)请写出氮和硅的原子结构示意图,并根据元素周期律的知识,写出氮化硅的化学式.
(3)氮化硅在19世纪已经被化学家合成出来,但直到100多年后才逐渐应用于工业领域。材料的基础研究和实际应用之间存在着一定距离,你认为二者之间的关系是怎样的?请查阅相关资料,与同学交流你的观点.
题目解答
答案
【答案】
(1)a、b、c、d
(2)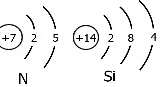 ,Si3N4
,Si3N4
 ,Si3N4
,Si3N4(3)材料的基础研究为实际应用提供了基础,而实际应用则是材料的基础研究的最终归宿。
【解析】
(1)氮化硅硬度大、熔点高可以用来制作坩埚,硬度大用作建筑陶瓷,熔点高、化学性质稳定可制作耐高温轴承,制作切削刀具,故答案为:a、b、c、d
(2)根据原子序数分别为7和14,电子层分别为2和3,最外层电子数分别为5和4,得出原子结构示意图分别为 ;氮原子最外层有5个电子,硅原子最外层有4个电子,氮元素的非金属性强于硅元素,而显-3价,硅元素显+4价,所以氮化硅的化学式为Si3N4;故答案为:
;氮原子最外层有5个电子,硅原子最外层有4个电子,氮元素的非金属性强于硅元素,而显-3价,硅元素显+4价,所以氮化硅的化学式为Si3N4;故答案为: ,Si3N4
,Si3N4
 ;氮原子最外层有5个电子,硅原子最外层有4个电子,氮元素的非金属性强于硅元素,而显-3价,硅元素显+4价,所以氮化硅的化学式为Si3N4;故答案为:
;氮原子最外层有5个电子,硅原子最外层有4个电子,氮元素的非金属性强于硅元素,而显-3价,硅元素显+4价,所以氮化硅的化学式为Si3N4;故答案为: ,Si3N4
,Si3N4(3)氮化硅在19世纪已经被化学家合成出来,但直到100多年后才逐渐应用于工业领域,材料的基础研究为实际应用提供了基础,而实际应用则是材料的基础研究的最终的目的;故答案为:材料的基础研究为实际应用提供了基础,而实际应用则是材料的基础研究的最终归宿。
解析
- (1)用途推测:本题考查物质性质与实际用途的关联。需结合氮化硅的熔点高、硬度大、电绝缘性好、化学性质稳定等特性,对应选项中的应用场景。
- (2)化学式书写:需掌握原子结构示意图的画法(根据原子序数确定电子层分布)和元素周期律(非金属性强弱决定化合价),最终通过化合价交叉确定化学式。
- (3)基础研究与应用关系:需理解科学研究的周期性,明确基础研究是应用的理论支撑,而应用是研究的最终目标。
第(1)题
关键点:根据氮化硅的性质逐一匹配选项:
- a. 制作坩埚:需耐高温,符合熔点高特性。
- b. 建筑陶瓷:硬度大适用。
- c. 耐高温轴承:熔点高、化学稳定。
- d. 切削刀具:硬度大适用。
结论:所有选项均符合,故全选。
第(2)题
原子结构示意图
- 氮原子:原子序数7,电子层分布为2、5,结构示意图:
$\text{N: } \begin{array}{c} +7 \\ \text{核电荷} \\ \end{array} \begin{array}{cc} 2 & 5 \end{array}$ - 硅原子:原子序数14,电子层分布为2、8、4,结构示意图:
$\text{Si: } \begin{array}{c} +14 \\ \text{核电荷} \\ \end{array} \begin{array}{ccc} 2 & 8 & 4 \end{array}$
化学式推导
- 化合价确定:氮非金属性强于硅,故氮显$-3$价,硅显$+4$价。
- 化合价交叉:$+4$(Si)与$-3$(N)交叉得化学式$\text{Si}_3\text{N}_4$。
第(3)题
核心观点:
- 基础研究(如合成氮化硅)是理论支撑,需时间验证其可行性。
- 实际应用(如工业使用)是研究的最终目标,需技术、经济等条件成熟后才能推广。
结论:二者相辅相成,研究推动应用,应用反哺研究方向。