题目
金属钠为体心立方结构,a=429pm,计算:(1)、钠的原子半径;(2)、金属钠的理论密度;(3)、(110)晶面的面间距。
金属钠为体心立方结构,a=429pm,计算:
(1)、钠的原子半径;
(2)、金属钠的理论密度;
(3)、(110)晶面的面间距。
题目解答
答案
解:
(1) 金属钠为体心立方结构,原子在晶胞体对角线方向上互相接触,由此推得原子半径r和晶胞参数a的关系为: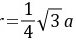 代入数据得:
代入数据得:
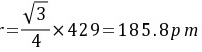
(2) 每个晶胞中含两个钠原子,因此,金属钠的理论密度为:
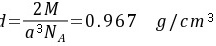
(3) (110)晶面的面间距为:
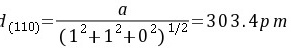
解析
步骤 1:计算钠的原子半径
金属钠为体心立方结构,原子在晶胞体对角线方向上互相接触。由此推得原子半径r和晶胞参数a的关系为:$r=\dfrac{1}{4}\sqrt{3}a$。代入数据得:$r=\dfrac{\sqrt{3}}{4}\times 429=185.8pm$。
步骤 2:计算金属钠的理论密度
每个晶胞中含两个钠原子,因此,金属钠的理论密度为:$\rho=\dfrac{2M}{{a}^{3}{N}_{A}}$,其中M为钠的摩尔质量,$N_{A}$为阿伏伽德罗常数。代入数据得:$\rho=\dfrac{2\times 22.99}{(429\times 10^{-10})^{3}\times 6.022\times 10^{23}}=0.967\quad g/{cm}^{3}$。
步骤 3:计算(110)晶面的面间距
(110)晶面的面间距为:$d(110)=\dfrac{a}{{({1}^{2}+{1}^{2}+{0}^{2})}^{1/2}}$。代入数据得:$d(110)=\dfrac{429}{{(1+1+0)}^{1/2}}=303.4pm$。
金属钠为体心立方结构,原子在晶胞体对角线方向上互相接触。由此推得原子半径r和晶胞参数a的关系为:$r=\dfrac{1}{4}\sqrt{3}a$。代入数据得:$r=\dfrac{\sqrt{3}}{4}\times 429=185.8pm$。
步骤 2:计算金属钠的理论密度
每个晶胞中含两个钠原子,因此,金属钠的理论密度为:$\rho=\dfrac{2M}{{a}^{3}{N}_{A}}$,其中M为钠的摩尔质量,$N_{A}$为阿伏伽德罗常数。代入数据得:$\rho=\dfrac{2\times 22.99}{(429\times 10^{-10})^{3}\times 6.022\times 10^{23}}=0.967\quad g/{cm}^{3}$。
步骤 3:计算(110)晶面的面间距
(110)晶面的面间距为:$d(110)=\dfrac{a}{{({1}^{2}+{1}^{2}+{0}^{2})}^{1/2}}$。代入数据得:$d(110)=\dfrac{429}{{(1+1+0)}^{1/2}}=303.4pm$。