题目
铋(熔点为271.5℃)和锑(熔点为630.7℃)在液态和固态时均能彼此无限互溶,wBi=50%的合金在520时开始结晶处成分为wSb=87%的固相。wBi=80%的合金在400℃时开始结晶出成分为wSb=64%的固相。根据上述条件,(1) 绘出Bi-Sb相图,并标出各线和各相区的名称。(2) 从相图上确定含锑量为wSb=40%合金的开始结晶和结晶终了温度,并求出它在400℃时的平衡相成分及相对量。
铋(熔点为271.5℃)和锑(熔点为630.7℃)在液态和固态时均能彼此无限互溶,wBi=50%的合金在520时开始结晶处成分为wSb=87%的固相。wBi=80%的合金在400℃时开始结晶出成分为wSb=64%的固相。根据上述条件,
(1) 绘出Bi-Sb相图,并标出各线和各相区的名称。
(2) 从相图上确定含锑量为wSb=40%合金的开始结晶和结晶终了温度,并求出它在400℃时的平衡相成分及相对量。
题目解答
答案
答:(1)
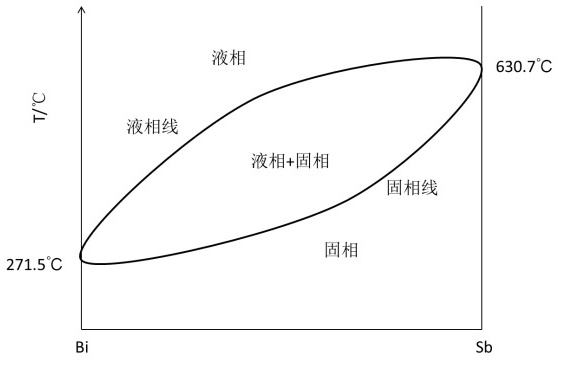
(2)根据相图,含锑量为40%合金开始结晶温度大约为490℃,终了温度为350℃,液相含量54.5%,固相含量45.5%。
解析
本题主要考查二元合金相图的绘制、分析以及利用相图确定合金的结晶温度、平衡相成分和相对量,解题思路如下:
(1)绘制Bi - - Sb相图
- 确定关键点:
- 铋(Bi)的熔点为$271.5^{\circ}C$,在相图中对应横坐标$w_{Bi}=100\%$(即$w_{Sb}=0\%$)处的点,标记为$A$点,温度为$271.5^{\circ}C$。
- 锑(Sb的熔点为$630.7^{\circ}C$,在图中对应横坐标$w_{Bi}=0\%$(即$w_{Sb}=100\%$)处,标记为$B$点,温度为$630.7^{\circ}C$。
- 已知$w_{Bi}=50\%$(即$w_{w_{Sb}} = 50\%$)的合金在$520^{\circ}C$时开始结晶出成分为$w_{Sb}=87\%$的固相,在图中找到横坐标$w_{Sb}=50\%$,纵坐标$520^{\circ}C$的点$C$,以及横坐标$w_{Sb}=87\%$纵坐标$520^{\circ}C$的点$D$。
- 已知$w_{Bi}=80\%}$(即$w_{Sb}=20\%$)的合金在$400^{\circ}C$时开始结晶出成分为$w_{Sb}=64\%$的固相,在图中找到横坐标$w_{Sb}=20\%}$纵坐标$400^{\circ}C$的点$E$,以及横坐标$w_{Sb}=64\%$纵坐标$400^{\circ}C$的点$F$。
绘制液相线和固相线: - 用平滑曲线连接$A$、$C$、$E$、$B$,此曲线为液相线,表示合金处于液态的温度范围。
- 用平滑曲线连接$A$、$过\(C$点作垂线与固相线交点)、(过$E$点作垂线与固相线交点)、$B$,此曲线为固相线,表示合金处于固态的温度范围。
标注相区: - 液相线以上区域为液相区,标注“液相”。
- 固相线以下区域为固相区,标注“固相”。
- 液相线和固相线之间的区域为液相 + 固相区,标注“液相 + 固相”。
- 横坐标两端分别标注$从左到右)“Bi”和“Sb”,纵坐标标注温度,单位为\(^{\circ}C$。
(2)确定含锑量为$w_{Sb}=40\%$合金的相关信息
确定开始结晶和结晶终了温度:
- 在相图横坐标上找到$w_{Sb}=40\%$的位置,作垂线与液相线相交,交点对应的温度即为开始结晶温度,从相图中可读出大约为$490^{\circ}C$。
- 该垂线与固相线交点对应的温度即为结晶终了温度,从相图中可读出大约为$350^{\circ}C$。
计算$400^{\circ}C$时的平衡相成分及相对量: - 确定平衡相成分:在相图中找到$400^{\circ}C$的水平线,该线与液相线交点对应的横坐标为液相成分,与固相线交点对应的为固相成分。从相图中可读出液相成分$w_{L}\approx w_{Sb}=20\%}$,固相成分$w_{S}\approx w_{Sb}=64\%$。
- 相对量计算:根据杠杆定律,设液相相对量为$W_{L}$,固相相对量为$W_{S}$,合金成分点为$w_{0}=w_{Sb}=40\%$。
杠杆定律公式为$W_{L}=\frac{w_{S}-w_{0}}{w_{S}-w_{L}}}$,$W_{S}=\frac{w_{0}-w_{S}}{w_{}-w_{L}}$。
代入数据可得:
$W_{L}=\frac{64 - 40}{64 - 20}=\frac{24}{44}\approx0.545 = 54.5$
$W_{S}=\frac{40 - 20}{64 - 20}=\frac{20}{44}\approx0.455 = 45.5\%$