题目
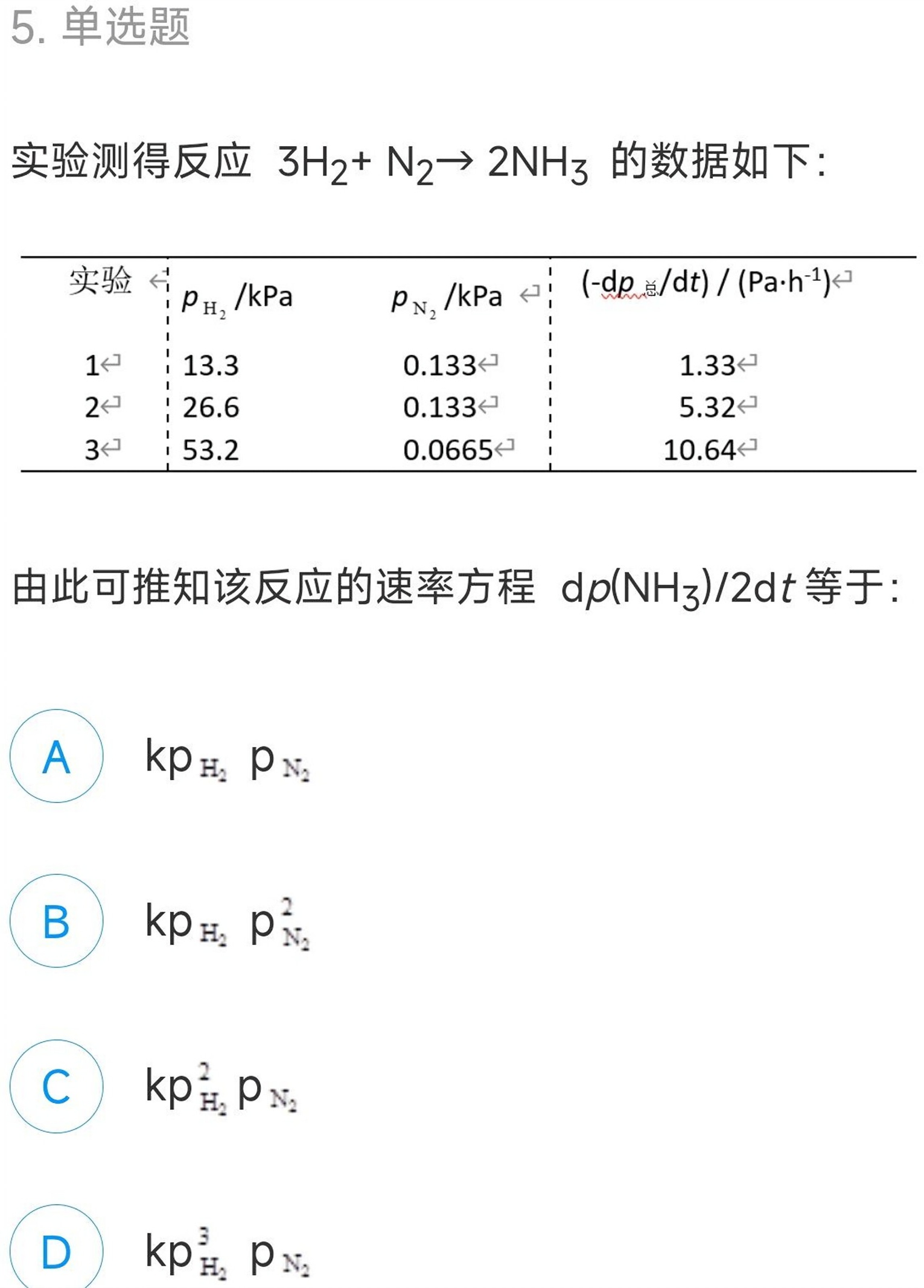
5.单选题-|||-实验测得反应 (H)_(2)+(N)_(2)arrow 2N(H)_(3) 的数据如下:-|||-实验 pH2/kPa ._({N)_(2)}/kPa .(-dp,|dt)/(pacdot (h)^-1)-|||-1 13.3 0.133 1.33-|||-2← 26.6 0.133 5.32-|||-3 53.2 0.0665 10.64-|||-由此可推知该反应的速率方程 (N(H)_(3))/2dt 等于:-|||-A kpH2 p N2-|||-B kpH2 p2^2-|||-C kp 2H2N2-|||-D kp3^(H2) pN2
题目解答
答案
A. kpH2 p N2
解析
步骤 1:分析实验数据
根据实验数据,当氢气的分压保持不变时,氮气的分压增大,反应速率也增大,且反应速率与氮气的分压成正比。这表明氮气的分压对反应速率的影响是线性的,即反应速率与氮气的分压成正比。
步骤 2:分析氢气的分压对反应速率的影响
当氮气的分压保持不变时,氢气的分压增大,反应速率也增大,且反应速率与氢气的分压成正比。这表明氢气的分压对反应速率的影响也是线性的,即反应速率与氢气的分压成正比。
步骤 3:确定反应速率方程
根据上述分析,反应速率与氢气和氮气的分压成正比,因此反应速率方程为:
\[ \frac{d[NH_3]}{dt} = k p_{H_2} p_{N_2} \]
根据实验数据,当氢气的分压保持不变时,氮气的分压增大,反应速率也增大,且反应速率与氮气的分压成正比。这表明氮气的分压对反应速率的影响是线性的,即反应速率与氮气的分压成正比。
步骤 2:分析氢气的分压对反应速率的影响
当氮气的分压保持不变时,氢气的分压增大,反应速率也增大,且反应速率与氢气的分压成正比。这表明氢气的分压对反应速率的影响也是线性的,即反应速率与氢气的分压成正比。
步骤 3:确定反应速率方程
根据上述分析,反应速率与氢气和氮气的分压成正比,因此反应速率方程为:
\[ \frac{d[NH_3]}{dt} = k p_{H_2} p_{N_2} \]