题目
某温度下,向10mL 0.1mol·L-1 CaCl2溶液中滴加0.1mol·L-1的Na2CO3溶液(此时不考虑CO(}_{3)^2-的水解),滴加过程中溶液中-lgc(Ca2+)与Na2CO3溶液体积V的关系如图所示,下列有关说法正确的是() -lgc(Ca^2) ----|||-------|||---- 72-|||-3 + x-|||-w-|||-o 10 20 V(Na,CO3)/m L A.z点对应的分散系很稳定 B.w、x、y三点中,水的电离程度最大的为w点 C.若用等浓度的Na2SO4溶液代替Na2CO3溶液,则图像在x点后的变化如虚线部分所示 D.此温度下,Ksp(CaCO3)=1×10-8.6
某温度下,向10mL 0.1mol·L-1 CaCl2溶液中滴加0.1mol·L-1的Na2CO3溶液(此时不考虑CO${}_{3}^{2-}$的水解),滴加过程中溶液中-lgc(Ca2+)与Na2CO3溶液体积V的关系如图所示,下列有关说法正确的是()
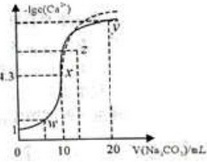
A.z点对应的分散系很稳定
B.w、x、y三点中,水的电离程度最大的为w点
C.若用等浓度的Na2SO4溶液代替Na2CO3溶液,则图像在x点后的变化如虚线部分所示
D.此温度下,Ksp(CaCO3)=1×10-8.6
题目解答
答案
D。
解:A、z点不在曲线上,此时碳酸钠过量,形成碳酸钙悬浊液,悬浊液不稳定,A错误;
B、y点碳酸钠过量最多,碳酸根水解促进水的电离,因此水的电离程度最大的为y点,B错误;
C、硫酸钙微溶,因此若用等浓度的Na2SO4溶液代替Na2CO3溶液,则图像在x点后的变化应该在实线下方,C错误;
D、x点二者恰好反应,此时溶液中碳酸根、钙离子浓度均是10-4.3mol/L,所以Ksp(CaCO3)=1×10-8.6mol2/L2,D正确;
故选D。
解析
步骤 1:分析z点对应的分散系稳定性
z点不在曲线上,此时碳酸钠过量,形成碳酸钙悬浊液,悬浊液不稳定。
步骤 2:分析w、x、y三点中水的电离程度
y点碳酸钠过量最多,碳酸根水解促进水的电离,因此水的电离程度最大的为y点。
步骤 3:分析Na_2SO_4溶液代替Na_2CO_3溶液后图像变化
硫酸钙微溶,因此若用等浓度的Na_2SO_4溶液代替Na_2CO_3溶液,则图像在x点后的变化应该在实线下方。
步骤 4:计算K_sp(CaCO_3)
x点二者恰好反应,此时溶液中碳酸根、钙离子浓度均是10^{-}^{4.3}mol/L,所以K_sp(CaCO_3)=1×10^{-8.6}mol^{2}/L^{2}。
z点不在曲线上,此时碳酸钠过量,形成碳酸钙悬浊液,悬浊液不稳定。
步骤 2:分析w、x、y三点中水的电离程度
y点碳酸钠过量最多,碳酸根水解促进水的电离,因此水的电离程度最大的为y点。
步骤 3:分析Na_2SO_4溶液代替Na_2CO_3溶液后图像变化
硫酸钙微溶,因此若用等浓度的Na_2SO_4溶液代替Na_2CO_3溶液,则图像在x点后的变化应该在实线下方。
步骤 4:计算K_sp(CaCO_3)
x点二者恰好反应,此时溶液中碳酸根、钙离子浓度均是10^{-}^{4.3}mol/L,所以K_sp(CaCO_3)=1×10^{-8.6}mol^{2}/L^{2}。