题目
一棕黑色固体(A)不溶于水,但可溶于浓盐酸,生成近乎无色溶液(B) 和黄绿色气体(C)。在少量(B)中加入硝酸和少量rm(NaBiO_3^) (s),生成紫红色溶液(D)。 在(D)中加入一淡绿色溶液(E),紫红色褪去,在得到的溶液(F)中加入KNCS溶液又生成血红色溶液(G)。再加入足量的NaF则溶液的颜色又褪去。在(E)中加入rm(BaCl_2^) 溶液则生成不溶于硝酸的白色沉淀(H)。试确定各字母所代表的物质,并写出有关反应的离子方程式。
一棕黑色固体(A)不溶于水,但可溶于浓盐酸,生成近乎无色溶液(B) 和黄绿色气体(C)。在少量(B)中加入硝酸和少量$$\rm{NaBiO_3^{}} $$(s),生成紫红色溶液(D)。 在(D)中加入一淡绿色溶液(E),紫红色褪去,在得到的溶液(F)中加入KNCS溶液又生成血红色溶液(G)。再加入足量的NaF则溶液的颜色又褪去。在(E)中加入$$\rm{BaCl_2^{}} $$ 溶液则生成不溶于硝酸的白色沉淀(H)。试确定各字母所代表的物质,并写出有关反应的离子方程式。
题目解答
答案
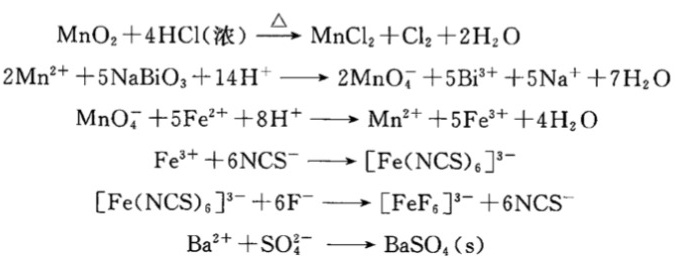
解析
步骤 1:确定固体(A)和生成物(B)、(C)
根据题目描述,固体(A)不溶于水,但可溶于浓盐酸,生成近乎无色溶液(B)和黄绿色气体(C)。这提示我们固体(A)可能是二氧化锰($$\rm{MnO_2}$$),因为二氧化锰不溶于水,但可以与浓盐酸反应生成氯化锰($$\rm{MnCl_2}$$)和氯气($$\rm{Cl_2}$$)。
步骤 2:确定溶液(D)
在少量(B)中加入硝酸和少量$$\rm{NaBiO_3^{}} $$(s),生成紫红色溶液(D)。这提示我们溶液(D)可能是高锰酸根离子($$\rm{MnO_4^-}$$),因为高锰酸根离子在酸性条件下是紫红色的。
步骤 3:确定溶液(E)和(F)
在(D)中加入一淡绿色溶液(E),紫红色褪去,在得到的溶液(F)中加入KNCS溶液又生成血红色溶液(G)。这提示我们溶液(E)可能是亚铁离子($$\rm{Fe^{2+}}$$),因为亚铁离子在酸性条件下是淡绿色的,与高锰酸根离子反应生成铁离子($$\rm{Fe^{3+}}$$),铁离子与硫氰酸根离子($$\rm{SCN^-}$$)反应生成血红色的硫氰酸铁络合物($$\rm{[Fe(SCN)_6]^{3-}}$$)。
步骤 4:确定溶液(G)和(H)
在(E)中加入$$\rm{BaCl_2^{}} $$ 溶液则生成不溶于硝酸的白色沉淀(H)。这提示我们溶液(E)中可能含有硫酸根离子($$\rm{SO_4^{2-}}$$),因为硫酸根离子与钡离子($$\rm{Ba^{2+}}$$)反应生成不溶于硝酸的硫酸钡($$\rm{BaSO_4}$$)沉淀。
根据题目描述,固体(A)不溶于水,但可溶于浓盐酸,生成近乎无色溶液(B)和黄绿色气体(C)。这提示我们固体(A)可能是二氧化锰($$\rm{MnO_2}$$),因为二氧化锰不溶于水,但可以与浓盐酸反应生成氯化锰($$\rm{MnCl_2}$$)和氯气($$\rm{Cl_2}$$)。
步骤 2:确定溶液(D)
在少量(B)中加入硝酸和少量$$\rm{NaBiO_3^{}} $$(s),生成紫红色溶液(D)。这提示我们溶液(D)可能是高锰酸根离子($$\rm{MnO_4^-}$$),因为高锰酸根离子在酸性条件下是紫红色的。
步骤 3:确定溶液(E)和(F)
在(D)中加入一淡绿色溶液(E),紫红色褪去,在得到的溶液(F)中加入KNCS溶液又生成血红色溶液(G)。这提示我们溶液(E)可能是亚铁离子($$\rm{Fe^{2+}}$$),因为亚铁离子在酸性条件下是淡绿色的,与高锰酸根离子反应生成铁离子($$\rm{Fe^{3+}}$$),铁离子与硫氰酸根离子($$\rm{SCN^-}$$)反应生成血红色的硫氰酸铁络合物($$\rm{[Fe(SCN)_6]^{3-}}$$)。
步骤 4:确定溶液(G)和(H)
在(E)中加入$$\rm{BaCl_2^{}} $$ 溶液则生成不溶于硝酸的白色沉淀(H)。这提示我们溶液(E)中可能含有硫酸根离子($$\rm{SO_4^{2-}}$$),因为硫酸根离子与钡离子($$\rm{Ba^{2+}}$$)反应生成不溶于硝酸的硫酸钡($$\rm{BaSO_4}$$)沉淀。