5.【重庆市2021年普通高中学业水平选择考适应性测试】草酸H2C2O4是二元弱酸。向100mL 0.40 mol/L H2C2O4溶液中加入1.0mol/L NaOH溶液调节pH,加水控制溶液体积为200mL。测得溶液中微粒的δ(x)随pH变化曲线如图所示,δ(x)=((H)_(2)(C)_(2)(O)_(4))+c((H{C)_(2)(O)_(4)}^-)+c(({C)_(2)(O)_(4)}^2-),x代表微粒H2C2O4、HC2O((H)_(2)(C)_(2)(O)_(4))+c((H{C)_(2)(O)_(4)}^-)+c(({C)_(2)(O)_(4)}^2-)或C2O((H)_(2)(C)_(2)(O)_(4))+c((H{C)_(2)(O)_(4)}^-)+c(({C)_(2)(O)_(4)}^2-)。下列叙述正确的是((H)_(2)(C)_(2)(O)_(4))+c((H{C)_(2)(O)_(4)}^-)+c(({C)_(2)(O)_(4)}^2-)A.曲线Ⅰ是HC2O((H)_(2)(C)_(2)(O)_(4))+c((H{C)_(2)(O)_(4)}^-)+c(({C)_(2)(O)_(4)}^2-)的变化曲线B.草酸H2C2O4的电离常数K=1.0×10-1.22C.在b点,c(C2O((H)_(2)(C)_(2)(O)_(4))+c((H{C)_(2)(O)_(4)}^-)+c(({C)_(2)(O)_(4)}^2-))+2c(OH-)=c(HC2O((H)_(2)(C)_(2)(O)_(4))+c((H{C)_(2)(O)_(4)}^-)+c(({C)_(2)(O)_(4)}^2-))+c(H+)D.在c点,c(HC2O((H)_(2)(C)_(2)(O)_(4))+c((H{C)_(2)(O)_(4)}^-)+c(({C)_(2)(O)_(4)}^2-))=0.06mol/L
5.【重庆市2021年普通高中学业水平选择考适应性测试】草酸H2C2O4是二元弱酸。向100mL 0.40 mol/L H2C2O4溶液中加入1.0mol/L NaOH溶液调节pH,加水控制溶液体积为200mL。测得溶液中微粒的δ(x)随pH变化曲线如图所示,δ(x)=![]() ,x代表微粒H2C2O4、HC2O
,x代表微粒H2C2O4、HC2O![]() 或C2O
或C2O![]() 。下列叙述正确的是
。下列叙述正确的是
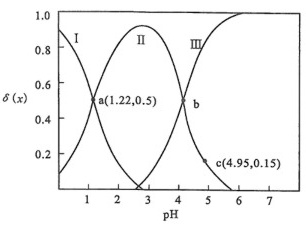
A.曲线Ⅰ是HC2O![]() 的变化曲线
的变化曲线
B.草酸H2C2O4的电离常数K=1.0×10-1.22
C.在b点,c(C2O![]() )+2c(OH-)=c(HC2O
)+2c(OH-)=c(HC2O![]() )+c(H+)
)+c(H+)
D.在c点,c(HC2O![]() )=0.06mol/L
)=0.06mol/L
题目解答
答案
【答案】B
【详解】
A.当酸性越强时,曲线Ⅰ表示的微粒的含量越高,可推知曲线Ⅰ是H2C2O4的变化曲线,曲线Ⅱ是HC2O![]() 的变化曲线,曲线Ⅲ是C2O
的变化曲线,曲线Ⅲ是C2O![]() 的变化曲线,A错误;
的变化曲线,A错误;
B.在a点H2C2O4的浓度和HC2O![]() 的浓度相等,pH=1.22,则草酸H2C2O4的电离常K=
的浓度相等,pH=1.22,则草酸H2C2O4的电离常K= 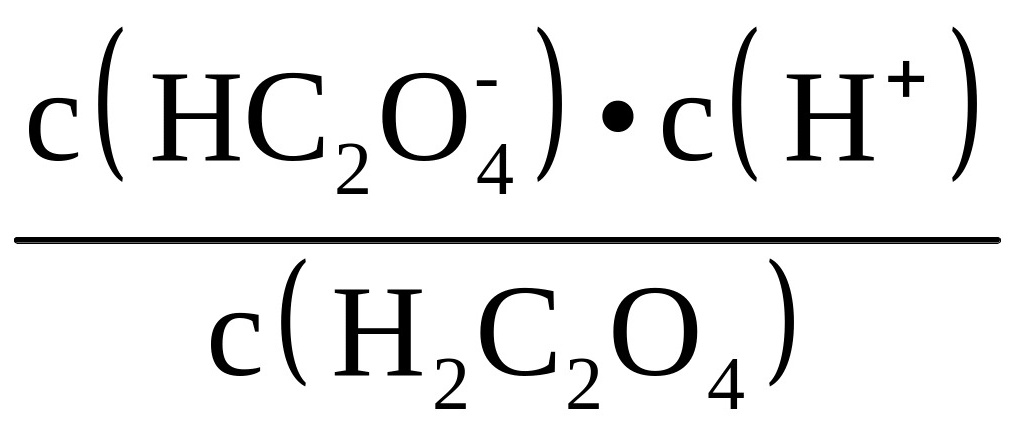 =
=![]() =10-1.22,则B正确;
=10-1.22,则B正确;
C.在b点,c(C2O![]() )=c(HC2O
)=c(HC2O![]() ),且溶液呈酸性,若c(C2O
),且溶液呈酸性,若c(C2O![]() )+2c(OH-)=c(HC2O
)+2c(OH-)=c(HC2O![]() )+c(H+),则2c(OH-)=c(H+),显然不成立,C错误;
)+c(H+),则2c(OH-)=c(H+),显然不成立,C错误;
D.在c点,HC2O![]() 的含量为0.15,而H2C2O4的物质的量为0.1L×0.40 mol/L=0.04 mol,则HC2O
的含量为0.15,而H2C2O4的物质的量为0.1L×0.40 mol/L=0.04 mol,则HC2O![]() 的物质的量为0.15×0.04mol=0.006 mol,溶液体积为0.2L,c(HC2O
的物质的量为0.15×0.04mol=0.006 mol,溶液体积为0.2L,c(HC2O![]() )=0.006mol÷0.2L=0.03 mol/L,D错误;
)=0.006mol÷0.2L=0.03 mol/L,D错误;
故选B。
解析
本题考查弱酸的电离平衡及溶液中微粒浓度关系,需结合δ(x)曲线分析各微粒浓度变化规律。关键点在于:
- 曲线对应关系:根据pH变化趋势,判断曲线Ⅰ、Ⅱ、Ⅲ分别对应H₂C₂O₄、HC₂O₄⁻、C₂O₄²⁻的浓度变化。
- 电离常数计算:利用等浓度点(如a点)确定电离常数。
- 电荷守恒与物料平衡:结合溶液酸碱性验证选项中的等式是否成立。
- 浓度计算:根据δ(x)定义及溶液体积计算微粒浓度。
选项A分析
当pH较低时,草酸主要以H₂C₂O₄分子形式存在,此时δ(x)主要由H₂C₂O₄贡献,对应曲线Ⅰ。随着pH升高,H₂C₂O₄电离为HC₂O₄⁻(曲线Ⅱ),进一步电离为C₂O₄²⁻(曲线Ⅲ)。因此,曲线Ⅰ是H₂C₂O₄的变化曲线,选项A错误。
选项B分析
在a点(pH=1.22),H₂C₂O₄与HC₂O₄⁻的浓度相等。根据电离平衡:
$K_1 = \frac{[HC_2O_4^-][H^+]}{[H_2C_2O_4]} = [H^+] = 10^{-\text{pH}} = 10^{-1.22}$
因此,草酸的电离常数$K_1 = 1.0 \times 10^{-1.22}$,选项B正确。
选项C分析
在b点(pH=4.95),$c(C_2O_4^{2-}) = c(HC_2O_4^-)$,溶液呈酸性($c(H^+) > c(OH^-)$)。若等式成立:
$c(C_2O_4^{2-}) + 2c(OH^-) = c(HC_2O_4^-) + c(H^+)$
代入$c(C_2O_4^{2-}) = c(HC_2O_4^-)$,得$2c(OH^-) = c(H^+)$,但此时$c(H^+) > c(OH^-)$,等式不成立,选项C错误。
选项D分析
在c点(δ(x)=0.15),HC₂O₄⁻的浓度占比为0.15。原草酸物质的量为:
$0.1 \, \text{L} \times 0.40 \, \text{mol/L} = 0.04 \, \text{mol}$
总溶液中δ(x)对应的物质的量为:
$0.15 \times 0.04 \, \text{mol} = 0.006 \, \text{mol}$
溶液体积为0.2 L,故:
$c(HC_2O_4^-) = \frac{0.006}{0.2} = 0.03 \, \text{mol/L}$
选项D中$c(HC_2O_4^-) = 0.06 \, \text{mol/L}$错误。