(12分,每空2分)(1)________________________________________________________________________________________________________________________(2)________(3)______、________________________(4)______。(5)______。一、选择题(每小题只有一个选项符合题意,-|||-每小题3分,共60分)-|||-1. 下 列 说 法正 确 的 是-|||-(-|||-)-|||-A.牺牲阴极的阳极保护法是应用电解原-|||-理防止金属的腐蚀-|||-B.CO的标准燃烧热是 .0kJcdot mo(l)^-1,-|||-则 (O)_(2)(g)=2CO(g)+(O)_(2)(g) 反应的-|||-Delta H=+566.0kJcdot mo(l)^-1-|||-C.一个反应能否自发进行取决于该反应一、选择题(每小题只有一个选项符合题意,-|||-每小题3分,共60分)-|||-1. 下 列 说 法正 确 的 是-|||-(-|||-)-|||-A.牺牲阴极的阳极保护法是应用电解原-|||-理防止金属的腐蚀-|||-B.CO的标准燃烧热是 .0kJcdot mo(l)^-1,-|||-则 (O)_(2)(g)=2CO(g)+(O)_(2)(g) 反应的-|||-Delta H=+566.0kJcdot mo(l)^-1-|||-C.一个反应能否自发进行取决于该反应粒太小的沉淀3.在中和热测定的实验中不需要用到的仪器是( )A.量筒B.温度计C.环形玻璃搅拌棒D.天平4.表中实验操作能达到实验目的的是( )5.氯化钴溶液中存在下列平衡:[CoCl4]2-+6H2O[Co(H2O)6]2++4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是()A.由粉红色变为蓝色B .蓝色加深C .红色加深D .由蓝色变为粉红色6.反应C(s)+H2O(g)一、选择题(每小题只有一个选项符合题意,-|||-每小题3分,共60分)-|||-1. 下 列 说 法正 确 的 是-|||-(-|||-)-|||-A.牺牲阴极的阳极保护法是应用电解原-|||-理防止金属的腐蚀-|||-B.CO的标准燃烧热是 .0kJcdot mo(l)^-1,-|||-则 (O)_(2)(g)=2CO(g)+(O)_(2)(g) 反应的-|||-Delta H=+566.0kJcdot mo(l)^-1-|||-C.一个反应能否自发进行取决于该反应CO(g)+H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是()A.在密闭容器中通入水蒸气B.升温C.保持体积不变,充入氦气使体系压强增大D.保持压强不变,充入氦气使容器体积增大7.为了除去氯化镁酸性溶液中的Fe3+离子,可在加热搅拌下加入一种试剂,过滤后再加入适量盐酸。这种试剂是()A.稀氨水B.氢氧化钠C. 碳酸镁D.碳酸钠8.汽车上用的铅蓄电池是以一组充满海绵状态的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解液。总反应为:Pb+PbO2+2H2SO42PbSO4+2H2O下列叙述正确的是()A.充电时阴极反应为:Pb + SO42--2e-=PbSO4B.放电时,当外电路上有2mol电子通过时,溶液中消耗H2SO4的物质的量为1molC.放电时溶液中H+向负极移动D.充电时阳极附近溶液的pH减小9.下列各组离子一定可以大量共存的是()A.在含大量Al3+的溶液中:NH、Na+、HCO3-、SO42-B.能使甲基橙试液变红的溶液中:Na+、K+、MnO4-、NO3-C.在水电离出的c(H+) =10-13mol·L-1的溶液中:NH一、选择题(每小题只有一个选项符合题意,-|||-每小题3分,共60分)-|||-1. 下 列 说 法正 确 的 是-|||-(-|||-)-|||-A.牺牲阴极的阳极保护法是应用电解原-|||-理防止金属的腐蚀-|||-B.CO的标准燃烧热是 .0kJcdot mo(l)^-1,-|||-则 (O)_(2)(g)=2CO(g)+(O)_(2)(g) 反应的-|||-Delta H=+566.0kJcdot mo(l)^-1-|||-C.一个反应能否自发进行取决于该反应、[Al(OH)4]-、SO、NOD.在pH=1的溶液中:K+、Fe2+、Cl-、NO2-10.0.1mol/LNaOH溶液和0.1mol/LNH4Cl溶液等体积混合后,溶液中离子浓度关系正确的是( )A.c(NH4+)+ c(H+) =c(OH-)B.c(Na+)=c(Cl-)>c(H+)=c(OH-)C.c(NH4+)+c(NH3·H2O) =2c(Cl-)D.c(NH4+) >c(NH3·H2O)>c(OH-)>c(H+)11.对水的电离平衡不产生影响的粒子是( )A.Al3+B.CH3COOHC.K+D.HCl12.向明矾溶液中滴加Ba(OH)2溶液,当SO42-沉淀完全时,铝元素的存在形式是A.部分为 Al(OH)3沉淀,部分以Al3+形式存在B.全部以[Al(OH)4]-形式存在C.全部为Al(OH)3沉淀D.部分为Al(OH)3,部分为[Al(OH)4]-13.由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol·L-1,c(SO42-)=0.8mol·L-1,则c(K+)为()A.0.15 mol·L-1B.0.2 mol·L-1C.0.3 mol·L-1D.0.4 mol·L-114.用0.2mol/L HCl溶液滴定0.2mol/L NaOH,如果到达滴定的终点时不慎多加了1滴盐酸溶液(1滴溶液的体积约为0.05mL),继续加水至100mL,所得溶液的pH是( )A.4B.1C.10D.3.315.室温下,pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )A.加水稀释2倍后,两溶液的pH均减小B.使温度都升高20℃后,两溶液的pH均不变C.加适量的醋酸钠晶体后,两溶液的pH均增大D.加足量的锌充分反应后,盐酸产生的氢气比醋酸多16.25℃时,5种银盐的溶度积常数(Ksp)分别是:下列说法正确的是( )A.氯化银、溴化银和碘化银的溶解度依次增大B.将硫酸银溶解于水后,向其中加入少量硫化钠溶液,不能得到黑色沉淀C.在5mL1.8×10-5mol/L的NaCl溶液中,加入1滴(1mL约20滴)0.1 mol/L的AgNO3溶液,不能观察到白色沉淀D.将浅黄色溴化银固体浸泡在饱和氯化钠溶液中,可以有少量白色固体生成17.当用碱滴定酸时,下列操作中可能使测定结果(酸的浓度)偏低的是( )A.滴定后读取标准液体积时仰视B.锥形瓶用蒸馏水洗后,未干燥C.碱式滴定管用蒸馏水洗后,未用标准液润洗D.滴定至溶液呈浅红色后,未等到半分钟立即开始读数18.对于反应A(g)+B(g)+C(g)2D(g) (△H>0),下列图象正确的是( )
(12分,每空2分)(1)________________________________________________________________________________________________________________________
(2)________
(3)______、________________________
(4)______。(5)______。


粒太小的沉淀
3.在中和热测定的实验中不需要用到的仪器是( )
A.量筒B.温度计C.环形玻璃搅拌棒D.天平
4.表中实验操作能达到实验目的的是( )
5.氯化钴溶液中存在下列平衡:[CoCl4]2-+6H2O[Co(H2O)6]2++4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是()
A.由粉红色变为蓝色B .蓝色加深C .红色加深D .由蓝色变为粉红色
6.反应C(s)+H2O(g)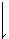 CO(g)+H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是()
CO(g)+H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是()
A.在密闭容器中通入水蒸气B.升温
C.保持体积不变,充入氦气使体系压强增大D.保持压强不变,充入氦气使容器体积增大
7.为了除去氯化镁酸性溶液中的Fe3+离子,可在加热搅拌下加入一种试剂,过滤后再加入适量盐酸。这种试剂是()
A.稀氨水B.氢氧化钠C. 碳酸镁D.碳酸钠
8.汽车上用的铅蓄电池是以一组充满海绵状态的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解液。总反应为:Pb+PbO2+2H2SO42PbSO4+2H2O
下列叙述正确的是()
A.充电时阴极反应为:Pb + SO42--2e-=PbSO4
B.放电时,当外电路上有2mol电子通过时,溶液中消耗H2SO4的物质的量为1mol
C.放电时溶液中H+向负极移动
D.充电时阳极附近溶液的pH减小
9.下列各组离子一定可以大量共存的是()
A.在含大量Al3+的溶液中:NH、Na+、HCO3-、SO42-
B.能使甲基橙试液变红的溶液中:Na+、K+、MnO4-、NO3-
C.在水电离出的c(H+) =10-13mol·L-1的溶液中:NH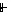 、[Al(OH)4]-、SO、NO
、[Al(OH)4]-、SO、NO
D.在pH=1的溶液中:K+、Fe2+、Cl-、NO2-
10.0.1mol/LNaOH溶液和0.1mol/LNH4Cl溶液等体积混合后,溶液中离子浓度关系正确的是( )
A.c(NH4+)+ c(H+) =c(OH-)B.c(Na+)=c(Cl-)>c(H+)=c(OH-)
C.c(NH4+)+c(NH3·H2O) =2c(Cl-)D.c(NH4+) >c(NH3·H2O)>c(OH-)>c(H+)
11.对水的电离平衡不产生影响的粒子是( )
A.Al3+B.CH3COOHC.K+D.HCl
12.向明矾溶液中滴加Ba(OH)2溶液,当SO42-沉淀完全时,铝元素的存在形式是
A.部分为 Al(OH)3沉淀,部分以Al3+形式存在B.全部以[Al(OH)4]-形式存在
C.全部为Al(OH)3沉淀D.部分为Al(OH)3,部分为[Al(OH)4]-
13.由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol·L-1,c(SO42-)=0.8mol·L-1,则c(K+)为()
A.0.15 mol·L-1B.0.2 mol·L-1C.0.3 mol·L-1D.0.4 mol·L-1
14.用0.2mol/L HCl溶液滴定0.2mol/L NaOH,如果到达滴定的终点时不慎多加了1滴盐酸溶液(1滴溶液的体积约为0.05mL),继续加水至100mL,所得溶液的pH是( )
A.4B.1C.10D.3.3
15.室温下,pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )
A.加水稀释2倍后,两溶液的pH均减小
B.使温度都升高20℃后,两溶液的pH均不变
C.加适量的醋酸钠晶体后,两溶液的pH均增大
D.加足量的锌充分反应后,盐酸产生的氢气比醋酸多
16.25℃时,5种银盐的溶度积常数(Ksp)分别是:
下列说法正确的是( )
A.氯化银、溴化银和碘化银的溶解度依次增大
B.将硫酸银溶解于水后,向其中加入少量硫化钠溶液,不能得到黑色沉淀
C.在5mL1.8×10-5mol/L的NaCl溶液中,加入1滴(1mL约20滴)0.1 mol/L的AgNO3溶
液,不能观察到白色沉淀
D.将浅黄色溴化银固体浸泡在饱和氯化钠溶液中,可以有少量白色固体生成
17.当用碱滴定酸时,下列操作中可能使测定结果(酸的浓度)偏低的是( )
A.滴定后读取标准液体积时仰视
B.锥形瓶用蒸馏水洗后,未干燥
C.碱式滴定管用蒸馏水洗后,未用标准液润洗
D.滴定至溶液呈浅红色后,未等到半分钟立即开始读数
18.对于反应A(g)+B(g)+C(g)2D(g) (△H>0),下列图象正确的是( )
题目解答
答案
(NH4)2SO4+2NaCl===2NH4Cl↓+ Na2SO4 蒸发皿 防止温度降低,氯化铵晶体析出而损失 布氏漏斗的颈口斜面未与吸滤瓶的支管口相对 AD 25%