题目
重铬酸钾常用作有机合成的氧化剂和催化剂等。由含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)制备K2Cr2O7的流程如图所示。KOH i.过量H2O2溶液-|||-滤液① ii.KOH调 =10-|||-含铬废液 一 滤液② i.加热ii.冷却 酸化-|||-喝=7... ... 8 滤渣① ,氧化 (主要溶质为K2C O4) 至 =1 结晶 →K2Cr2O2晶体-|||-滤渣②已知:i.在酸性条件下,H2O2能将Cr2O72-还原为Cr3+。ii.相关金属离子形成氢氧化物沉淀的pH范围如表: 金属离子 Fe3+ Cr3+ 开始沉淀的pH 1.5 4.9 沉淀完全的pH 2.8 6.8 回答下列问题:(1)滤渣①的主要成分为 ____ (填化学式)。(2)“氧化”步骤中发生反应的离子方程式为 ____ 。(3)“加热“操作的目的是 ____ 。(4)“酸化“过程中发生的反应为2CrO42-+2H+⇌Cr2O72-+H2O (K=4.0×1014L3•mol-3)。已知“酸化”后溶液(pH=1)中c(Cr2O72-)=6.4×10-8mol•L-1,则溶液中c(CrO42-)= ____ 。(5)可利用微生物电池将镀铬废水中的Cr2O72-催化还原,其工作原理如图所示:KOH i.过量H2O2溶液-|||-滤液① ii.KOH调 =10-|||-含铬废液 一 滤液② i.加热ii.冷却 酸化-|||-喝=7... ... 8 滤渣① ,氧化 (主要溶质为K2C O4) 至 =1 结晶 →K2Cr2O2晶体-|||-滤渣②在该电池中,b作 ____ 极,a极的电极反应为 ____ (6)K2Cr2O7标准溶液还可用于测定市售硫代硫酸钠晶体(Na2S2O3•5H2O,M=248g•mol-1)的纯度。测定步骤如下:i.溶液配制:称取1.2400g市售硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后。全部转移至100mL容量瓶中。加蒸馏水至刻度线。ii.滴定:取0.01000mol•L-1的K2Cr2O7标准溶液20.00mL,稀硫酸酸化后加入过量KI溶液,发生反应(Cr2O72-被还原成Cr3+,I-被氧化成I2)。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32-═S4O62-+2I-.加入淀粉溶液作为指示剂,继续滴定,当溶液蓝色褪去。即为终点。平行滴定3次,样品溶液的平均用量为25.00mL。①稀硫酸酸化的K2Cr2O7标准溶液与KI溶液反应的离子方程式为 ____ ②该市售硫代硫酸钠晶体样品的纯度为 ____ %(保留1位小数)。
重铬酸钾常用作有机合成的氧化剂和催化剂等。由含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)制备K2Cr2O7的流程如图所示。

已知:i.在酸性条件下,H2O2能将Cr2O72-还原为Cr3+。
ii.相关金属离子形成氢氧化物沉淀的pH范围如表:
回答下列问题:
(1)滤渣①的主要成分为 ____ (填化学式)。
(2)“氧化”步骤中发生反应的离子方程式为 ____ 。
(3)“加热“操作的目的是 ____ 。
(4)“酸化“过程中发生的反应为2CrO42-+2H+⇌Cr2O72-+H2O (K=4.0×1014L3•mol-3)。
已知“酸化”后溶液(pH=1)中c(Cr2O72-)=6.4×10-8mol•L-1,则溶液中c(CrO42-)= ____ 。
(5)可利用微生物电池将镀铬废水中的Cr2O72-催化还原,其工作原理如图所示: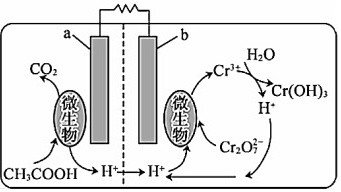
在该电池中,b作 ____ 极,a极的电极反应为 ____
(6)K2Cr2O7标准溶液还可用于测定市售硫代硫酸钠晶体(Na2S2O3•5H2O,M=248g•mol-1)的纯度。测定步骤如下:
i.溶液配制:称取1.2400g市售硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后。全部转移至100mL容量瓶中。加蒸馏水至刻度线。
ii.滴定:取0.01000mol•L-1的K2Cr2O7标准溶液20.00mL,稀硫酸酸化后加入过量KI溶液,发生反应(Cr2O72-被还原成Cr3+,I-被氧化成I2)。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32-═S4O62-+2I-.加入淀粉溶液作为指示剂,继续滴定,当溶液蓝色褪去。即为终点。平行滴定3次,样品溶液的平均用量为25.00mL。
①稀硫酸酸化的K2Cr2O7标准溶液与KI溶液反应的离子方程式为 ____
②该市售硫代硫酸钠晶体样品的纯度为 ____ %(保留1位小数)。

已知:i.在酸性条件下,H2O2能将Cr2O72-还原为Cr3+。
ii.相关金属离子形成氢氧化物沉淀的pH范围如表:
| 金属离子 | Fe3+ | Cr3+ |
| 开始沉淀的pH | 1.5 | 4.9 |
| 沉淀完全的pH | 2.8 | 6.8 |
(1)滤渣①的主要成分为 ____ (填化学式)。
(2)“氧化”步骤中发生反应的离子方程式为 ____ 。
(3)“加热“操作的目的是 ____ 。
(4)“酸化“过程中发生的反应为2CrO42-+2H+⇌Cr2O72-+H2O (K=4.0×1014L3•mol-3)。
已知“酸化”后溶液(pH=1)中c(Cr2O72-)=6.4×10-8mol•L-1,则溶液中c(CrO42-)= ____ 。
(5)可利用微生物电池将镀铬废水中的Cr2O72-催化还原,其工作原理如图所示:

在该电池中,b作 ____ 极,a极的电极反应为 ____
(6)K2Cr2O7标准溶液还可用于测定市售硫代硫酸钠晶体(Na2S2O3•5H2O,M=248g•mol-1)的纯度。测定步骤如下:
i.溶液配制:称取1.2400g市售硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后。全部转移至100mL容量瓶中。加蒸馏水至刻度线。
ii.滴定:取0.01000mol•L-1的K2Cr2O7标准溶液20.00mL,稀硫酸酸化后加入过量KI溶液,发生反应(Cr2O72-被还原成Cr3+,I-被氧化成I2)。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32-═S4O62-+2I-.加入淀粉溶液作为指示剂,继续滴定,当溶液蓝色褪去。即为终点。平行滴定3次,样品溶液的平均用量为25.00mL。
①稀硫酸酸化的K2Cr2O7标准溶液与KI溶液反应的离子方程式为 ____
②该市售硫代硫酸钠晶体样品的纯度为 ____ %(保留1位小数)。
题目解答
答案
解:(1)由以上分析可知滤渣①为Cr(OH)3、Fe(OH)3,
故答案为:Cr(OH)3、Fe(OH)3;
(2)“氧化”步骤中,碱性条件下,过氧化氢氧化Cr(OH)3生成K2CrO4溶液,反应的化学方程式为2Cr(OH)3+3H2O2+4KOH=2K2CrO4+8H2O,
故答案为:2Cr(OH)3+3H2O2+4KOH=2K2CrO4+8H2O;
(3)因为在酸性条件下,H2O2能将Cr2O72-还原为Cr3+,为防止后续“酸化”步骤中H2O2将Cr2O72-还原为Cr3+而混入杂质,所以酸化之前必须除去H2O2,并且H2O2对热不稳定、易分解,通过加热可除去,
故答案为:分解除去过量的H2O2;
(4)“酸化“过程中发生的反应为2CrO42-+2H+⇌Cr2O72-+H2O (K=4.0×1014L3•mol-3),酸化”过程中pH=1,即c(H+)=0.1mol/L,c(Cr2O72-)=6.4×10-8mol•L-1,K=$\frac{6.4×1{0}^{-8}}{{c}^{2}(Cr{{O}_{4}}^{2-})×(0.1)^{2}}$=4×1014,解得c(CrO42-)=4.0×10-8mol•L-1,
故答案为:4.0×10-8mol/L;
(5)由图可知,b上Cr得到电子,发生还原反应,b为正极,a为负极,负极反应式为CH3COOH+2H2O-8e-=2CO2↑+8H+,
故答案为:正;CH3COOH+2H2O-8e-=2CO2↑+8H+;
(6)①稀硫酸酸化的K2Cr2O7标准溶液与KI溶液反应的离子方程式为Cr2O72-+6I-+14H+=3I2+2Cr3++7H2O,
故答案为:Cr2O72-+6I-+14H+=3I2+2Cr3++7H2O;
②由滴定反应Cr2O72-+6I-+14H+=3I2+2Cr3++7H2O、I2+2S2O32-=S4O62-+2I-,可知存在Cr2O72-~3I2~6S2O32-,该市售硫代硫酸钠晶体样品的纯度为$\frac{0.02L×0.01mol/L×6×\frac{100mL}{25mL}×248g/mol}{1.2400g}$×100%=96.0%,
故答案为:96.0。
故答案为:Cr(OH)3、Fe(OH)3;
(2)“氧化”步骤中,碱性条件下,过氧化氢氧化Cr(OH)3生成K2CrO4溶液,反应的化学方程式为2Cr(OH)3+3H2O2+4KOH=2K2CrO4+8H2O,
故答案为:2Cr(OH)3+3H2O2+4KOH=2K2CrO4+8H2O;
(3)因为在酸性条件下,H2O2能将Cr2O72-还原为Cr3+,为防止后续“酸化”步骤中H2O2将Cr2O72-还原为Cr3+而混入杂质,所以酸化之前必须除去H2O2,并且H2O2对热不稳定、易分解,通过加热可除去,
故答案为:分解除去过量的H2O2;
(4)“酸化“过程中发生的反应为2CrO42-+2H+⇌Cr2O72-+H2O (K=4.0×1014L3•mol-3),酸化”过程中pH=1,即c(H+)=0.1mol/L,c(Cr2O72-)=6.4×10-8mol•L-1,K=$\frac{6.4×1{0}^{-8}}{{c}^{2}(Cr{{O}_{4}}^{2-})×(0.1)^{2}}$=4×1014,解得c(CrO42-)=4.0×10-8mol•L-1,
故答案为:4.0×10-8mol/L;
(5)由图可知,b上Cr得到电子,发生还原反应,b为正极,a为负极,负极反应式为CH3COOH+2H2O-8e-=2CO2↑+8H+,
故答案为:正;CH3COOH+2H2O-8e-=2CO2↑+8H+;
(6)①稀硫酸酸化的K2Cr2O7标准溶液与KI溶液反应的离子方程式为Cr2O72-+6I-+14H+=3I2+2Cr3++7H2O,
故答案为:Cr2O72-+6I-+14H+=3I2+2Cr3++7H2O;
②由滴定反应Cr2O72-+6I-+14H+=3I2+2Cr3++7H2O、I2+2S2O32-=S4O62-+2I-,可知存在Cr2O72-~3I2~6S2O32-,该市售硫代硫酸钠晶体样品的纯度为$\frac{0.02L×0.01mol/L×6×\frac{100mL}{25mL}×248g/mol}{1.2400g}$×100%=96.0%,
故答案为:96.0。