题目
石墨在材料领域有重要 应用.某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质.设计的提纯与综合利用工艺如图:(注:SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃)活性炭 气体I 80℃冷凝 气体Ⅱ NaOH溶液 含水玻璃的混合溶 过量NaOH溶液酸氢钠溶液 固体Ⅲ 步骤① 溶液IV 加热 →沉淀v -|||-初级 Cl2-|||-石墨1500℃-|||-纯化石 墨→..... 石墨电极(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是 ____ .(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物.气体Ⅰ中的碳氧化物主要为 ____ .由气体Ⅱ中某物得到水玻璃的化学反应方程式为 ____ .(3)步骤①为:搅拌、 ____ .所得溶液Ⅳ中的阴离子有 ____ .(4)由溶液Ⅳ生成沉淀Ⅴ的总反应的离子方程式为 ____ ,100kg初级石墨最多可能获得Ⅴ的质量为 ____ kg.
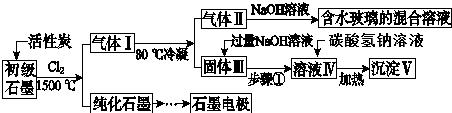
石墨在材料领域有重要 应用.某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质.设计的提纯与综合利用工艺如图:(注:SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃)
(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是 ____ .
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物.气体Ⅰ中的碳氧化物主要为 ____ .由气体Ⅱ中某物得到水玻璃的化学反应方程式为 ____ .
(3)步骤①为:搅拌、 ____ .所得溶液Ⅳ中的阴离子有 ____ .
(4)由溶液Ⅳ生成沉淀Ⅴ的总反应的离子方程式为 ____ ,100kg初级石墨最多可能获得Ⅴ的质量为 ____ kg.

(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是 ____ .
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物.气体Ⅰ中的碳氧化物主要为 ____ .由气体Ⅱ中某物得到水玻璃的化学反应方程式为 ____ .
(3)步骤①为:搅拌、 ____ .所得溶液Ⅳ中的阴离子有 ____ .
(4)由溶液Ⅳ生成沉淀Ⅴ的总反应的离子方程式为 ____ ,100kg初级石墨最多可能获得Ⅴ的质量为 ____ kg.
题目解答
答案
解:(1)石墨化学性质在常温下稳定,而在高温下可与氧气发生反应,所以通入氮气排尽装置中的空气,防止石墨发生氧化反应,减少石墨损失,
故答案为:排除装置中的空气;
(2)石墨过量高温反应后,石墨中氧化物杂质均转变为相应的氯化物,根据杂质的含量可知,气体I中氯化物主要为SiCl4、AlCl3、FeCl3等,气体I中碳氧化物主要为CO,SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃,80℃冷却得到的气体Ⅱ含有SiCl4及CO,SiCl4与氢氧化钠溶液反应得到硅酸钠与氯化钠,化学反应方程式为:SiCl4+6NaOH=Na2SiO3+4NaCl+3H2O,
故答案为:CO;SiCl4+6NaOH=Na2SiO3+4NaCl+3H2O;
(3)金属氯化物的沸点均高于150℃,则固体Ⅲ中存在AlCl3、FeCl3、MgCl2,其中FeCl3、MgCl2与过量的氢氧化钠溶液反应得到沉淀,而氯化铝与过量的氢氧化钠溶液反应生成偏铝酸钠,搅拌、过滤得到溶液IV,故溶液IV中的阴离子有:AlO2-、OH-、Cl-,
故答案为:过滤;AlO2-、OH-、Cl-;
(4)偏铝酸钠发生水解,加入乙酸乙酯除去过量的氢氧化钠,且加热条件下水解平衡一直正向移动,得到氢氧化铝沉淀、醋酸钠、乙醇,由溶液IV生成沉淀V的总反应的离子方程式为AlO2-+CH3COOCH2CH3+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CH3COO-+CH3CH2OH+Al(OH)3↓,
Al2O3的质量分数为5.1%,则100kg初级石墨中氧化铝的质量=100kg×5.1%=5.1kg,根据Al元素守恒,可知氢氧化铝的质量为$\frac{5.1kg×\frac{54}{102}}{\frac{27}{78}}$=7.8kg,
故答案为:AlO2-+CH3COOCH2CH3+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CH3COO-+CH3CH2OH+Al(OH)3↓;7.8.
故答案为:排除装置中的空气;
(2)石墨过量高温反应后,石墨中氧化物杂质均转变为相应的氯化物,根据杂质的含量可知,气体I中氯化物主要为SiCl4、AlCl3、FeCl3等,气体I中碳氧化物主要为CO,SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃,80℃冷却得到的气体Ⅱ含有SiCl4及CO,SiCl4与氢氧化钠溶液反应得到硅酸钠与氯化钠,化学反应方程式为:SiCl4+6NaOH=Na2SiO3+4NaCl+3H2O,
故答案为:CO;SiCl4+6NaOH=Na2SiO3+4NaCl+3H2O;
(3)金属氯化物的沸点均高于150℃,则固体Ⅲ中存在AlCl3、FeCl3、MgCl2,其中FeCl3、MgCl2与过量的氢氧化钠溶液反应得到沉淀,而氯化铝与过量的氢氧化钠溶液反应生成偏铝酸钠,搅拌、过滤得到溶液IV,故溶液IV中的阴离子有:AlO2-、OH-、Cl-,
故答案为:过滤;AlO2-、OH-、Cl-;
(4)偏铝酸钠发生水解,加入乙酸乙酯除去过量的氢氧化钠,且加热条件下水解平衡一直正向移动,得到氢氧化铝沉淀、醋酸钠、乙醇,由溶液IV生成沉淀V的总反应的离子方程式为AlO2-+CH3COOCH2CH3+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CH3COO-+CH3CH2OH+Al(OH)3↓,
Al2O3的质量分数为5.1%,则100kg初级石墨中氧化铝的质量=100kg×5.1%=5.1kg,根据Al元素守恒,可知氢氧化铝的质量为$\frac{5.1kg×\frac{54}{102}}{\frac{27}{78}}$=7.8kg,
故答案为:AlO2-+CH3COOCH2CH3+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CH3COO-+CH3CH2OH+Al(OH)3↓;7.8.
解析
步骤 1:通入氮气的目的
石墨在高温下可与氧气发生反应,通入氮气排尽装置中的空气,防止石墨发生氧化反应,减少石墨损失。
步骤 2:气体I中的碳氧化物
石墨过量高温反应后,石墨中氧化物杂质均转变为相应的氯化物,根据杂质的含量可知,气体I中氯化物主要为SiCl_4、AlCl_3、FeCl_3等,气体I中碳氧化物主要为CO。
步骤 3:气体II中某物得到水玻璃的化学反应方程式
SiCl_4的沸点为57.6℃,金属氯化物的沸点均高于150℃,80℃冷却得到的气体Ⅱ含有SiCl_4及CO,SiCl_4与氢氧化钠溶液反应得到硅酸钠与氯化钠,化学反应方程式为:SiCl_4+6NaOH=Na_2SiO_3+4NaCl+3H_2O。
步骤 4:步骤①的操作及溶液IV中的阴离子
金属氯化物的沸点均高于150℃,则固体Ⅲ中存在AlCl_3、FeCl_3、MgCl_2,其中FeCl_3、MgCl_2与过量的氢氧化钠溶液反应得到沉淀,而氯化铝与过量的氢氧化钠溶液反应生成偏铝酸钠,搅拌、过滤得到溶液IV,故溶液IV中的阴离子有:AlO_2^{-}、OH^{-}、Cl^{-}。
步骤 5:由溶液IV生成沉淀V的总反应的离子方程式
偏铝酸钠发生水解,加入乙酸乙酯除去过量的氢氧化钠,且加热条件下水解平衡一直正向移动,得到氢氧化铝沉淀、醋酸钠、乙醇,由溶液IV生成沉淀V的总反应的离子方程式为AlO_2^{-}+CH_3COOCH_2CH_3+2H_2O$\frac{\underline{\;\;△\;\;}}{\;}$CH_3COO^{-}+CH_3CH_2OH+Al(OH)_3↓。
步骤 6:100kg初级石墨最多可能获得Ⅴ的质量
Al_2O_3的质量分数为5.1%,则100kg初级石墨中氧化铝的质量=100kg×5.1%=5.1kg,根据Al元素守恒,可知氢氧化铝的质量为$\frac{5.1kg×\frac{54}{102}}{\frac{27}{78}}$=7.8kg。
石墨在高温下可与氧气发生反应,通入氮气排尽装置中的空气,防止石墨发生氧化反应,减少石墨损失。
步骤 2:气体I中的碳氧化物
石墨过量高温反应后,石墨中氧化物杂质均转变为相应的氯化物,根据杂质的含量可知,气体I中氯化物主要为SiCl_4、AlCl_3、FeCl_3等,气体I中碳氧化物主要为CO。
步骤 3:气体II中某物得到水玻璃的化学反应方程式
SiCl_4的沸点为57.6℃,金属氯化物的沸点均高于150℃,80℃冷却得到的气体Ⅱ含有SiCl_4及CO,SiCl_4与氢氧化钠溶液反应得到硅酸钠与氯化钠,化学反应方程式为:SiCl_4+6NaOH=Na_2SiO_3+4NaCl+3H_2O。
步骤 4:步骤①的操作及溶液IV中的阴离子
金属氯化物的沸点均高于150℃,则固体Ⅲ中存在AlCl_3、FeCl_3、MgCl_2,其中FeCl_3、MgCl_2与过量的氢氧化钠溶液反应得到沉淀,而氯化铝与过量的氢氧化钠溶液反应生成偏铝酸钠,搅拌、过滤得到溶液IV,故溶液IV中的阴离子有:AlO_2^{-}、OH^{-}、Cl^{-}。
步骤 5:由溶液IV生成沉淀V的总反应的离子方程式
偏铝酸钠发生水解,加入乙酸乙酯除去过量的氢氧化钠,且加热条件下水解平衡一直正向移动,得到氢氧化铝沉淀、醋酸钠、乙醇,由溶液IV生成沉淀V的总反应的离子方程式为AlO_2^{-}+CH_3COOCH_2CH_3+2H_2O$\frac{\underline{\;\;△\;\;}}{\;}$CH_3COO^{-}+CH_3CH_2OH+Al(OH)_3↓。
步骤 6:100kg初级石墨最多可能获得Ⅴ的质量
Al_2O_3的质量分数为5.1%,则100kg初级石墨中氧化铝的质量=100kg×5.1%=5.1kg,根据Al元素守恒,可知氢氧化铝的质量为$\frac{5.1kg×\frac{54}{102}}{\frac{27}{78}}$=7.8kg。