题目
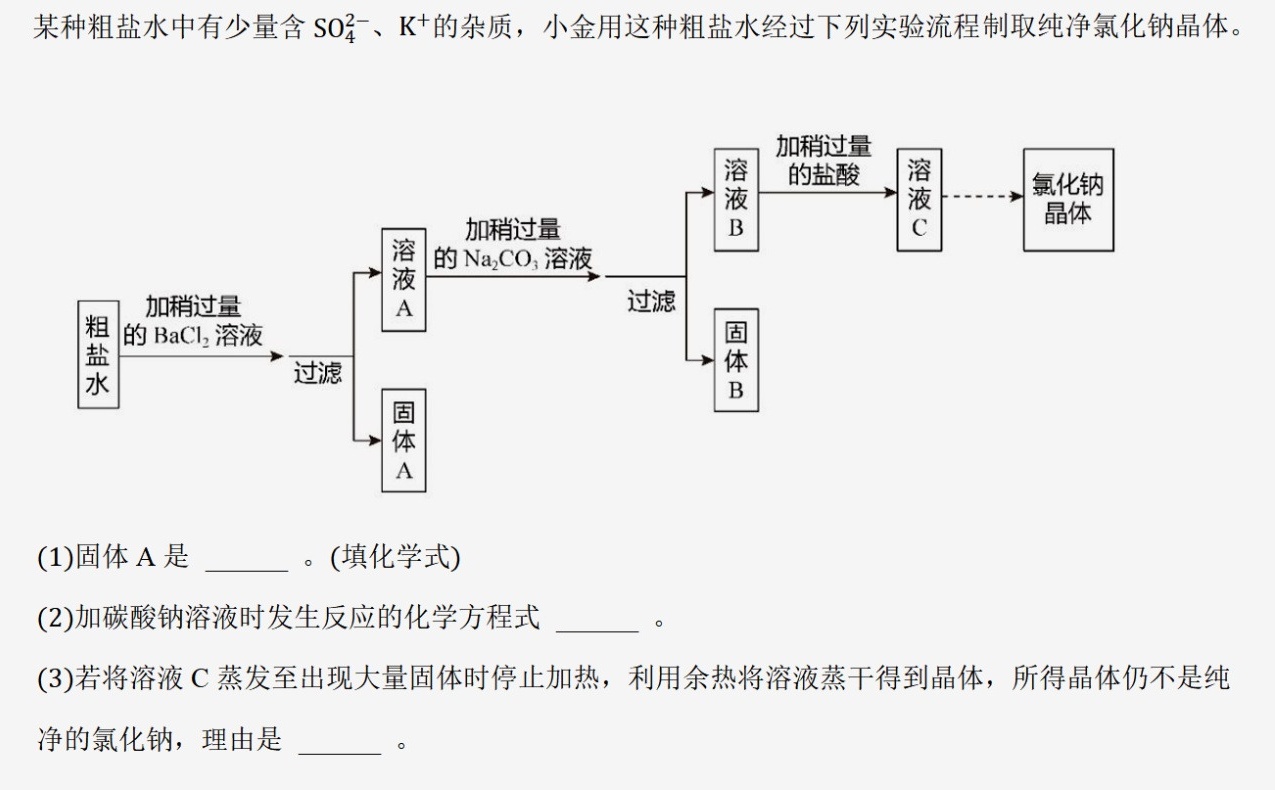
某种粗盐水中有少量含 (S{O)_(4)}^- 、K^+ 的杂质,小金用这种粗盐水经过下列实验流程制取纯净氯化钠晶体。-|||-加稍过量-|||-溶 的Na2CO3溶液-|||-加稍过量 液 的盐酸 液 氯化钠 晶体-|||-加稍过量 A 过滤-|||-盐 的BaCl2溶液 体-|||-过滤-|||-体-|||-(1)固体A是 __ (填化学式)-|||-(2)加碳酸钠溶液时发生反应的化学方程式 __ o-|||-(3)若将溶液C蒸发至出现大量固体时停止加热,利用余热将溶液蒸干得到晶体,所得晶体仍不是纯-|||-净的氯化钠,理由是 __ 。.
题目解答
答案
(1)$rm BaSO_4$
(2)$rm BaCl_2+Na_2CO_3!=!=!= BaCO_3downarrow +2NaCl$
(3)钾离子未除去
.解析
步骤 1:确定固体A的成分
在粗盐水中加入稍过量的BaCl2溶液,BaCl2与${S{O}_{4}}^{2-}$反应生成BaSO4沉淀,因此固体A是BaSO4。
步骤 2:写出加碳酸钠溶液时发生的化学反应方程式
加入稍过量的Na2CO3溶液,Na2CO3与BaCl2反应生成BaCO3沉淀和NaCl,反应方程式为:$rm BaCl_2+Na_2CO_3!=!=!= BaCO_3downarrow +2NaCl$。
步骤 3:分析蒸发至出现大量固体时停止加热的原因
若将溶液C蒸发至出现大量固体时停止加热,利用余热将溶液蒸干得到晶体,所得晶体仍不是纯净的氯化钠,因为钾离子未除去,钾离子会残留在晶体中。
在粗盐水中加入稍过量的BaCl2溶液,BaCl2与${S{O}_{4}}^{2-}$反应生成BaSO4沉淀,因此固体A是BaSO4。
步骤 2:写出加碳酸钠溶液时发生的化学反应方程式
加入稍过量的Na2CO3溶液,Na2CO3与BaCl2反应生成BaCO3沉淀和NaCl,反应方程式为:$rm BaCl_2+Na_2CO_3!=!=!= BaCO_3downarrow +2NaCl$。
步骤 3:分析蒸发至出现大量固体时停止加热的原因
若将溶液C蒸发至出现大量固体时停止加热,利用余热将溶液蒸干得到晶体,所得晶体仍不是纯净的氯化钠,因为钾离子未除去,钾离子会残留在晶体中。