题目
11.计算下列反应的:(1) (Delta )_(t)(H)_(m)^theta (298.15K) ;(2) (Delta )_(r)(U)_(m)^theta (298.15K) 和(3)298.15K选-|||-反应进度为1 mol的体积功。-|||-(H)_(4)(g)+4(Cl)_(2)(g)=!=!= C(Cl)_(4)(l)+4HCl(g)
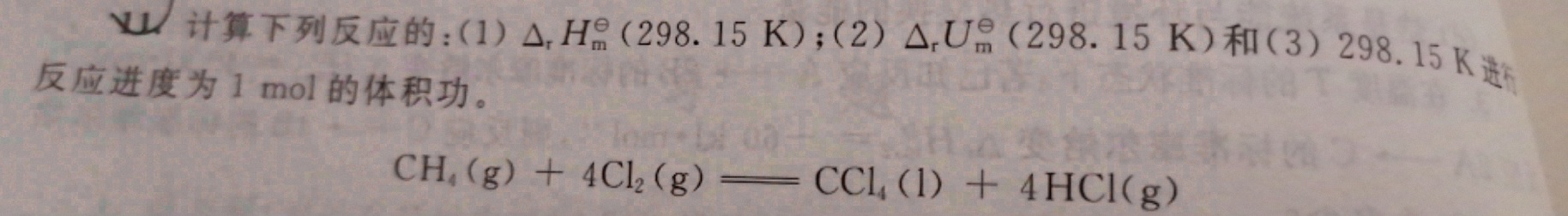
题目解答
答案

解析
步骤 1:计算反应的焓变 ${\Delta }_{r}{H}_{m}^{\theta }(298.15K)$
根据标准生成焓的定义,反应的焓变等于生成物的标准生成焓之和减去反应物的标准生成焓之和。即:
${\Delta }_{r}{H}_{m}^{\theta }(298.15K) = \sum \Delta _{f}H_{m}^{\theta }(\text{生成物}) - \sum \Delta _{f}H_{m}^{\theta }(\text{反应物})$
步骤 2:计算反应的内能变 ${\Delta }_{r}{U}_{m}^{\theta }(298.15K)$
反应的内能变等于反应的焓变减去反应前后气体摩尔数变化乘以理想气体常数和温度的乘积。即:
${\Delta }_{r}{U}_{m}^{\theta }(298.15K) = {\Delta }_{r}{H}_{m}^{\theta }(298.15K) - \Delta nRT$
步骤 3:计算反应进度为1 mol的体积功
体积功等于反应前后气体摩尔数变化乘以理想气体常数和温度的乘积。即:
${W}_{体} = -\Delta nRT$
根据标准生成焓的定义,反应的焓变等于生成物的标准生成焓之和减去反应物的标准生成焓之和。即:
${\Delta }_{r}{H}_{m}^{\theta }(298.15K) = \sum \Delta _{f}H_{m}^{\theta }(\text{生成物}) - \sum \Delta _{f}H_{m}^{\theta }(\text{反应物})$
步骤 2:计算反应的内能变 ${\Delta }_{r}{U}_{m}^{\theta }(298.15K)$
反应的内能变等于反应的焓变减去反应前后气体摩尔数变化乘以理想气体常数和温度的乘积。即:
${\Delta }_{r}{U}_{m}^{\theta }(298.15K) = {\Delta }_{r}{H}_{m}^{\theta }(298.15K) - \Delta nRT$
步骤 3:计算反应进度为1 mol的体积功
体积功等于反应前后气体摩尔数变化乘以理想气体常数和温度的乘积。即:
${W}_{体} = -\Delta nRT$