题目
称取纯碱试样(含NaHCO3及惰性杂质)1.000g溶于水后,以酚酞为指示剂滴至终点,需0.2500mol·L-1HCl20.40ml;再以甲基橙作指示剂继续以HCl滴定,到终点时消耗同浓度HCl28.46ml,求试样中Na2CO3和NaHCO3的质量分数。
称取纯碱试样(含NaHCO3及惰性杂质)1.000g溶于水后,以酚酞为指示剂滴至终点,需0.2500mol·L-1HCl20.40ml;再以甲基橙作指示剂继续以HCl滴定,到终点时消耗同浓度HCl28.46ml,求试样中Na2CO3和NaHCO3的质量分数。
题目解答
答案
解:w(Na2CO3)=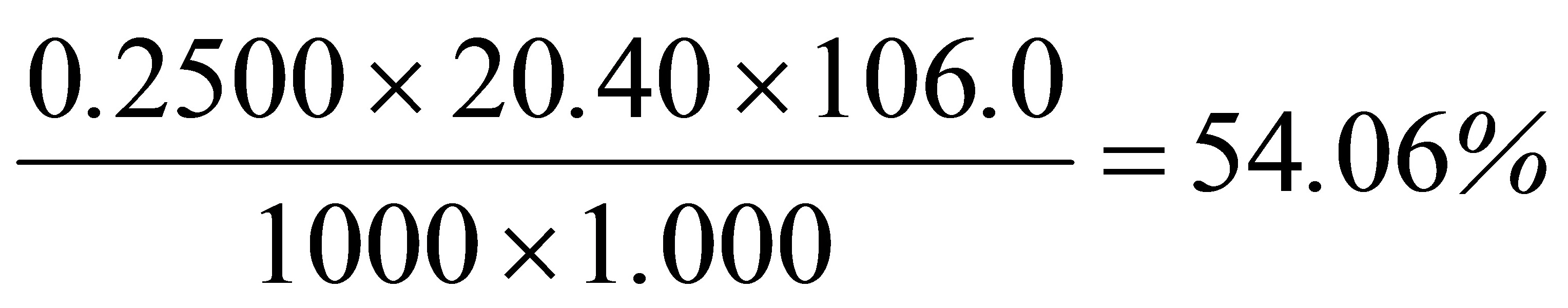
w(NaHCO3)=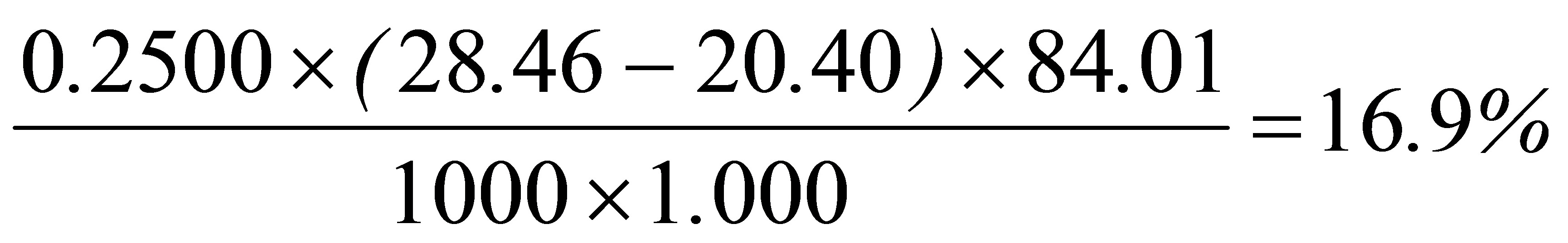
解析
步骤 1:确定反应方程式
Na2CO3与HCl反应的方程式为:Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑
NaHCO3与HCl反应的方程式为:NaHCO3 + HCl → NaCl + H2O + CO2↑
步骤 2:计算Na2CO3的物质的量
以酚酞为指示剂滴定至终点,消耗HCl的物质的量为0.2500 mol/L × 0.02040 L = 0.005100 mol。根据反应方程式,Na2CO3的物质的量为0.005100 mol / 2 = 0.002550 mol。
步骤 3:计算NaHCO3的物质的量
以甲基橙为指示剂继续滴定至终点,消耗HCl的物质的量为0.2500 mol/L × 0.02846 L = 0.007115 mol。根据反应方程式,NaHCO3的物质的量为0.007115 mol - 0.005100 mol = 0.002015 mol。
步骤 4:计算Na2CO3和NaHCO3的质量分数
Na2CO3的质量分数为(0.002550 mol × 106.0 g/mol) / 1.000 g = 54.06%
NaHCO3的质量分数为(0.002015 mol × 84.01 g/mol) / 1.000 g = 16.90%
Na2CO3与HCl反应的方程式为:Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑
NaHCO3与HCl反应的方程式为:NaHCO3 + HCl → NaCl + H2O + CO2↑
步骤 2:计算Na2CO3的物质的量
以酚酞为指示剂滴定至终点,消耗HCl的物质的量为0.2500 mol/L × 0.02040 L = 0.005100 mol。根据反应方程式,Na2CO3的物质的量为0.005100 mol / 2 = 0.002550 mol。
步骤 3:计算NaHCO3的物质的量
以甲基橙为指示剂继续滴定至终点,消耗HCl的物质的量为0.2500 mol/L × 0.02846 L = 0.007115 mol。根据反应方程式,NaHCO3的物质的量为0.007115 mol - 0.005100 mol = 0.002015 mol。
步骤 4:计算Na2CO3和NaHCO3的质量分数
Na2CO3的质量分数为(0.002550 mol × 106.0 g/mol) / 1.000 g = 54.06%
NaHCO3的质量分数为(0.002015 mol × 84.01 g/mol) / 1.000 g = 16.90%