题目
称取Na2CO3和NaHCO3的混合试样0.3010g,溶于适量水中,用酚酞为指示剂,用0.1060 mol/L HCl滴定至终点时,消耗HC溶液20.10mL;继续用甲基橙为指示剂,再用上述HCl溶液滴定至终点,共消耗HCl 47.70mL。计算试样中Na2CO3和NaHCO3的质量分数。[M(Na2CO3)=105.99g·mol-1;M(NaHCO3)=84.01 g·mol-1]
称取Na2CO3和NaHCO3的混合试样0.3010g,溶于适量水中,用酚酞为指示剂,用0.1060 mol/L HCl滴定至终点时,消耗HC溶液20.10mL;继续用甲基橙为指示剂,再用上述HCl溶液滴定至终点,共消耗HCl 47.70mL。计算试样中Na2CO3和NaHCO3的质量分数。[M(Na2CO3)=105.99g·mol-1;M(NaHCO3)=84.01 g·mol-1]
题目解答
答案
解:V1=20.10mL,V2=47.70-20.10=27.60mL
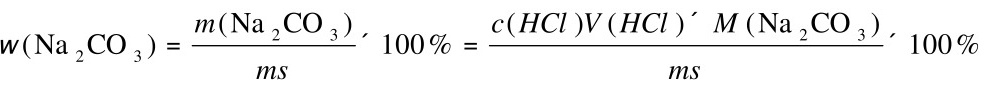
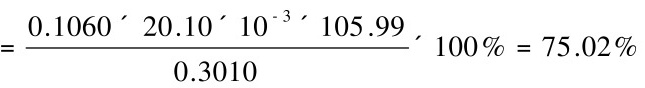
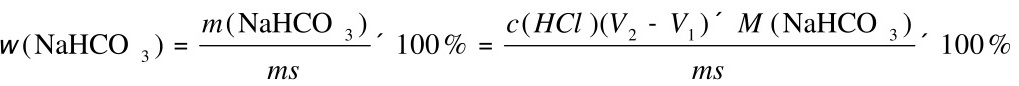
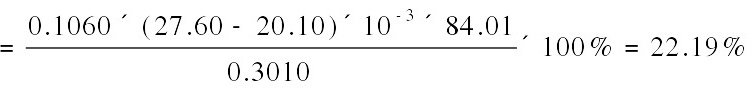
解析
步骤 1:确定滴定反应
在使用酚酞作为指示剂时,Na2CO3与HCl反应生成NaHCO3和NaCl。反应方程式为:
\[ \text{Na}_2\text{CO}_3 + \text{HCl} \rightarrow \text{NaHCO}_3 + \text{NaCl} \]
步骤 2:计算Na2CO3的摩尔数
根据滴定消耗的HCl体积和浓度,可以计算出Na2CO3的摩尔数。消耗的HCl体积为20.10mL,浓度为0.1060 mol/L,因此Na2CO3的摩尔数为:
\[ n(\text{Na}_2\text{CO}_3) = 0.1060 \times 20.10 \times 10^{-3} \]
步骤 3:计算Na2CO3的质量分数
根据Na2CO3的摩尔数和摩尔质量,可以计算出Na2CO3的质量,进而计算出质量分数。Na2CO3的摩尔质量为105.99 g/mol,因此Na2CO3的质量分数为:
\[ \omega(\text{Na}_2\text{CO}_3) = \frac{n(\text{Na}_2\text{CO}_3) \times M(\text{Na}_2\text{CO}_3)}{m_{\text{试样}}} \times 100\% \]
步骤 4:计算NaHCO3的摩尔数
在使用甲基橙作为指示剂时,NaHCO3与HCl反应生成CO2和NaCl。反应方程式为:
\[ \text{NaHCO}_3 + \text{HCl} \rightarrow \text{CO}_2 + \text{NaCl} + \text{H}_2\text{O} \]
根据滴定消耗的HCl体积和浓度,可以计算出NaHCO3的摩尔数。消耗的HCl体积为47.70mL - 20.10mL = 27.60mL,浓度为0.1060 mol/L,因此NaHCO3的摩尔数为:
\[ n(\text{NaHCO}_3) = 0.1060 \times 27.60 \times 10^{-3} \]
步骤 5:计算NaHCO3的质量分数
根据NaHCO3的摩尔数和摩尔质量,可以计算出NaHCO3的质量,进而计算出质量分数。NaHCO3的摩尔质量为84.01 g/mol,因此NaHCO3的质量分数为:
\[ \omega(\text{NaHCO}_3) = \frac{n(\text{NaHCO}_3) \times M(\text{NaHCO}_3)}{m_{\text{试样}}} \times 100\% \]
在使用酚酞作为指示剂时,Na2CO3与HCl反应生成NaHCO3和NaCl。反应方程式为:
\[ \text{Na}_2\text{CO}_3 + \text{HCl} \rightarrow \text{NaHCO}_3 + \text{NaCl} \]
步骤 2:计算Na2CO3的摩尔数
根据滴定消耗的HCl体积和浓度,可以计算出Na2CO3的摩尔数。消耗的HCl体积为20.10mL,浓度为0.1060 mol/L,因此Na2CO3的摩尔数为:
\[ n(\text{Na}_2\text{CO}_3) = 0.1060 \times 20.10 \times 10^{-3} \]
步骤 3:计算Na2CO3的质量分数
根据Na2CO3的摩尔数和摩尔质量,可以计算出Na2CO3的质量,进而计算出质量分数。Na2CO3的摩尔质量为105.99 g/mol,因此Na2CO3的质量分数为:
\[ \omega(\text{Na}_2\text{CO}_3) = \frac{n(\text{Na}_2\text{CO}_3) \times M(\text{Na}_2\text{CO}_3)}{m_{\text{试样}}} \times 100\% \]
步骤 4:计算NaHCO3的摩尔数
在使用甲基橙作为指示剂时,NaHCO3与HCl反应生成CO2和NaCl。反应方程式为:
\[ \text{NaHCO}_3 + \text{HCl} \rightarrow \text{CO}_2 + \text{NaCl} + \text{H}_2\text{O} \]
根据滴定消耗的HCl体积和浓度,可以计算出NaHCO3的摩尔数。消耗的HCl体积为47.70mL - 20.10mL = 27.60mL,浓度为0.1060 mol/L,因此NaHCO3的摩尔数为:
\[ n(\text{NaHCO}_3) = 0.1060 \times 27.60 \times 10^{-3} \]
步骤 5:计算NaHCO3的质量分数
根据NaHCO3的摩尔数和摩尔质量,可以计算出NaHCO3的质量,进而计算出质量分数。NaHCO3的摩尔质量为84.01 g/mol,因此NaHCO3的质量分数为:
\[ \omega(\text{NaHCO}_3) = \frac{n(\text{NaHCO}_3) \times M(\text{NaHCO}_3)}{m_{\text{试样}}} \times 100\% \]