题目
答案:C解析:解:A.离子化合物中可能含有共价键,如KOH、A.等,故A错误; B.构成单质分子的粒子中不一定含有共价键,如稀有气体中不存在化学键,故B错误; C.只含共价键的化合物是共价化合物,所以共价化合物中只含共价键,故C正确; D.仅由非金属元素组成的化合物中可能含有离子键,如铵盐,故D错误; 故选C. A.离子化合物中可能含有共价键; B.构成单质分子的粒子中不一定含有共价键; C.共价化合物中只含共价键; D.仅由非金属元素组成的化合物中可能含有离子键. 本题考查了物质和化学键的关系,不能根据是否含有金属元素判断离子键,如D选项,稀有气体分子是单原子分子,不存在化学键,为易错点. 6.答案:B解析:A. 离子键本质是阴、阳离子间的静电作用; B. 共价化合物中原子之间通过共用电子对形成化学键; C. 离子晶体中一个阳离子周围存在多个阴离子; D. 金属元素和非金属元素可能形成共价键。 本题考查了化学键,题目难度不大,注意把握共价键和离子键的含义及区别,侧重于考查学生对基础知识的应用能力。 解:A.离子键本质是阴、阳离子间的静电作用,不只是引力,还有斥力,故A错误; B.共价化合物中原子之间通过共用电子对形成化学键,所以共价化合物中只含有共价键,故B正确; C.离子晶体中一个阳离子周围存在多个阴离子,所以一个阳离子可与多个阴离子之间存在离子键,故C错误; D.金属元素和非金属元素可能形成共价键,如氯化铝是由金属元素和非金属元素化合形成的共价化合物,只含有共价键,故D错误。 故选B。 7.答案:A E. 离子化合物的构成微粒为离子 F. 单质分子中可能不存在化学键,如稀有气体单质,多原子构成的单质含化学键,故B错误; G. 氯化铝是由金属元素和非金属元素形成的共价化合物,所以含活泼金属元素的化合物可能是共价化合物,故C错误; 离子化合物中可能含共价键,如NaOH为离子化合物含共价键,故D错误; 故选:A。 A.离子化合物的构成微粒为离子; B.单质分子中可能不存在化学键; C.氯化铝是由金属元素和非金属元素形成的共价化合物; D.离子化合物中可能含共价键. 本题考查化学键与化合物的分类,把握化学键的形成及判断的一般规律为解答的关键,侧重常见物质中化学键的考查,注意利用实例分析,题目难度不大. 8.答案:D 正确; 化学键可以是原子之间的作用力,如共价化合物和多原子分子的单质等,也可以是离子之间的作用力,如离子晶体中阴阳离子之间的作用力,故B正确; 化学键存在于分子内,存在于相邻原子之间,故C正确; 分子之间的作用力是范德华力,不是化学键,故D错误; 故选D. 化学键是相邻原子或离子之间强烈的相互作用,化学键是一种作用力,离子键和共价键、金属键都属于化学键. 本题考查了化学键的判断,明确化学键的概念是解本题关键,注意化学键中的几个关键词“相邻”、“强烈的相互作用”,题目难度不大. 9.答案:B 解析: b、c、d、e、f、 g依次是钠、镁、铝、硅、磷、硫、氯,形成离子键的是活泼金属A.如钠、镁A.和活泼非金属A.如硫、氯A.之间的化合,故 正确。 故选B。 10.答案:B 解析: 族和第ⅦA族原子化合时,不一定生成离子键,可能生成共价键,如H元素和F元素能形成共价化合物HF,故错误; A.由非金属元素形成的化合物可能是离子化合物,如铵盐,故错误; A.活泼金属与非金属化合时,能形成离子键,如第IA族A.除外A.、第IIA族元素和第VIA族、第VIIA族元素易形成离子键,故正确; A.含有离子键的化合物一定是离子化合物,离子化合物中可能含有共价键,如KOH,故正确; A.离子化合物中可能同时含有离子键和共价键,如NaOH,故正确。 故选 。 11.答案:C 阴、阳离子通过静电作用所形成的化学键是离子键; 氯化铵只由非金属元素组成是离子化合物,故B错误; 氯化铝是金属元素与非金属元素化合时,是共价化合物,所以不一定形成离子键,故C正确; 活泼金属与活泼非金属之间能形成离子键,铵根离子与酸根离也能形成离子键,故D错误; 故选C. A.阴、阳离子通过静电作用所形成的化学键是离子键; B、氯化铵是离子化合物; C、氯化铝是金属元素与非金属元素化合时,是共价化合物; D、铵根离子与酸根离也能形成离子键; 本题主要考查化学键的概念与化合物的关系,题目难度不大,注意离子键和共价键与化合物的关系是解题的关键. 12.答案:B 不选; A.中只含C、O之间的极性共价键,为共价化合物,故B选; HCl中只含共价键,为共价化合物,故C不选; NaOH中含离子键和A.极性共价键,为离子化合物,故D不选; 故选B. 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,含离子键的一定为离子化合物,以此来解答. 本题考查化学键,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大. 13.答案:D 解析: 本题考查了离子键、共价键的判断及用电子式书写化合物的性质过程,明确化合物中存在的化学键是解本题关键,难点是用电子式表示化合物的形成过程,注意把握书写方法。 共价键的形成为共用电子对,没有电子的得失,不能有箭头,故A错误; 硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物,形成过程为:A.,故B错误; 生成物氯离子不能合并,故C错误; 氟画面为离子化合物,形成过程为:A. ;故D正确。 。
答案:C
解析:解: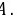 离子化合物中可能含有共价键,如KOH、
离子化合物中可能含有共价键,如KOH、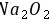 等,故A错误; B.构成单质分子的粒子中不一定含有共价键,如稀有气体中不存在化学键,故B错误; C.只含共价键的化合物是共价化合物,所以共价化合物中只含共价键,故C正确; D.仅由非金属元素组成的化合物中可能含有离子键,如铵盐,故D错误; 故选C. A.离子化合物中可能含有共价键; B.构成单质分子的粒子中不一定含有共价键; C.共价化合物中只含共价键; D.仅由非金属元素组成的化合物中可能含有离子键. 本题考查了物质和化学键的关系,不能根据是否含有金属元素判断离子键,如D选项,稀有气体分子是单原子分子,不存在化学键,为易错点. 6.答案:B
等,故A错误; B.构成单质分子的粒子中不一定含有共价键,如稀有气体中不存在化学键,故B错误; C.只含共价键的化合物是共价化合物,所以共价化合物中只含共价键,故C正确; D.仅由非金属元素组成的化合物中可能含有离子键,如铵盐,故D错误; 故选C. A.离子化合物中可能含有共价键; B.构成单质分子的粒子中不一定含有共价键; C.共价化合物中只含共价键; D.仅由非金属元素组成的化合物中可能含有离子键. 本题考查了物质和化学键的关系,不能根据是否含有金属元素判断离子键,如D选项,稀有气体分子是单原子分子,不存在化学键,为易错点. 6.答案:B
解析:
A. 离子键本质是阴、阳离子间的静电作用;B. 共价化合物中原子之间通过共用电子对形成化学键;
C. 离子晶体中一个阳离子周围存在多个阴离子;
D. 金属元素和非金属元素可能形成共价键。 本题考查了化学键,题目难度不大,注意把握共价键和离子键的含义及区别,侧重于考查学生对基础知识的应用能力。 解:
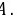 离子键本质是阴、阳离子间的静电作用,不只是引力,还有斥力,故A错误; B.共价化合物中原子之间通过共用电子对形成化学键,所以共价化合物中只含有共价键,故B正确; C.离子晶体中一个阳离子周围存在多个阴离子,所以一个阳离子可与多个阴离子之间存在离子键,故C错误; D.金属元素和非金属元素可能形成共价键,如氯化铝是由金属元素和非金属元素化合形成的共价化合物,只含有共价键,故D错误。 故选B。 7.答案:A
离子键本质是阴、阳离子间的静电作用,不只是引力,还有斥力,故A错误; B.共价化合物中原子之间通过共用电子对形成化学键,所以共价化合物中只含有共价键,故B正确; C.离子晶体中一个阳离子周围存在多个阴离子,所以一个阳离子可与多个阴离子之间存在离子键,故C错误; D.金属元素和非金属元素可能形成共价键,如氯化铝是由金属元素和非金属元素化合形成的共价化合物,只含有共价键,故D错误。 故选B。 7.答案:AE. 离子化合物的构成微粒为离子
F. 单质分子中可能不存在化学键,如稀有气体单质,多原子构成的单质含化学键,故B错误;
G. 氯化铝是由金属元素和非金属元素形成的共价化合物,所以含活泼金属元素的化合物可能是共价化合物,故C错误;
离子化合物中可能含共价键,如NaOH为离子化合物含共价键,故D错误; 故选:A。 A.离子化合物的构成微粒为离子; B.单质分子中可能不存在化学键; C.氯化铝是由金属元素和非金属元素形成的共价化合物; D.离子化合物中可能含共价键. 本题考查化学键与化合物的分类,把握化学键的形成及判断的一般规律为解答的关键,侧重常见物质中化学键的考查,注意利用实例分析,题目难度不大. 8.答案:D
正确;
化学键可以是原子之间的作用力,如共价化合物和多原子分子的单质等,也可以是离子之间的作用力,如离子晶体中阴阳离子之间的作用力,故B正确;
化学键存在于分子内,存在于相邻原子之间,故C正确;
分子之间的作用力是范德华力,不是化学键,故D错误; 故选D. 化学键是相邻原子或离子之间强烈的相互作用,化学键是一种作用力,离子键和共价键、金属键都属于化学键. 本题考查了化学键的判断,明确化学键的概念是解本题关键,注意化学键中的几个关键词“相邻”、“强烈的相互作用”,题目难度不大. 9.答案:B
解析:
b、c、d、e、f、 g依次是钠、镁、铝、硅、磷、硫、氯,形成离子键的是活泼金属
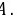 如钠、镁
如钠、镁 和活泼非金属
和活泼非金属 如硫、氯
如硫、氯 之间的化合,故
之间的化合,故正确。 故选B。 10.答案:B
解析:
族和第ⅦA族原子化合时,不一定生成离子键,可能生成共价键,如H元素和F元素能形成共价化合物HF,故错误;
 由非金属元素形成的化合物可能是离子化合物,如铵盐,故错误;
由非金属元素形成的化合物可能是离子化合物,如铵盐,故错误;  活泼金属与非金属化合时,能形成离子键,如第IA族
活泼金属与非金属化合时,能形成离子键,如第IA族 除外
除外 、第IIA族元素和第VIA族、第VIIA族元素易形成离子键,故正确;
、第IIA族元素和第VIA族、第VIIA族元素易形成离子键,故正确;  含有离子键的化合物一定是离子化合物,离子化合物中可能含有共价键,如KOH,故正确;
含有离子键的化合物一定是离子化合物,离子化合物中可能含有共价键,如KOH,故正确;  离子化合物中可能同时含有离子键和共价键,如NaOH,故正确。 故选
离子化合物中可能同时含有离子键和共价键,如NaOH,故正确。 故选。 11.答案:C
阴、阳离子通过静电作用所形成的化学键是离子键;
氯化铵只由非金属元素组成是离子化合物,故B错误;
氯化铝是金属元素与非金属元素化合时,是共价化合物,所以不一定形成离子键,故C正确;
活泼金属与活泼非金属之间能形成离子键,铵根离子与酸根离也能形成离子键,故D错误; 故选C. A.阴、阳离子通过静电作用所形成的化学键是离子键; B、氯化铵是离子化合物; C、氯化铝是金属元素与非金属元素化合时,是共价化合物; D、铵根离子与酸根离也能形成离子键; 本题主要考查化学键的概念与化合物的关系,题目难度不大,注意离子键和共价键与化合物的关系是解题的关键. 12.答案:B
不选;
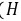 中只含C、O之间的极性共价键,为共价化合物,故B选;
中只含C、O之间的极性共价键,为共价化合物,故B选;HCl中只含共价键,为共价化合物,故C不选;
NaOH中含离子键和
 极性共价键,为离子化合物,故D不选; 故选B. 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,含离子键的一定为离子化合物,以此来解答. 本题考查化学键,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大. 13.答案:D
极性共价键,为离子化合物,故D不选; 故选B. 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,含离子键的一定为离子化合物,以此来解答. 本题考查化学键,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大. 13.答案:D解析:
本题考查了离子键、共价键的判断及用电子式书写化合物的性质过程,明确化合物中存在的化学键是解本题关键,难点是用电子式表示化合物的形成过程,注意把握书写方法。
共价键的形成为共用电子对,没有电子的得失,不能有箭头,故A错误;
硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物,形成过程为:
 ,故B错误;
,故B错误; 生成物氯离子不能合并,故C错误;
氟画面为离子化合物,形成过程为:
 ;故D正确。
;故D正确。。
题目解答
答案
7. 答案: 解析: 8. 答案: 解析: 9. 答案: 解析: 10. 答案: 解析: 11. 答案: 解析: 12. 答案: 解析: 13. 答案: 解析: