在273 K 和293 K时,固体苯的蒸气压分别为3.27 kPa和12.30kPa,液体苯在293 K时的蒸气压为10.02 kPa。液体苯的摩尔汽化热为34.17 cdot (mol)^-1。 试求:(1) 303 K时液体苯的蒸气压;(2) 固体苯的摩尔升华焓;(3) 固体苯的摩尔熔化热。
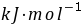 。 试求:(1) 303 K时液体苯的蒸气压;(2) 固体苯的摩尔升华焓;(3) 固体苯的摩尔熔化热。
。 试求:(1) 303 K时液体苯的蒸气压;(2) 固体苯的摩尔升华焓;(3) 固体苯的摩尔熔化热。题目解答
答案
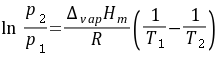
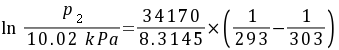
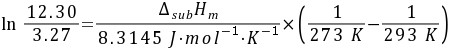
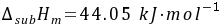
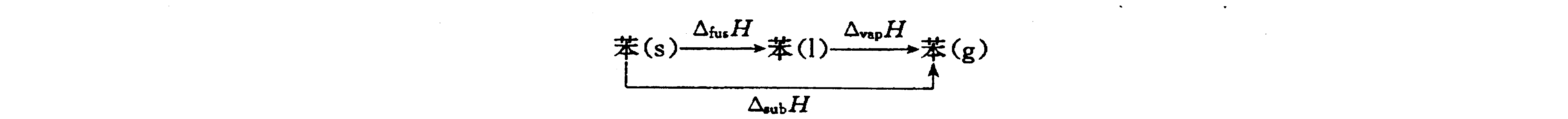
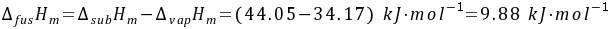
解析
考查要点:本题主要考查克劳修斯-克拉佩龙方程的应用,以及相变焓之间的关系。
解题思路:
- 液体苯蒸气压的计算:利用克劳修斯-克拉佩龙方程,结合已知的汽化热和温度-蒸气压数据,外推303 K时的蒸气压。
- 升华焓的计算:对固态苯的两个温度-蒸气压数据应用克劳修斯-克拉佩龙方程,求解升华焓。
- 熔化热的计算:通过升华焓与汽化热的关系($\Delta_{\text{sub}}H_m = \Delta_{\text{fus}}H_m + \Delta_{\text{vap}}H_m$),间接求解熔化热。
关键点:
- 克劳修斯-克拉佩龙方程的正确应用,注意单位统一(温度用开尔文,焓用焦耳)。
- 相变焓的关系:升华焓是熔化热与汽化热之和。
(1) 液体苯在303 K时的蒸气压
克劳修斯-克拉佩龙方程:
$\ln \frac{p_2}{p_1} = \frac{\Delta H_{\text{vap}}}{R} \left( \frac{1}{T_1} - \frac{1}{T_2} \right)$
代入数据:
- $p_1 = 10.02 \, \text{kPa}$,$T_1 = 293 \, \text{K}$
- $T_2 = 303 \, \text{K}$,$\Delta H_{\text{vap}} = 34.17 \, \text{kJ/mol} = 34170 \, \text{J/mol}$
- $R = 8.3145 \, \text{J/mol·K}$
计算得:
$\ln \frac{p_2}{10.02} = \frac{34170}{8.3145} \left( \frac{1}{293} - \frac{1}{303} \right) \approx 0.460$
解得:
$p_2 = 10.02 \cdot e^{0.460} \approx 15.92 \, \text{kPa}$
(2) 固体苯的摩尔升华焓
克劳修斯-克拉佩龙方程:
$\ln \frac{p_2}{p_1} = \frac{\Delta H_{\text{sub}}}{R} \left( \frac{1}{T_1} - \frac{1}{T_2} \right)$
代入数据:
- $p_1 = 3.27 \, \text{kPa}$,$T_1 = 273 \, \text{K}$
- $p_2 = 12.30 \, \text{kPa}$,$T_2 = 293 \, \text{K}$
计算得:
$\ln \frac{12.30}{3.27} = \frac{\Delta H_{\text{sub}}}{8.3145} \left( \frac{1}{273} - \frac{1}{293} \right)$
解得:
$\Delta H_{\text{sub}} \approx 44.05 \, \text{kJ/mol}$
(3) 固体苯的摩尔熔化热
相变焓关系:
$\Delta H_{\text{sub}} = \Delta H_{\text{fus}} + \Delta H_{\text{vap}}$
代入已知数据:
$\Delta H_{\text{fus}} = \Delta H_{\text{sub}} - \Delta H_{\text{vap}} = 44.05 \, \text{kJ/mol} - 34.17 \, \text{kJ/mol} = 9.88 \, \text{kJ/mol}$