题目
例 11-1 讨论 ([ Fe{({H)_(2)O)}_(6)] }^3+ 的中心离子的杂化方式和配位单元中的成键情况。
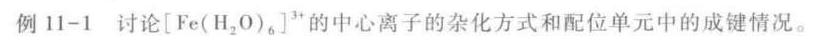
题目解答
答案
解析
步骤 1:确定中心离子的电子构型
Fe 的电子构型为 3d^6 4s^2。在形成 ${[ Fe{({H}_{2}O)}_{6}] }^{3+}$ 过程中,Fe 失去三个电子,形成 ${Fe}^{3+}$,其电子构型为 3d^5。
步骤 2:确定中心离子的杂化方式
${Fe}^{3+}$ 的 3d^5 电子构型表明,它需要进行杂化以形成配位键。由于 ${[ Fe{({H}_{2}O)}_{6}] }^{3+}$ 是一个八面体配位单元,中心离子需要进行 sp^3d^2 杂化,以形成 6 个配位键。
步骤 3:确定配位单元的成键情况
由于中心离子进行 sp^3d^2 杂化,其杂化轨道在空间呈八面体分布。6 个配体 H2O 的孤电子对配入其中形成 6 个配位键,故 ${[ Fe{({H}_{2}O)}_{6}] }^{3+}$ 形成八面体构型的配位单元。由于配体的电子对配入中心的外层空轨道,即 nsnpnd 杂化轨道,形成外轨型配位化合物,所成的配位键称为电价配键。电价配键较弱。
Fe 的电子构型为 3d^6 4s^2。在形成 ${[ Fe{({H}_{2}O)}_{6}] }^{3+}$ 过程中,Fe 失去三个电子,形成 ${Fe}^{3+}$,其电子构型为 3d^5。
步骤 2:确定中心离子的杂化方式
${Fe}^{3+}$ 的 3d^5 电子构型表明,它需要进行杂化以形成配位键。由于 ${[ Fe{({H}_{2}O)}_{6}] }^{3+}$ 是一个八面体配位单元,中心离子需要进行 sp^3d^2 杂化,以形成 6 个配位键。
步骤 3:确定配位单元的成键情况
由于中心离子进行 sp^3d^2 杂化,其杂化轨道在空间呈八面体分布。6 个配体 H2O 的孤电子对配入其中形成 6 个配位键,故 ${[ Fe{({H}_{2}O)}_{6}] }^{3+}$ 形成八面体构型的配位单元。由于配体的电子对配入中心的外层空轨道,即 nsnpnd 杂化轨道,形成外轨型配位化合物,所成的配位键称为电价配键。电价配键较弱。