题目
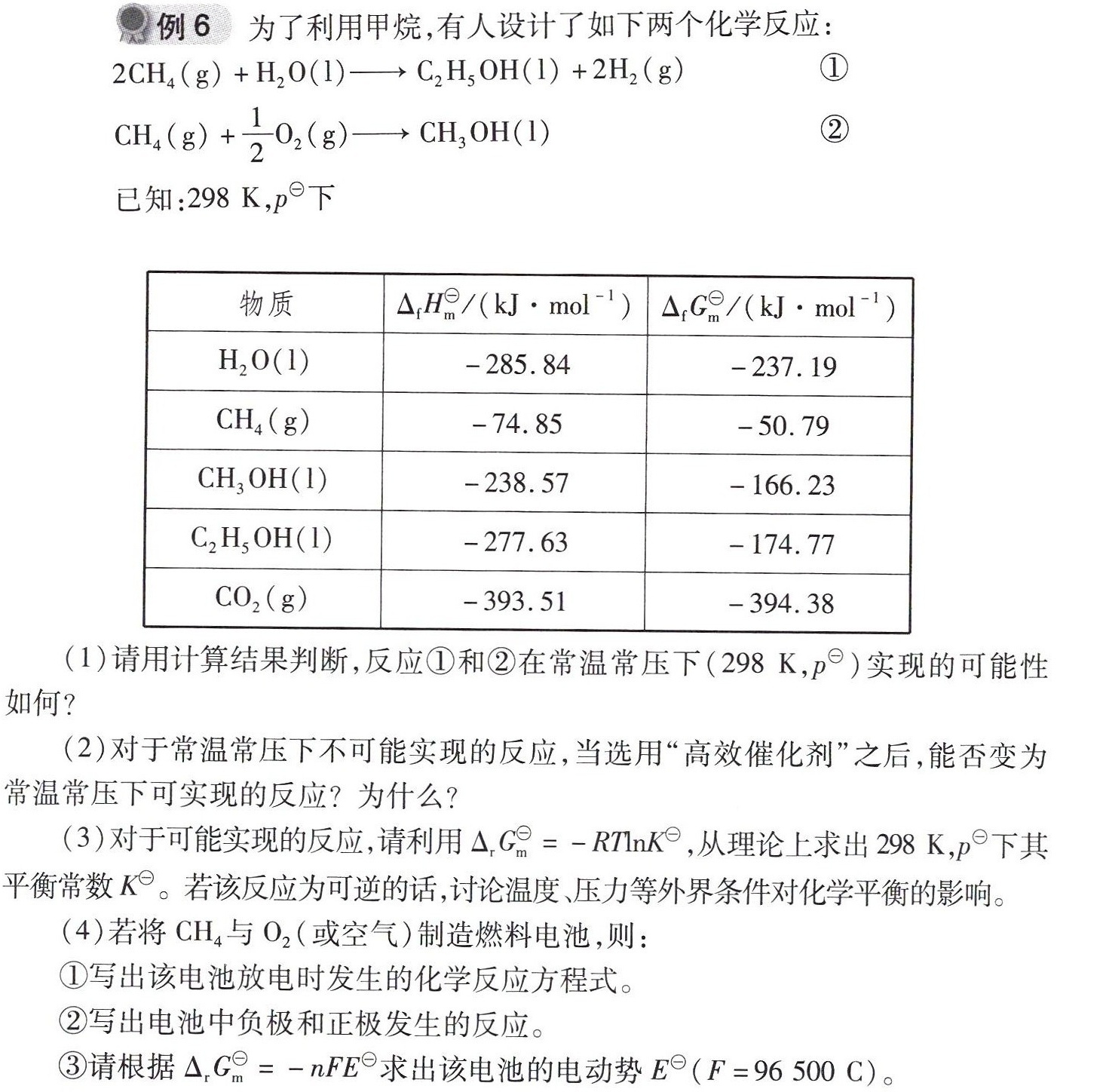
例6 为了利用甲烷,有人设计了如下两个化学反应:-|||-(H)_(4)(g)+(H)_(2)O(l)arrow (C)_(2)(H)_(5)OH(l)+2(H)_(2)(g) ①-|||-(H)_(4)(g)+dfrac (1)(2)(O)_(2)(g)arrow C(H)_(3)OH(1) ②-|||-已知:298K,p^哪下-|||-物质 (Delta )_(1)(H)_(m)/(kJcdot mo(l)^-1) (Delta )_(1)(G)_(m)/(kJcdot mo(l)^-1)-|||-H2O(1) -285.84 -237.19-|||-CH4(g) -74.85 -50.79-|||-CH3OH(1) -238.57 -166.23-|||-C2H5OH(1 ) -277.63 -174.77-|||-CO2(g) -393.51 -394.38-|||-(1)请用计算结果判断,反应①和②在常温常压下(298K,p = )实现的可能性-|||-如何?-|||-(2)对于常温常压下不可能实现的反应,当选用"高效催化剂"之后,能否变为-|||-常温常压下可实现的反应?为什么?-|||-(3)对于可能实现的反应,请利用 (Delta )_(r)(C)_(m)^circled (-)(R)_(m)=-RTln (K)^circled (-), 从理论上求出298K,p⊆下其-|||-平衡常数K^0。若该反应为可逆的话,讨论温度、压力等外界条件对化学平衡的影响。-|||-(4)若将CH4与O2(或空气)制造燃料电池,则:-|||-①写出该电池放电时发生的化学反应方程式。-|||-②写出电池中负极和正极发生的反应。-|||-③请根据 (Delta )_(r)(G)_(m)=-n(FE)^theta 求出该电池的电动势 (F=96500c)
题目解答
答案

解析
步骤 1:计算反应①的焓变和熵变
根据已知数据,计算反应①的焓变和熵变。
步骤 2:计算反应②的焓变和熵变
根据已知数据,计算反应②的焓变和熵变。
步骤 3:判断反应①和②在常温常压下的可能性
根据计算出的焓变和熵变,判断反应①和②在常温常压下的可能性。
步骤 4:讨论催化剂对反应①和②的影响
讨论催化剂对反应①和②的影响。
步骤 5:计算反应②的平衡常数
利用 ${\Delta }_{r}{G}_{m}^{\theta }=-R{m}^{\theta }$ 计算反应②的平衡常数。
步骤 6:讨论温度、压力等外界条件对化学平衡的影响
讨论温度、压力等外界条件对化学平衡的影响。
步骤 7:写出燃料电池的化学反应方程式
写出燃料电池的化学反应方程式。
步骤 8:写出电池中负极和正极发生的反应
写出电池中负极和正极发生的反应。
步骤 9:计算电池的电动势
利用 ${\Delta }_{r}{G}_{m}^{\theta }=-nFE\theta $ 计算电池的电动势。
根据已知数据,计算反应①的焓变和熵变。
步骤 2:计算反应②的焓变和熵变
根据已知数据,计算反应②的焓变和熵变。
步骤 3:判断反应①和②在常温常压下的可能性
根据计算出的焓变和熵变,判断反应①和②在常温常压下的可能性。
步骤 4:讨论催化剂对反应①和②的影响
讨论催化剂对反应①和②的影响。
步骤 5:计算反应②的平衡常数
利用 ${\Delta }_{r}{G}_{m}^{\theta }=-R{m}^{\theta }$ 计算反应②的平衡常数。
步骤 6:讨论温度、压力等外界条件对化学平衡的影响
讨论温度、压力等外界条件对化学平衡的影响。
步骤 7:写出燃料电池的化学反应方程式
写出燃料电池的化学反应方程式。
步骤 8:写出电池中负极和正极发生的反应
写出电池中负极和正极发生的反应。
步骤 9:计算电池的电动势
利用 ${\Delta }_{r}{G}_{m}^{\theta }=-nFE\theta $ 计算电池的电动势。