磷酸氯喹是一种抗疟疾药物, 研究发现,该药在细胞水平上能有效抑制新型冠状病毒的感染。其合成路线如下:a ^9(H)_(3) H^9-|||-N .to vord NIO^9H^95 20NIO^+H^9-|||-.0. (H2^2HOO)H2 lOH^-ad o to ad a B v-|||-ō HO t(H2)^2H2^(200))a ^9(H)_(3) H^9-|||-N .to vord NIO^9H^95 20NIO^+H^9-|||-.0. (H2^2HOO)H2 lOH^-ad o to ad a B v-|||-ō HO t(H2)^2H2^(200))已知:a ^9(H)_(3) H^9-|||-N .to vord NIO^9H^95 20NIO^+H^9-|||-.0. (H2^2HOO)H2 lOH^-ad o to ad a B v-|||-ō HO t(H2)^2H2^(200))回答下列问题:(1)A是一种芳香经, B 中官能团的名称为__________________。(2)反应 A→B 中须加入的试剂a 为___________________。2.熟悉常见试剂的保存a ^9(H)_(3) H^9-|||-N .to vord NIO^9H^95 20NIO^+H^9-|||-.0. (H2^2HOO)H2 lOH^-ad o to ad a B v-|||-ō HO t(H2)^2H2^(200))a ^9(H)_(3) H^9-|||-N .to vord NIO^9H^95 20NIO^+H^9-|||-.0. (H2^2HOO)H2 lOH^-ad o to ad a B v-|||-ō HO t(H2)^2H2^(200))3.基本实验操作中应注意的问题归纳(1)酸式滴定管不能装碱性溶液,碱式滴定管不能装酸性及氧化性溶液。(2)容量瓶不能长期存放溶液,更不能作为反应容器,也不可加热,瓶塞不可互换。(3)烧瓶、烧杯、锥形瓶不可直接加热。(4)用 pH试纸检测溶液时不能先润湿,不能用试纸直接蘸取待测液。试纸检验气体前需先湿润,试纸不能直接用手拿,要用镊子夹取。(5)药品不能入口和用手直接接触,实验剩余药品不能放回原处(K、Na等除外),不能随意丢弃,要放入指定容器中。(6)中和滴定实验中锥形瓶不能用待测液润洗。(7)温度计不能代替玻璃棒用于搅拌,测液体温度时不能与容器内壁接触。(8)量筒不能用来配制溶液或用作反应容器,更不能用来加热或量取热的溶液。4.正确选择物质分离的物理方法过滤(除去不溶物);蒸馏(分离沸点不同的液体);分液(分离互不相溶的液体);萃取(利用溶质在不同溶剂中的溶解度不同)。a ^9(H)_(3) H^9-|||-N .to vord NIO^9H^95 20NIO^+H^9-|||-.0. (H2^2HOO)H2 lOH^-ad o to ad a B v-|||-ō HO t(H2)^2H2^(200))a ^9(H)_(3) H^9-|||-N .to vord NIO^9H^95 20NIO^+H^9-|||-.0. (H2^2HOO)H2 lOH^-ad o to ad a B v-|||-ō HO t(H2)^2H2^(200))例1a ^9(H)_(3) H^9-|||-N .to vord NIO^9H^95 20NIO^+H^9-|||-.0. (H2^2HOO)H2 lOH^-ad o to ad a B v-|||-ō HO t(H2)^2H2^(200)) 基本仪器操作陷阱举例判断正误解释或说明基本仪器使用与安全(1)试管、蒸发皿既能用于给固体加热也能用于给溶液加热×蒸发皿不能用来加热固体(2)分液漏斗既能用于某些混合物的分离也能用于组装气体发生装置√分液漏斗可用于分液以及气体的制备,如实验室制备氯气,可用分液漏斗加入浓盐酸(3)称取 2.0 g NaOH 固体的实验操作是先在托盘上各放一张滤纸,然后在右盘上添加 2 g砝码,左盘上添加 NaOH 固体×NaOH具有吸水性和腐蚀性不能直接放在滤纸上(4)取液体时,先将胶头滴管伸入试剂瓶中,用手指捏紧滴管的胶头再放开手指×使用胶头滴管吸取液体时,先挤压胶头排出空气,再将胶头滴管伸入液体中吸入液体基本仪器使用与安全(5)容量瓶在使用前一定要检漏、洗涤并烘干×容量瓶在使用之前不需烘干(6)酸碱滴定实验中,用待测溶液润洗锥形瓶,以减小实验误差×锥形瓶不能用待测液润洗,否则测定结果偏大(7)酸式滴定管装标准溶液前,必须用该溶液润洗√确保滴定管中溶液的浓度与标准液的浓度相同,装液前要用所盛标准液润洗(8)金属钠着火时使用泡沫灭火器灭火×钠能与水剧烈反应产生氢气,生成的Na2O2也能与水或CO2反应药品的保存(9)可用磨口玻璃瓶保存 NaOH 溶液×玻璃中含有二氧化硅,易与 NaOH 溶液反应生成具有黏性的硅酸钠(10)氢氟酸或浓硝酸要保存在棕色细口玻璃试剂瓶中×氢氟酸能和二氧化硅反应生成四氟化硅和水,所以不能保存在玻璃瓶中,应该保存在塑料瓶中(11)保存液溴时向其中加入少量洒精,减少挥发×溴易溶于酒精,但酒精是易挥发性的物质,导致加速溴的挥发,保存液溴时常加少量水液封pH试纸使用(12)用湿润的pH 试纸测稀碱液的pH,测定值偏小√湿润的pH试纸可以稀释碱液(13)可用pH试纸测氯水的pH×氯气可与水反应生成次氯酸,次氯酸具有强氧化性,可漂白试纸(14)测定未知液的pH时,应该用干燥的pH试纸,否则一定会产生误差×若测中性溶液的pH,则不产生误差(15)直接将pH试纸浸入待测液中×直接将pH试纸浸入待测液中会污染待测液(16)用广泛pH试纸测得某溶液的pH为3.5×广泛pH试纸只能精确到整数溶液的稀释和配制(17)把水沿着器壁慢慢地注入浓硫酸中,并不断搅动×水的密度比浓硫酸的密度小,若将水倒入浓硫酸中,水会浮在浓硫酸的上面沸腾而造成液滴飞溅(18)用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小×定容时俯视容量瓶的刻度线,导致所配溶液的体积偏小,所配溶液的浓度偏大(19)用容量瓶配制溶液,定容时仰视刻度线,所配溶液浓度偏大×定容时仰视容量瓶的刻度线,导致所配溶液的体积偏大,所配溶液的浓度偏低(20)将称得的碳酸钠小心转移至250 mL容量瓶中,加入蒸馏水至刻度线×要先在烧杯中溶解,待溶液冷却到室温再转移到容量瓶中(21)将量好的浓硫酸直接转移到容量瓶中×浓硫酸要先在烧杯中稀释,待冷却到室温再转移到容量瓶中(22)将 NaOH在烧杯中溶解后,应立即将溶液转移至容量瓶中×要冷却到室温再转移到容量瓶中,否则溶液的体积偏小,浓度偏大(23)容量瓶中含有少量蒸馏水对所配的溶液无影响√定容时还要加蒸馏水,所以容量瓶中含有少量的蒸馏水对所配的溶液无影响(3)B 反应生成 C 的反应化学反应方程式是______________________。(4)C→D 反应类型是_________, D的结构简式为_______________。(5)F→G反应类型为________________。(6)I是E的同分异构体,与E 具有相同的环状结构, 写出任意一种符合下列条件的I的结构简式是__________________________。①I是三取代的环状有机物, 氯原子和羟基的取代位置与E相同;②核磁共振氢谱显示I 除了环状结构上的氢外,还有4组峰, 峰面积比3:1:1:1;③I加入NaHCO3溶液产生气体。
磷酸氯喹是一种抗疟疾药物, 研究发现,该药在细胞水平上能有效抑制新型冠状病毒的感染。其合成路线如下:
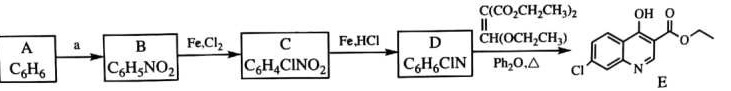
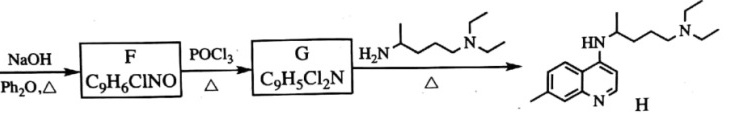
已知:
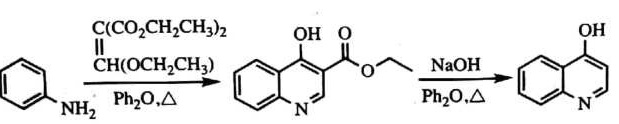
回答下列问题:
(1)A是一种芳香经, B 中官能团的名称为__________________。
(2)反应 A→B 中须加入的试剂a 为___________________。
2.熟悉常见试剂的保存
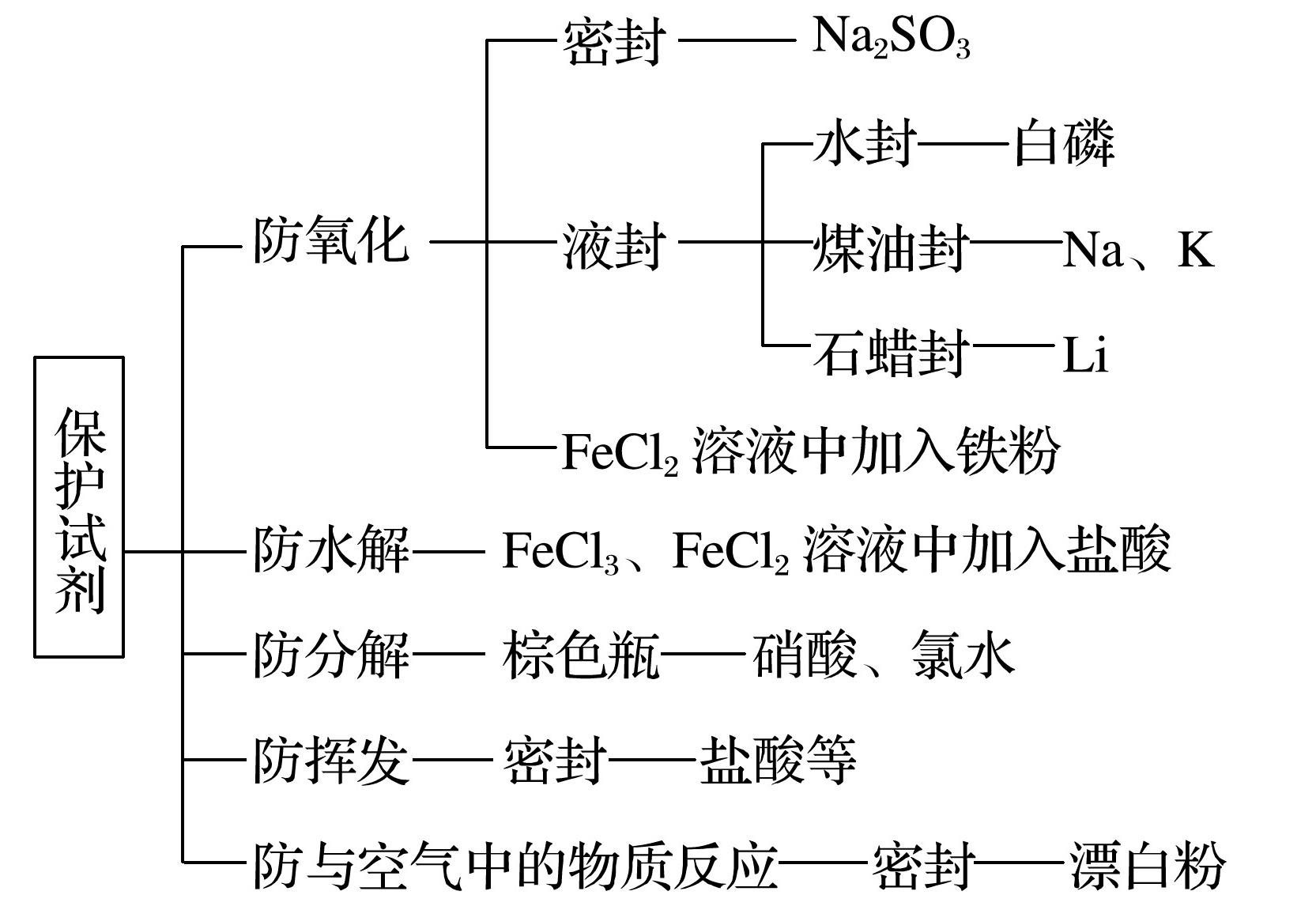

3.基本实验操作中应注意的问题归纳
(1)酸式滴定管不能装碱性溶液,碱式滴定管不能装酸性及氧化性溶液。
(2)容量瓶不能长期存放溶液,更不能作为反应容器,也不可加热,瓶塞不可互换。
(3)烧瓶、烧杯、锥形瓶不可直接加热。
(4)用 pH试纸检测溶液时不能先润湿,不能用试纸直接蘸取待测液。试纸检验气体前需先湿润,试纸不能直接用手拿,要用镊子夹取。
(5)药品不能入口和用手直接接触,实验剩余药品不能放回原处(K、Na等除外),不能随意丢弃,要放入指定容器中。
(6)中和滴定实验中锥形瓶不能用待测液润洗。
(7)温度计不能代替玻璃棒用于搅拌,测液体温度时不能与容器内壁接触。
(8)量筒不能用来配制溶液或用作反应容器,更不能用来加热或量取热的溶液。
4.正确选择物质分离的物理方法
过滤(除去不溶物);蒸馏(分离沸点不同的液体);分液(分离互不相溶的液体);萃取(利用溶质在不同溶剂中的溶解度不同)。

 例1
例1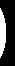 基本仪器操作陷阱
基本仪器操作陷阱
举例
判断正误
解释或说明
基本仪器使用与安全
(1)试管、蒸发皿既能用于给固体加热也能用于给溶液加热
×
蒸发皿不能用来加热固体
(2)分液漏斗既能用于某些混合物的分离也能用于组装气体发生装置
√
分液漏斗可用于分液以及气体的制备,如实验室制备氯气,可用分液漏斗加入浓盐酸
(3)称取 2.0 g NaOH 固体的实验操作是先在托盘上各放一张滤纸,然后在右盘上添加 2 g砝码,左盘上添加 NaOH 固体
×
NaOH具有吸水性和腐蚀性不能直接放在滤纸上
(4)取液体时,先将胶头滴管伸入试剂瓶中,用手指捏紧滴管的胶头再放开手指
×
使用胶头滴管吸取液体时,先挤压胶头排出空气,再将胶头滴管伸入液体中吸入液体
基本仪器使用与安全
(5)容量瓶在使用前一定要检漏、洗涤并烘干
×
容量瓶在使用之前不需烘干
(6)酸碱滴定实验中,用待测溶液润洗锥形瓶,以减小实验误差
×
锥形瓶不能用待测液润洗,否则测定结果偏大
(7)酸式滴定管装标准溶液前,必须用该溶液润洗
√
确保滴定管中溶液的浓度与标准液的浓度相同,装液前要用所盛标准液润洗
(8)金属钠着火时使用泡沫灭火器灭火
×
钠能与水剧烈反应产生氢气,生成的Na2O2也能与水或CO2反应
药品的
保存
(9)可用磨口玻璃瓶保存 NaOH 溶液
×
玻璃中含有二氧化硅,易与 NaOH 溶液反应生成具有黏性的硅酸钠
(10)氢氟酸或浓硝酸要保存在棕色细口玻璃试剂瓶中
×
氢氟酸能和二氧化硅反应生成四氟化硅和水,所以不能保存在玻璃瓶中,应该保存在塑料瓶中
(11)保存液溴时向其中加入少量洒精,减少挥发
×
溴易溶于酒精,但酒精是易挥发性的物质,导致加速溴的挥发,保存液溴时常加少量水液封
pH试
纸使用
(12)用湿润的pH 试纸测稀碱液的pH,测定值偏小
√
湿润的pH试纸可以稀释碱液
(13)可用pH试纸测氯水的pH
×
氯气可与水反应生成次氯酸,次氯酸具有强氧化性,可漂白试纸
(14)测定未知液的pH时,应该用干燥的pH试纸,否则一定会产生误差
×
若测中性溶液的pH,则不产生误差
(15)直接将pH试纸浸入待测液中
×
直接将pH试纸浸入待测液中会污染待测液
(16)用广泛pH试纸测得某溶液的pH为3.5
×
广泛pH试纸只能精确到整数
溶液的
稀释和
配制
(17)把水沿着器壁慢慢地注入浓硫酸中,并不断搅动
×
水的密度比浓硫酸的密度小,若将水倒入浓硫酸中,水会浮在浓硫酸的上面沸腾而造成液滴飞溅
(18)用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
×
定容时俯视容量瓶的刻度线,导致所配溶液的体积偏小,所配溶液的浓度偏大
(19)用容量瓶配制溶液,定容时仰视刻度线,所配溶液浓度偏大
×
定容时仰视容量瓶的刻度线,导致所配溶液的体积偏大,所配溶液的浓度偏低
(20)将称得的碳酸钠小心转移至250 mL容量瓶中,加入蒸馏水至刻度线
×
要先在烧杯中溶解,待溶液冷却到室温再转移到容量瓶中
(21)将量好的浓硫酸直接转移到容量瓶中
×
浓硫酸要先在烧杯中稀释,待冷却到室温再转移到容量瓶中
(22)将 NaOH在烧杯中溶解后,应立即将溶液转移至容量瓶中
×
要冷却到室温再转移到容量瓶中,否则溶液的体积偏小,浓度偏大
(23)容量瓶中含有少量蒸馏水对所配的溶液无影响
√
定容时还要加蒸馏水,所以容量瓶中含有少量的蒸馏水对所配的溶液无影响
(3)B 反应生成 C 的反应化学反应方程式是______________________。
(4)C→D 反应类型是_________, D的结构简式为_______________。
(5)F→G反应类型为________________。
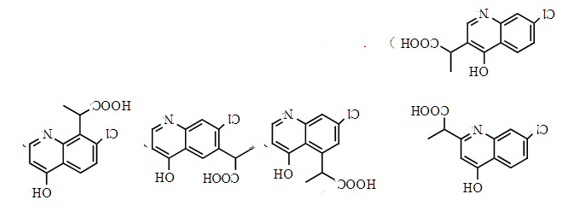
(6)I是E的同分异构体,与E 具有相同的环状结构, 写出任意一种符合下列条件的I的结构简式是__________________________。
①I是三取代的环状有机物, 氯原子和羟基的取代位置与E相同;
②核磁共振氢谱显示I 除了环状结构上的氢外,还有4组峰, 峰面积比3:1:1:1;
③I加入NaHCO3溶液产生气体。
题目解答
答案
硝基 浓硫酸、浓硝酸 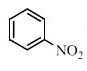 +Cl2
+Cl2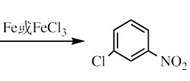 +HCl 还原反应
+HCl 还原反应 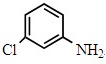 取代反应
取代反应