4.氯酸钾和亚硫酸钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图所示,已知这个反应速率随着溶液中c(H+)增大而加快。(1)反应开始进行时反应速率加快的原因是______。(2)反应后期,反应速率下降的原因是______。第二节 化学平衡1.在一定的温度下,可逆反应A(g)+3B(g)ll2C(g)达到平衡的标志是()。A.C生成速率与C分解速率相等B.A、B、C的浓度不再变化C.单位时间生成nmolA,同时生成3nmolBD.A、B、C的分子数之比为1∶3∶22.在相同条件下(T=500K),有相同体积的甲、乙两容器。甲容器中充入1gSO2和1gO2;乙容器中充入2gSO2和2gO2。下列叙述错误的是()。A.化学反应速率:乙>甲B.平衡后的浓度:乙>甲C.SO2的转化率:乙>甲D.平衡后SO2的体积分数:乙>甲3.已知氯水中有如下平衡:Cl2+H2OllHCl+HClO。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水,写出针筒中可能观察到的现象。若将此针筒长时间放置,又可能看到何种变化?试用平衡的观点加以解释?4.反应CaCO3llCaO+CO2在不同的温度下在密闭容器中达到平衡的压强如下:按要求填空:(1)若升高CaCO3分解平衡体系温度,同时缩小反应容器体积,则平衡______(填代号)。A.向左移动 B.向右移动C.不移动 D.无法确定平衡移动的方向(2)在一个与外界不能进行热交换的密闭容器中,足量的CaCO3在850℃时建立了分解平衡,若将容器扩大为原来的2倍,当重新达到平衡时,容器内的温度将______(填“升高”、“降低”、“不变”、“无法确定”),平衡时容器内的压强将______(填“大于”、“等于”、“小于”、“无法确定”)4.94×104Pa,理由是______。第三节 影响化学平衡的条件1.下列反应达到平衡时:N2(g)+3H2(g)2NH3(g)(正反应为放热反应)如果在其他条件不变时,分别改变下列条件:①增加压强,②增大N2浓度,③减小NH3的浓度,④升高温度,⑤使用催化剂,将对化学平衡有何影响?简要说明理由。2.有一化学平衡:mA(g)+nB(g)llpC(g)+qD(g)。如图2,表示的是A的转化率与压强、温度的关系。分析图中曲线可以得出的结论是()。A.正反应吸热,m+n>p+qB.正反应吸热,m+n<p+qC.正反应放热,m+n>p+qD.正反应放热,m+n<p+q3.已知工业真空炼铷的原理如下:2RbCl+MgMgCl2+2Rb(气),对于此反应的进行能给予正确解释的是()。A.铷的金属活动性不如镁强,故镁可置换铷B.铷的沸点比镁低,把铷蒸气抽出,平衡右移C.MgCl2的热稳定性不如RbCl强D.铷的单质状态较化合态更稳定4.牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:ll(1)进食后,细菌和酶作用与食物,产生有机酸,这时牙齿就受到腐蚀,其原因是______。(2)已知Ca5(PO4)3F(s)的溶解度比上面的矿产物更小,质地更坚硬。当牙膏中配有氟化物添加剂后就能防止龋齿的原因是(用离子方程式表示)______。(3)根据以上原理,请你提出一种其他促进矿化的方法______。第四节 合成氨条件的选择1.工业上合成氨,除了采用高压和催化剂,还选择500℃左右的温度,其作用是()。A.提高氨的百分含量B.提高氢气的转化率C.加快反应速率,缩短反应达到平衡的时间D.500℃左右时,催化剂的活性最大2.有平衡体系CO(g)+2H2(g)CH3OH(g)(正反应为放热反应)。为了增加甲醇的产量,工厂应采取的正确措施是()。A.高温、高压B.适宜温度、高压、催化剂C.低温、低压D.低温、高压、催化剂3.在一定条件下,气体反应N3+3H22NH3达到平衡时,在平衡混合物中NH3的体积分数为25%,则达到平衡时,气体减少的体积与反应前的体积之比是()。A.1∶2 B.1∶3 C.1∶4 D.1∶54.有甲、乙、丙三瓶新制氯水,浓度均为0.1mol·L-1,现向甲瓶中加入少量NaHCO3晶体,向乙瓶中加入少量NaHSO3晶体;丙瓶中不加入其他物质。片刻后,甲、乙、丙三瓶中c(HClO)(mol/L)间关系正确的是______,简述判断的理由______。全章训练1.NO2溶于水制HNO3的反应为:3NO2(g)+H2O(l)2HNO3(l)+NO(g)(正反应为放热反应),为了提高硝酸的产率,硝酸厂实际生产中采取的措施是()。A.升温 B.加压C.通入过量O2D.降温2.对于已达到平衡状态的可逆反应:2SO2+O22SO3(正反应为放热反应),下列叙述正确的是()。A.反应物和生成物的浓度相等B.反应物和生成物的浓度不在变化C.降低温度,平衡混合物里SO2的浓度减小D.增大压强,平衡混合物里SO2的浓度减小3.把Ca(OH)2放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2(s)llCa2++2OH-当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是()。A.溶液中Ca2+数减少B.Ca2+浓度减小C.溶液pH不变D.溶液pH增大4.在一密闭容器中,反应aA(g)bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是()。A.平衡向正反应方向移动了B.物质A的转化率减少了C.物质B的质量分数增加了D.a>b5.痛风是以关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因是在关节滑液中形成尿酸钠晶体:Ur-(aq)+Na+(aq)NaUr(s),其中Ur-表示尿酸根离子,第一次关节炎发作大都在脚趾或手指的关节处,这说明()。A.尿酸钠水溶液成酸性B.尿酸钠晶体难溶于水C.该反应为放热反应D.该反应为吸热反应6.在固定的2L密闭容器中,充入X、Y各2mol,发生可逆反应X(g)+2Y(g)ll2Z(g),并达平衡,以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如右图3,则Y的平衡浓度表示式正确的是(式中S指对应区域的面积)()。A.2—SaobB.1—SaobC.2—Sabdo D.1—Sbod7.如图4所示,烧杯甲中盛入100mL6mol·L-1HCl溶液,烧杯乙中盛入100mL冷水,现向烧杯甲中放入25gNaOH固体,同时向烧杯乙中放入25gNHNO3固体,搅拌使之溶解。(1)左瓶中气体颜色______,简述理由______。(2)右瓶中气体颜色______,简述理由______。8.某化学反应2A________3B+D在四种不同的条件下进行,B、D的起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下:根据实验数据,完成下列填空:(1)在实验1,反应在10min至20min时间平均为______mol/(L·min)。(2)设实验2的反应速率为v2,实验1的反应速率为v1,则v2______v1(填“<”、“=”、“>”)且c2______2.0mol/L(填“<”、“=”、“>”)。(3)在实验3,A的初始浓度c3=______mol/L,反应经过20min就达到平衡,可推测实验3中还隐含的条件是______。(4)比较实验4和实验1,可推测该反应的逆反应是______反应(选填吸热、放热)。理由是______。9.如图5所示,温度不变时,把某容器分割成A、B两部分,A容器体积固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2molSO3和1molN2,在相同条件下发生可逆反应:2SO2+O2________2SO3。根据下列要求写空白:(1)固定活塞位置在3处不动,达到平衡时,设A中压强为pA,B中压强为pB,则pA与pB的关系是pA______pB(填“<”、“=”、“>”)。(2)若要使A与B中平衡状态相同,可移动活塞的位置应在______处。(3)若活塞右移到5处,达到平衡后,B中SO3为xmol,A中SO3为ymol,则x和y的关系是x______y。(填“<”、“=”、“>”)。参考答案第一节1.B、D 2.C 3.(1)O2、SO2,反应速率表示单位时间浓度的变化量,O2、SO2浓度可变 (2)0.55mol/(L·s)6.6mol/L第二节1.A、B 2.D 3.气体颜色变浅,液体呈现浅黄绿色;长时间放置后,气体变为无色,有气泡生成,最后气体约为25mL。4.(1)D(2)降低;小于;体积增大,压强减小,平衡右移,根据勒夏特列原理,重新达到平衡时,压强减小,同时由于反应吸热,温度降低,重新达到平衡时,CO2的压强小于850℃时的平衡压强。第三节1.2.A3.B4.(1)有机酸与OH-反应,降低了OH-浓度,平衡右移,牙齿受到腐蚀。(2)5Ca2++3PO33-+F-=Ca5(PO4)3F↓(3)经常用含Ca2+浓度较大的水溶液漱口第四节1.C、D 2.B 3.D 4.甲>丙>乙,甲瓶氯水中H+与加入的NaHCO3反应,降低了H+浓度,使平衡Cl2+H2OllHCl+HClO右移,HClO浓度增大;乙瓶氯水中Cl2与加入的NaHSO3反应,降低了Cl2浓度,使平衡Cl2+H2OHCl+HClO左移,HClO浓度减小。全章训练1.C 2.B、C 3.A、C 4.A、C 5.C 6.B7.(1)变深,加入NaOH后,反应放热,平衡2NO2N2O4左移,颜色加深。(2)变浅,加入NH4NO3溶解吸热,平衡右移,颜色变浅。8.(1)0.026mol/(L·min) (2)>;> (3)2.0;催化剂(4)放热,升温反应物A的浓度降低9.(1)> (2)右3处(3)y>x
4.氯酸钾和亚硫酸钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图
所示,已知这个反应速率随着溶液中c(H+)增大而加快。(1)反应开始进行时反应速率加快的原因是______。(2)反应后期,反应速率下降的原因是______。第二节 化学平衡1.在一定的温度下,可逆反应A(g)+3B(g) 2C(g)达到平衡的标志是()。A.C生成速率与C分解速率相等B.A、B、C的浓度不再变化C.单位时间生成nmolA,同时生成3nmolBD.A、B、C的分子数之比为1∶3∶22.在相同条件下(T=500K),有相同体积的甲、乙两容器。甲容器中充入1gSO2和1gO2;乙容器中充入2gSO2和2gO2。下列叙述错误的是()。A.化学反应速率:乙>甲B.平衡后的浓度:乙>甲C.SO2的转化率:乙>甲D.平衡后SO2的体积分数:乙>甲3.已知氯水中有如下平衡:Cl2+H2O
2C(g)达到平衡的标志是()。A.C生成速率与C分解速率相等B.A、B、C的浓度不再变化C.单位时间生成nmolA,同时生成3nmolBD.A、B、C的分子数之比为1∶3∶22.在相同条件下(T=500K),有相同体积的甲、乙两容器。甲容器中充入1gSO2和1gO2;乙容器中充入2gSO2和2gO2。下列叙述错误的是()。A.化学反应速率:乙>甲B.平衡后的浓度:乙>甲C.SO2的转化率:乙>甲D.平衡后SO2的体积分数:乙>甲3.已知氯水中有如下平衡:Cl2+H2O HCl+HClO。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水,写出针筒中可能观察到的现象。若将此针筒长时间放置,又可能看到何种变化?试用平衡的观点加以解释?4.反应CaCO3
HCl+HClO。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水,写出针筒中可能观察到的现象。若将此针筒长时间放置,又可能看到何种变化?试用平衡的观点加以解释?4.反应CaCO3 CaO+CO2在不同的温度下在密闭容器中达到平衡的压强如下:
CaO+CO2在不同的温度下在密闭容器中达到平衡的压强如下:
按要求填空:(1)若升高CaCO3分解平衡体系温度,同时缩小反应容器体积,则平衡______(填代号)。A.向左移动 B.向右移动C.不移动 D.无法确定平衡移动的方向(2)在一个与外界不能进行热交换的密闭容器中,足量的CaCO3在850℃时建立了分解平衡,若将容器扩大为原来的2倍,当重新达到平衡时,容器内的温度将______(填“升高”、“降低”、“不变”、“无法确定”),平衡时容器内的压强将______(填“大于”、“等于”、“小于”、“无法确定”)4.94×104Pa,理由是______。第三节 影响化学平衡的条件1.下列反应达到平衡时:N2(g)+3H2(g)2NH3(g)(正反应为放热反应)如果在其他条件不变时,分别改变下列条件:①增加压强,②增大N2浓度,③减小NH3的浓度,④升高温度,⑤使用催化剂,将对化学平衡有何影响?简要说明理由。
2.有一化学平衡:mA(g)+nB(g) pC(g)+qD(g)。如图2,表示的是A的转化率与压强、温度的关系。分析图中曲线可以得出的结论是()。
pC(g)+qD(g)。如图2,表示的是A的转化率与压强、温度的关系。分析图中曲线可以得出的结论是()。
A.正反应吸热,m+n>p+qB.正反应吸热,m+n<p+qC.正反应放热,m+n>p+qD.正反应放热,m+n<p+q3.已知工业真空炼铷的原理如下:2RbCl+MgMgCl2+2Rb(气),对于此反应的进行能给予正确解释的是()。A.铷的金属活动性不如镁强,故镁可置换铷
B.铷的沸点比镁低,把铷蒸气抽出,平衡右移C.MgCl2的热稳定性不如RbCl强D.铷的单质状态较化合态更稳定4.牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡: (1)进食后,细菌和酶作用与食物,产生有机酸,这时牙齿就受到腐蚀,其原因是______。(2)已知Ca5(PO4)3F(s)的溶解度比上面的矿产物更小,质地更坚硬。当牙膏中配有氟化物添加剂后就能防止龋齿的原因是(用离子方程式表示)______。(3)根据以上原理,请你提出一种其他促进矿化的方法______。第四节 合成氨条件的选择1.工业上合成氨,除了采用高压和催化剂,还选择500℃左右的温度,其作用是()。A.提高氨的百分含量B.提高氢气的转化率C.加快反应速率,缩短反应达到平衡的时间D.500℃左右时,催化剂的活性最大2.有平衡体系CO(g)+2H2(g)CH3OH(g)(正反应为放热反应)。为了增加甲醇的产量,工厂应采取的正确措施是()。A.高温、高压B.适宜温度、高压、催化剂C.低温、低压D.低温、高压、催化剂3.在一定条件下,气体反应N3+3H22NH3达到平衡时,在平衡混合物中NH3的体积分数为25%,则达到平衡时,气体减少的体积与反应前的体积之比是()。A.1∶2 B.1∶3 C.1∶4 D.1∶54.有甲、乙、丙三瓶新制氯水,浓度均为0.1mol·L-1,现向甲瓶中加入少量NaHCO3晶体,向乙瓶中加入少量NaHSO3晶体;丙瓶中不加入其他物质。片刻后,甲、乙、丙三瓶中c(HClO)(mol/L)间关系正确的是______,简述判断的理由______。全章训练1.NO2溶于水制HNO3的反应为:3NO2(g)+H2O(l)2HNO3(l)+NO(g)(正反应为放热反应),为了提高硝酸的产率,硝酸厂实际生产中采取的措施是()。A.升温 B.加压C.通入过量O2D.降温2.对于已达到平衡状态的可逆反应:2SO2+O22SO3(正反应为放热反应),下列叙述正确的是()。A.反应物和生成物的浓度相等B.反应物和生成物的浓度不在变化C.降低温度,平衡混合物里SO2的浓度减小
(1)进食后,细菌和酶作用与食物,产生有机酸,这时牙齿就受到腐蚀,其原因是______。(2)已知Ca5(PO4)3F(s)的溶解度比上面的矿产物更小,质地更坚硬。当牙膏中配有氟化物添加剂后就能防止龋齿的原因是(用离子方程式表示)______。(3)根据以上原理,请你提出一种其他促进矿化的方法______。第四节 合成氨条件的选择1.工业上合成氨,除了采用高压和催化剂,还选择500℃左右的温度,其作用是()。A.提高氨的百分含量B.提高氢气的转化率C.加快反应速率,缩短反应达到平衡的时间D.500℃左右时,催化剂的活性最大2.有平衡体系CO(g)+2H2(g)CH3OH(g)(正反应为放热反应)。为了增加甲醇的产量,工厂应采取的正确措施是()。A.高温、高压B.适宜温度、高压、催化剂C.低温、低压D.低温、高压、催化剂3.在一定条件下,气体反应N3+3H22NH3达到平衡时,在平衡混合物中NH3的体积分数为25%,则达到平衡时,气体减少的体积与反应前的体积之比是()。A.1∶2 B.1∶3 C.1∶4 D.1∶54.有甲、乙、丙三瓶新制氯水,浓度均为0.1mol·L-1,现向甲瓶中加入少量NaHCO3晶体,向乙瓶中加入少量NaHSO3晶体;丙瓶中不加入其他物质。片刻后,甲、乙、丙三瓶中c(HClO)(mol/L)间关系正确的是______,简述判断的理由______。全章训练1.NO2溶于水制HNO3的反应为:3NO2(g)+H2O(l)2HNO3(l)+NO(g)(正反应为放热反应),为了提高硝酸的产率,硝酸厂实际生产中采取的措施是()。A.升温 B.加压C.通入过量O2D.降温2.对于已达到平衡状态的可逆反应:2SO2+O22SO3(正反应为放热反应),下列叙述正确的是()。A.反应物和生成物的浓度相等B.反应物和生成物的浓度不在变化C.降低温度,平衡混合物里SO2的浓度减小
D.增大压强,平衡混合物里SO2的浓度减小3.把Ca(OH)2放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2(s) Ca2++2OH-当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是()。A.溶液中Ca2+数减少B.Ca2+浓度减小C.溶液pH不变D.溶液pH增大4.在一密闭容器中,反应aA(g)bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是()。A.平衡向正反应方向移动了B.物质A的转化率减少了C.物质B的质量分数增加了D.a>b5.痛风是以关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因是在关节滑液中形成尿酸钠晶体:Ur-(aq)+Na+(aq)NaUr(s),其中Ur-表示尿酸根离子,第一次关节炎发作大都在脚趾或手指的关节处,这说明()。A.尿酸钠水溶液成酸性B.尿酸钠晶体难溶于水C.该反应为放热反应D.该反应为吸热反应
Ca2++2OH-当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是()。A.溶液中Ca2+数减少B.Ca2+浓度减小C.溶液pH不变D.溶液pH增大4.在一密闭容器中,反应aA(g)bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是()。A.平衡向正反应方向移动了B.物质A的转化率减少了C.物质B的质量分数增加了D.a>b5.痛风是以关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因是在关节滑液中形成尿酸钠晶体:Ur-(aq)+Na+(aq)NaUr(s),其中Ur-表示尿酸根离子,第一次关节炎发作大都在脚趾或手指的关节处,这说明()。A.尿酸钠水溶液成酸性B.尿酸钠晶体难溶于水C.该反应为放热反应D.该反应为吸热反应
6.在固定的2L密闭容器中,充入X、Y各2mol,发生可逆反应X(g)+2Y(g)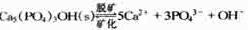 2Z(g),并达平衡,以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如右图3,则Y的平衡浓度表示式正确的是(式中S指对应区域的面积)()。A.2—SaobB.1—SaobC.2—Sabdo D.1—Sbod
2Z(g),并达平衡,以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如右图3,则Y的平衡浓度表示式正确的是(式中S指对应区域的面积)()。A.2—SaobB.1—SaobC.2—Sabdo D.1—Sbod
7.如图4所示,烧杯甲中盛入100mL6mol·L-1HCl溶液,烧杯乙中盛入100mL冷水,现向烧杯甲中放入25gNaOH固体,同时向烧杯乙中放入25gNH
NO3固体,搅拌使之溶解。(1)左瓶中气体颜色______,简述理由______。(2)右瓶中气体颜色______,简述理由______。8.某化学反应2A________3B+D在四种不同的条件下进行,B、D的起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下:根据实验数据,完成下列填空:(1)在实验1,反应在10min至20min时间平均为______mol/(L·min)。(2)设实验2的反应速率为v2,实验1的反应速率为v1,则v2______v1(填“<”、“=”、“>”)且c2______2.0mol/L(填“<”、“=”、“>”)。(3)在实验3,A的初始浓度c3=______mol/L,反应经过20min就达到平衡,可推测实验3中还隐含的条件是______。(4)比较实验4和实验1,可推测该反应的逆反应是______反应(选填吸热、放热)。理由是______。
9.如图5所示,温度不变时,把某容器分割成A、B两部分,A容器体积固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2molSO3和1molN2,在相同条件下发生可逆反应:2SO2+O2________2SO3。根据下列要求
写空白:(1)固定活塞位置在3处不动,达到平衡时,设A中压强为pA,B中压强为pB,则pA与pB的关系是pA______pB(填“<”、“=”、“>”)。(2)若要使A与B中平衡状态相同,可移动活塞的位置应在______处。(3)若活塞右移到5处,达到平衡后,B中SO3为xmol,A中SO3为ymol,则x和y的关系是x______y。(填“<”、“=”、“>”)。参考答案第一节1.B、D 2.C 3.(1)O2、SO2,反应速率表示单位时间浓度的变化量,O2、SO2浓度可变 (2)0.55mol/(L·s)6.6mol/L第二节1.A、B 2.D 3.气体颜色变浅,液体呈现浅黄绿色;长时间放置后,气体变为无色,有气泡生成,最后气体约为25mL。4.(1)D(2)降低;小于;体积增大,压强减小,平衡右移,根据勒夏特列原理,重新达到平衡时,压强减小,同时由于反应吸热,温度降低,重新达到平衡时,CO2的压强小于850℃时的平衡压强。第三节1.
2.A3.B4.(1)有机酸与OH-反应,降低了OH-浓度,
平衡右移,牙齿受到腐蚀。(2)5Ca2++3PO33-+F-=Ca5(PO4)3F↓(3)经常用含Ca2+浓度较大的水溶液漱口第四节1.C、D 2.B 3.D 4.甲>丙>乙,甲瓶氯水中H+与加入的NaHCO3反应,降低了H+浓度,使平衡Cl2+H2O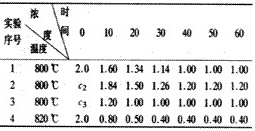 HCl+HClO右移,HClO浓度增大;乙瓶氯水中Cl2与加入的NaHSO3反应,降低了Cl2浓度,使平衡Cl2+H2OHCl+HClO左移,HClO浓度减小。全章训练1.C 2.B、C 3.A、C 4.A、C 5.C 6.B7.(1)变深,加入NaOH后,反应放热,平衡2NO2N2O4左移,颜色加深。(2)变浅,加入NH4NO3溶解吸热,平衡右移,颜色变浅。8.(1)0.026mol/(L·min) (2)>;> (3)2.0;催化剂(4)放热,升温反应物A的浓度降低9.(1)> (2)右3处(3)y>x
HCl+HClO右移,HClO浓度增大;乙瓶氯水中Cl2与加入的NaHSO3反应,降低了Cl2浓度,使平衡Cl2+H2OHCl+HClO左移,HClO浓度减小。全章训练1.C 2.B、C 3.A、C 4.A、C 5.C 6.B7.(1)变深,加入NaOH后,反应放热,平衡2NO2N2O4左移,颜色加深。(2)变浅,加入NH4NO3溶解吸热,平衡右移,颜色变浅。8.(1)0.026mol/(L·min) (2)>;> (3)2.0;催化剂(4)放热,升温反应物A的浓度降低9.(1)> (2)右3处(3)y>x
题目解答
答案