题目
10mL0.20mol/L的HAc溶液与10mL0.50mol/L的NaAc溶液混合后,计算:① 溶液的pH值;② 在混合溶液中加入1mL0.50mol/LNaOH溶液的pH值;③ 在混合溶液中加入1mL0.50mol/LHCl溶液的pH值;④ 将混合溶液稀释一倍,溶液的pH值。以上结果说明什么问题?
10mL0.20mol/L的HAc溶液与10mL0.50mol/L的NaAc溶液混合后,计算:
① 溶液的pH值;
② 在混合溶液中加入1mL0.50mol/LNaOH溶液的pH值;
③ 在混合溶液中加入1mL0.50mol/LHCl溶液的pH值;
④ 将混合溶液稀释一倍,溶液的pH值。
以上结果说明什么问题?
题目解答
答案
解: ①两溶液混合后ca = c( HAc)=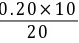 =0.1 mol/L
=0.1 mol/L
同理 cb═c( NaAc)=0.25 mol/L
HAc的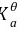 =1.75×10-5
=1.75×10-5
则[H+] ═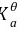
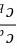 =1.75×10-5×
=1.75×10-5×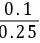 =7.0×10-6 mol/L
=7.0×10-6 mol/L
pH ═ -lg (7.0×10-6)=5.16
②加入 1 mL0.50 mol/L的NaOH的溶液后,则
ca = c(HAc)=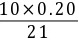 -
-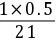 =0.07143 mol/L
=0.07143 mol/L
cb═c( NaAc)= 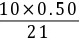 +
+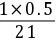 =0.2619 mol/L
=0.2619 mol/L
[H+] ═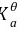
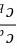 =1.75×10-5×
=1.75×10-5×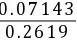 =4.773×10-6 mol/L
=4.773×10-6 mol/L
pH ═ -lg (4.773×10-6)=5.32
③加入 1 mL0.50 mol/L的HCl的溶液后,则
ca = c(HAc)=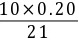 +
+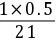 =0.1190 mol/L
=0.1190 mol/L
cb═c( NaAc)= 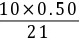 -
-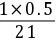 =0.2143mol/L
=0.2143mol/L
[H+] ═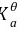
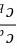 =1.75×10-5×
=1.75×10-5×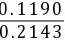 =9.718×10-6 mol/L
=9.718×10-6 mol/L
pH ═ -lg (9.718×10-6)=5.01
④将溶液稀释一倍,则,
ca =c( HAc)= 0.05 mol/L
同理 cb═c( NaAc)=0.125 mol/L
则 [H+] ═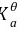
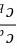 =1.75×10-5×
=1.75×10-5×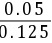 =7.0×10-6 mol/L
=7.0×10-6 mol/L
pH ═ -lg (7.0×10-6)=5.16
解析
步骤 1:计算混合溶液中HAc和NaAc的浓度
混合后总体积为20mL,HAc和NaAc的浓度分别为:
ca = c(HAc) = (0.20 mol/L * 10 mL) / 20 mL = 0.10 mol/L
cb = c(NaAc) = (0.50 mol/L * 10 mL) / 20 mL = 0.25 mol/L
步骤 2:计算混合溶液的pH值
HAc的Ka = 1.75×10^-5
[H+] = Ka * ca / cb = 1.75×10^-5 * 0.10 / 0.25 = 7.0×10^-6 mol/L
pH = -lg(7.0×10^-6) = 5.16
步骤 3:加入1mL0.50mol/LNaOH溶液后的pH值
ca = c(HAc) = (0.20 mol/L * 10 mL) / 21 mL = 0.0952 mol/L
cb = c(NaAc) = (0.50 mol/L * 10 mL + 0.50 mol/L * 1 mL) / 21 mL = 0.2619 mol/L
[H+] = Ka * ca / cb = 1.75×10^-5 * 0.0952 / 0.2619 = 4.773×10^-6 mol/L
pH = -lg(4.773×10^-6) = 5.32
步骤 4:加入1mL0.50mol/LHCl溶液后的pH值
ca = c(HAc) = (0.20 mol/L * 10 mL + 0.50 mol/L * 1 mL) / 21 mL = 0.1190 mol/L
cb = c(NaAc) = (0.50 mol/L * 10 mL - 0.50 mol/L * 1 mL) / 21 mL = 0.2143 mol/L
[H+] = Ka * ca / cb = 1.75×10^-5 * 0.1190 / 0.2143 = 9.718×10^-6 mol/L
pH = -lg(9.718×10^-6) = 5.01
步骤 5:将混合溶液稀释一倍后的pH值
ca = c(HAc) = 0.10 mol/L / 2 = 0.05 mol/L
cb = c(NaAc) = 0.25 mol/L / 2 = 0.125 mol/L
[H+] = Ka * ca / cb = 1.75×10^-5 * 0.05 / 0.125 = 7.0×10^-6 mol/L
pH = -lg(7.0×10^-6) = 5.16
步骤 6:结果说明
以上结果说明,加入少量强酸或强碱,缓冲溶液的pH值变化不大,稀释缓冲溶液,pH值基本不变。
混合后总体积为20mL,HAc和NaAc的浓度分别为:
ca = c(HAc) = (0.20 mol/L * 10 mL) / 20 mL = 0.10 mol/L
cb = c(NaAc) = (0.50 mol/L * 10 mL) / 20 mL = 0.25 mol/L
步骤 2:计算混合溶液的pH值
HAc的Ka = 1.75×10^-5
[H+] = Ka * ca / cb = 1.75×10^-5 * 0.10 / 0.25 = 7.0×10^-6 mol/L
pH = -lg(7.0×10^-6) = 5.16
步骤 3:加入1mL0.50mol/LNaOH溶液后的pH值
ca = c(HAc) = (0.20 mol/L * 10 mL) / 21 mL = 0.0952 mol/L
cb = c(NaAc) = (0.50 mol/L * 10 mL + 0.50 mol/L * 1 mL) / 21 mL = 0.2619 mol/L
[H+] = Ka * ca / cb = 1.75×10^-5 * 0.0952 / 0.2619 = 4.773×10^-6 mol/L
pH = -lg(4.773×10^-6) = 5.32
步骤 4:加入1mL0.50mol/LHCl溶液后的pH值
ca = c(HAc) = (0.20 mol/L * 10 mL + 0.50 mol/L * 1 mL) / 21 mL = 0.1190 mol/L
cb = c(NaAc) = (0.50 mol/L * 10 mL - 0.50 mol/L * 1 mL) / 21 mL = 0.2143 mol/L
[H+] = Ka * ca / cb = 1.75×10^-5 * 0.1190 / 0.2143 = 9.718×10^-6 mol/L
pH = -lg(9.718×10^-6) = 5.01
步骤 5:将混合溶液稀释一倍后的pH值
ca = c(HAc) = 0.10 mol/L / 2 = 0.05 mol/L
cb = c(NaAc) = 0.25 mol/L / 2 = 0.125 mol/L
[H+] = Ka * ca / cb = 1.75×10^-5 * 0.05 / 0.125 = 7.0×10^-6 mol/L
pH = -lg(7.0×10^-6) = 5.16
步骤 6:结果说明
以上结果说明,加入少量强酸或强碱,缓冲溶液的pH值变化不大,稀释缓冲溶液,pH值基本不变。