一试样仅含NaOH和Na2C03,一份重0.3515g试样需35.00mL 0.198 Imol-L 'HCI溶液滴定到酚猷变色,那么还 需再加人多少毫升0.1982 mol-L 'HCI溶液可达到以甲基橙为指示剂的终点?并分别计算试样中NaOH和NazCth的质 量分数 解:设NaOH含量为X% , Na2CO3含量为>% ,需V mL HC1,则s 0.13_(甲)=dfrac (|{x)_(6)-(x)_(5)|}(|{x)_(6)-(x)_(1)|}-|||-8.69-8.32-|||-=0.46,查 G 值表,G0.95 = 1.82, G0.99 = 1.94,故 8.69 应保留。Q 检验法:查 Q 值表,Qo.95 = O.64, Qo.99 = O.74,故 8.69 应保留。置信度95%时,〃 =8.47 ± 2"15=0.13(%)=岱.47 ±0.11)% , V 6置信度 99%时,u. = 8.17 ± 4・。32 二0.13(%)= (8 47 ± 0.21)%7.有一标样,其标准值为0.123%,今用一新方法测定,得四次数据如下(%): 0.112, 0.118, 0. 115, 0. 119,判 断新方法是否存在系统误差。(置信度选95%)_ |.F-/| 匚 _ |0.116 - 0.123 | 解.亍=0.116,s = 3.20X10-3 ? = 3.20x10-3查t值表,知to. 95 = 3. 18, t计算〉to.95 ,故新方法存在系统误差。8.用两种不同方法测得数据如下:9._(甲)=dfrac (|{x)_(6)-(x)_(5)|}(|{x)_(6)-(x)_(1)|}-|||-8.69-8.32-|||-=0.46,_(甲)=dfrac (|{x)_(6)-(x)_(5)|}(|{x)_(6)-(x)_(1)|}-|||-8.69-8.32-|||-=0.46,_(甲)=dfrac (|{x)_(6)-(x)_(5)|}(|{x)_(6)-(x)_(1)|}-|||-8.69-8.32-|||-=0.46,方法 1: = 6,亍 1 = 71.26%, % = 0.13%
一试样仅含NaOH和Na2C03,一份重0.3515g试样需35.00mL 0.198 Imol-L 'HCI溶液滴定到酚猷变色,那么还 需再加人多少毫升0.1982 mol-L 'HCI溶液可达到以甲基橙为指示剂的终点?并分别计算试样中NaOH和NazCth的质 量分数 解:设NaOH含量为X% , Na2CO3含量为>% ,需V mL HC1,则
s 0.13
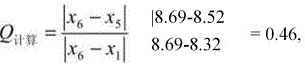 查 G 值表,G0.95 = 1.82, G0.99 = 1.94,故 8.69 应保留。Q 检验法:
查 G 值表,G0.95 = 1.82, G0.99 = 1.94,故 8.69 应保留。Q 检验法:
查 Q 值表,Qo.95 = O.64, Qo.99 = O.74,故 8.69 应保留。
置信度95%时,〃 =8.47 ± 2"15=0.13(%)=岱.47 ±0.11)% , V 6
置信度 99%时,u. = 8.17 ± 4・。32 二0.13(%)= (8 47 ± 0.21)%
7.有一标样,其标准值为0.123%,今用一新方法测定,得四次数据如下(%): 0.112, 0.118, 0. 115, 0. 119,判 断新方法是否存在系统误差。(置信度选95%)
_ |.F-//| 匚 _ |0.116 - 0.123 | 解.亍=0.116,s = 3.20X10-3 ? = 3.20x10-3
查t值表,知to. 95 = 3. 18, t计算〉to.95 ,故新方法存在系统误差。
8.用两种不同方法测得数据如下:
9.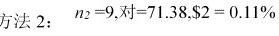
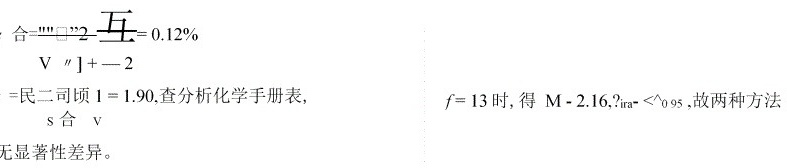
 方法 1: = 6,亍 1 = 71.26%, % = 0.13%
方法 1: = 6,亍 1 = 71.26%, % = 0.13%
题目解答
答案
解: K2SiF6+2H2O = 2KF+SiO2+4HF NaOH+HF = NaF+H2O n (SiO2) = — n (NaOH)
4
1 ,
-x 0.1477x24.72x103、 x 60.08
SiO2% = 0 100() x 100 % = 54.84%
23.欲检测贴有“3%H202”的旧瓶中002的含量,吸取瓶中溶液5.00 mL,加入过量Br?,发生下列反应:H22 + Br2 == 2Br +02 + 2H+作用10 min后,赶去过量的B.,再以0.316 2 mol-L 溶液滴定上述反应产生的H、需17.08mL达 到终点,计算瓶中H22的含量(以g / lOOmL表示)。
解:n (H2O2) = (NaOH )
0.3168 x 7.08 x 10x 34.02 x-
玦。2 的含量= 厂而 X 100 = 1.837( g/100mL )
24.有一 HCI+H3B03混合试液,吸取25.00 mL,用甲基红一漠甲酚绿指示终点,需0.199 Imol L 'NaOH溶液21.22mL, 另取25.00mL试液,加入甘露醇后,需38.74mL上述碱溶液滴定至酚猷终点,求试液中HCI与H3B03的含量,以 mg-mL'1 表示。
_ 0.1992 x 21.22 x 103、 x 36.46 x 1000 _
解:HC1的含量 = 云而 =6.165 ( mg mL-1 ) H3BO3的含量 =
01992X (38.74 - 21.22) xl03、 x 61.83x1000 ,
用相同量醋酸酊作空白试验时,需用同一浓度的NaOH溶液14.71 mL滴定所生成的酸,试计算醇的相对分子质量, 设其分子中只有一个一 OH。
解:由题义知:2n(醋酸酊)= n(NaOH)湘
2n (醋酸酣 一 n (醇)=n (NaOH)样所以, n (醇)=n (NaOH)诵—n(NaOH)样
M(醇)=0.09690 x (14.71 -10.23) =126-7
28.有一纯的(100%)未知有机酸400mg,用0. 09996mol L NaOH溶液滴定,滴定曲线表明该酸为一元酸,加入32.80 mLNaOH溶液时到达终点。当加入16.40 mL NaOH溶液时,pH为4.20。根据上述数据求:⑴酸的pKa; (2)酸的相 对分子质量;(3)如酸只含C、H、O,写出符合逻辑的经验式(本题中C=12.0、H=1.0、0=16.0)。
0.400
解.(i) m = = 122
0.3280x0.09996
当加入16.40mLNaOH时,溶液体积为V mL
0.09996 x 0.03280 - 0.01640 x 0.09996 答:金属指示剂是一类有机弱酸碱,存在着酸效应,不同pH时指示剂颜色可能不同,K5MIn不同,所以需要控制一 定的pH值范围。指示剂变色点的lgK,Min应大致等于pMep,不同的金属离子由于其稳定常数不同,其pMep也不同。 金属指示剂不象酸碱指示剂那样有一个确定的变色点。所以,同一种指示剂用于不同金属离子滴定时,适宜的pH条 件不一定相同。
6.什么是金属指示剂的封闭和僵化?如何避免?
答:指示剂-金属离子配合物稳定常数比EDTA与金属离子稳定常数大,虽加入大量EDTA也不能置换,无法达到终 点,称为指示剂的封闭,产生封闭的离子多为干扰离子。消除方法:可加入掩蔽剂来掩蔽能封闭指示剂的离子或更换 指示剂。指示剂或指示剂-金属离子配合物溶解度较小,使得指示剂与滴定剂的置换速率缓慢,使终点拖长,称为指示 剂的僵化。消除方法:可加入适当有机溶剂或加热以增大溶解度。
7.两种金属离子M和N共存时,什么条件下才可用控制酸度的方法进行分别滴定?
答:当 Cm=Cn 时,IgCM K,my= AlgK。若 ApM=±0.3, Et^±0.1%,则 AlgKN6; ApM=±0.3, Et W
±0.5%,则 lgcMK'MY^5, AlgK》5; ApM=±0.3, Et^±l%,则 IgcM K'MY^4, AlgK^4;才可用控制酸度的方法进 行分别滴定。
8.掩蔽的方法有哪些?各运用于什么场合?为防止干扰,是否在任何情况下都能使用掩蔽方法?
答:配位掩蔽法、沉淀掩蔽法、氧化还原掩蔽法。有时用掩蔽法亦无法解决问题,可用预先分离法。配位掩蔽法用于 干扰离子与掩蔽剂形成很稳定配合物时,沉淀掩蔽法用于沉淀剂能和干扰离子形成溶解度很小的沉淀时,氧化还原掩 蔽法用于氧化还原反应能使干扰离子变更价态以消除其干扰时。当存在干扰离子不能使用控制酸度方法进行滴定时才 使用掩蔽方法。
9.用EDTA滴定含有少量Fe3+的Ca2+和Mg2+«液时,用三乙醇胺、KCN都可以掩蔽Fe%抗坏血酸则不能掩蔽;在 滴定有少量Fe3+存在的Bi,+时,恰恰相反,即抗坏血酸可以掩蔽Fe3+,而三乙醇胺、KCN则不能掩蔽?请说明理由? 答:Ca2+、Mg?+滴定条件为碱性,Bi’+滴定条件为强酸性;KCN仅能用于碱性条件掩蔽Fe3+,若在酸性溶液中加入将 产生剧毒的HCN,对环境和人有严重危害,三乙醇胺须在酸性溶液中加入,然后再碱化掩蔽Fe3+,否则Fe3+将生成 氢氧化物沉淀而不能被配位掩蔽;抗坏血酸只能在酸性条件掩蔽Fe3+o
10.如何利用掩蔽和解蔽作用来测定Ni2+, Zn2 Mg2+混合溶液中各组分的含量?
答:在碱性条件下,加入过量KCN掩蔽,控制溶液pH=10.0, EBT指示剂,可用EDTA标准溶液滴定Mg2+;加入 HCHO解蔽出Z—+离子,pH=5.0, XO指示剂,可用EDTA标准溶液滴定Zn2+;另取一份溶液,调节溶液pH值在5~ 6, XO指示剂,滴定出Ni2+> Z—+总量,扣除Z—+含量,即得 皿+含量。
11.配位滴定中,在什么情况下不能采用直接滴定方式?试举例说明之?
答:不能直接滴定的条件主要有三种:(1)待测离子与EDTA配位反应速率较慢,或本身易水解,或能封闭指示剂, 如AF+、CF+等;(2)滴定反应缺乏变色敏锐的指示剂,如Ba?*、+等的滴定;(3)待测离子与EDTA不能形成配 合物或形成的配合物不稳定,如碱金属。
12.欲测定含Pb2 Af+和Mg2+试液中的Pb2+含量,共存的二种离子是否有干扰?应如何测定Pb2+含量?试拟出简 要方案。
答:logKMgY=8.69, logKPbY=18.04, logKAIY=16.3, Mg2+与 Pb2+稳定常数对数相差较大,大于 5, Mg?+不干扰;但 A「+ 与Pb2+稳定常数相差较小,有干扰作用。
测定方法:调溶液pH=5〜6,加入过量NH4F掩蔽Al3+,以二甲酚橙为指示剂,用EDTA标准溶液滴定Pb2
EDTA
Al3+ | pH=5 〜6 | aif63- | 二甲酚橙 | PbY |
Pb2+ | — | ——却2+ |
| |
Mg2+ | 过量NH F 4 | Mg2+ | aif63 |
13.若配制EDTA溶液时所用的水中含有Ca2+,则下列情况对测定结果有何影响?
(1)以CaCO3为基准物质标定EDTA溶液,用所得EDTA标准溶液滴定试液中的Z—+,以二甲酚橙为指示剂;(偏 低)
(2)以金属锌为基准物质,二甲酚橙为指示剂标定EDTA溶液。用所得EDTA标准溶液滴定试液中Ca?+的含量;(偏 高)
(3)以金属锌为基准物质,铭黑T为指示剂标定EDTA溶液。用所得EDTA标准溶液滴定试液中Ca?+的含量。(影 响不确定)
答:(1)以CaCO3为基准物质标定EDTA溶液时pH N 12.0,水中钙离子与EDTA络合,消耗部分EDTA,从公式c (EDTA) =[m/M(CaCO3)] xiO-3/V (EDTA)看出,使标定EDTD浓度偏低,而以二甲酚橙为指示剂,用所得EDTA标准溶液滴 定试液中的Zi?+时,pH=5~6,此时EDTA不与钙离子反应,因此用所得EDTA标准溶液滴定试液中的Z—+时使测 定结果偏低;(2 )以金属锌为基准物质,二甲酚橙为指示剂标定EDTA溶液时pHR5.0~6.0,水中含有的Ca?+不与EDTA 反应,标定的EDTA浓度准确,用所得EDTA标准溶液滴定试液中Ca2+的含量时pHN12.0,此时水中钙离子与EDTA 络合,消耗部分EDTA,因此用所得EDTA标准溶液滴定试液中Ca?+的含量时使测定结果偏高;(3)以金属锌为基准 物质,铭黑T为指示剂标定EDTA溶液时pHMO.O (NH3-NH4缓冲液),水中钙离子与EDTA络合,消耗部分EDTA,使 标定EDTD浓度偏低,用所得EDTA标准溶液滴定试液中Ca,+的含量时pH>12.0,此时EDTA也能与水中钙离子配 位,使测定结果与所需用的EDTA的量有关,因此对测定结果影响不确定。
14.用返滴定法测定含量时,首先在pH 3.0左右加入过量EDTA并加热,使A「+配位。试说明选择此pH的理由。 答:A1(OH)3的Ksp= 2x103、2,非常小,当pH值接近4时即可产生A1(OH)3沉淀,所以选择溶液pH=3.0左右加入过 量EDTA并加热,使A1*配位完全,然后再调节合适的pH用金属离子的标准溶液返滴定加入过量的未与AF+反应的 EDTA标准溶液。
15.今欲不经分离用配位滴定法测定下列混合溶液中各组分的含量,试设计简要方案(包括滴定剂、酸度、指示剂、 所需其他试剂以及滴定方式)。
(1)Zn2 Mg?+混合液中两者含量的测定;
(2)含有Fe‘+的试液中测定Bi3+;
(3)Fe3 Cu2 Ni?+混合液中各含量的测定;
(4)水泥中Fe3+, Af+、ca2+和Mg?+的分别测定。
答:(1) logKMgY=8.69, logKZnY=16.50, AlogK>5,可控制酸度分别滴定.
EDTA EDTA
Zn2+ pHu5〜6,六次甲基四胺 ZnY h=ioJ NH3 NH4CI MgY j
Mg2+ xo Mg2+ EBT ZnY
(2)logK Fe3+Y=25.10, logK Fe2+Y=14.33, logK BiY=27.94,把 Fe3+W化为 Fe?:则 AlogK>5,
EDTA EDTA
Bi3+ Vc Bi3+ xo Bi HNO3 Fe3^ Ssai FeY _
pe3+ pH=l~2 2+ pH=l~2 BiY A H=L5~2.
(3)logK Fe3+Y = 25.10, logK CuY=18.80, logK NiY=18.60, Ni2+^D Cu2+ 的 AlogK<5, Fe‘+和 Cu2+ 的 AlogK>5,可控制酸 度滴定Fe3+., Ni2+和Cu2+的测定须使用掩蔽和解蔽法。
EDTA | | EDTA | | |
Fe3+ | * FeY | V CuY |
Cu2+ | Ssai Cu2+ | xo NiY」 |
Ni2+ | pH =1.5 〜2 而+ pH =5.0 〜6.0 | |
测铁 | 测Ni、Cu总量 | |
EDTA标液 | ||
Fe3+ | FeF63' | FeF63 Ni2+ NiY |
Cu2+ | NH4F Cu2+ | KCN Ni(CN)/ AgNO3 Cu(CN)42- xo Cu(CN)J |