(二)化学平衡化学平衡状态“化学平衡”研究的对象是______反应——即在_____________下,既可以向_____________进行;也可以向___________进行的反应,方程式中用________符号表示。中学化学中常见的可逆反应(除水解平衡、溶解平衡)有:_____________________________________________________________________________________________________________________________________________________________________________________________________。化学平衡状态是指可逆反应在一定条件下_____________________________相等的状态(本质特征),处于化学平衡状态时,化学反应_______进行,达到该条件下反应的_____________;通常表现为某一组分的质量或浓度_______时间变化而变化,表明某一组分的______速率等于其______速率。对于一定条件下进行反应A(g)+3B(g) 3C(g) +2D(g),①若恒容,ρ(气)不变,若恒压,ρ(气)不变,②若恒容,Mr(气)不变,③若恒容,V(B)% 不变,④若生成1molA同时,消耗3molC⑤若3v(D)逆=2 v(C)正,______表明反应已达平衡状态;______表明反应已达平衡状态;______表明反应已达平衡状态;______表明反应已达平衡状态;______表明反应已达平衡状态;______表明反应已达平衡状态;对于一定条件下进行反应A(g)+4B(g) 3C(g) +2D(g),①若恒容,ρ(气)不变,若恒压,ρ(气)不变,②若恒容,Mr(气)不变,③若恒容,V(B)% 不变,④若生成4molB同时,消耗2molD⑤若v(A)正=4v(B)逆,______表明反应已达平衡状态;______表明反应已达平衡状态;______表明反应已达平衡状态;______表明反应已达平衡状态;______表明反应已达平衡状态;______表明反应已达平衡状态;化学平衡的移动根据平衡移动原理,若增加某一组分浓度,平衡向着___________________________的方向移动;若增大压强,平衡向着___________________的方向移动;若升高温度,平衡向着___________________________的方向移动;使用催化剂与否,____________________化学平衡状态。K2Cr2O7溶液中存在平衡:Cr2O2- 7(______色)+ H2O ________+ ________ (_____色),若滴入几滴浓硫酸,溶液____色加深(___向移动);若滴入几滴浓NaOH溶液,溶液____色加深(___向移动)。⑴对于已达平衡的N2 (g)+3H2 (g) 2NH3(g),若在某时刻,恒容充入一定量H2,瞬时的v正 ___v逆___;达新平衡的过程中v正 ___________、v逆_____________;原平衡_____向移动。与原平衡状态相比,在新平衡中,V(N2)%______、α(H2)_____、α( N2)_____。(2)恒容密闭容器中,充入一定量反应物A,一段时间后达平衡,再充入一定量A,移动方向利用_____________分析A的转化率①3A(g) B(g) +C(g)____向移动将再充入的A置于一假想容器中, 其建立的平衡状态与原平衡_________,然后再“加压”。与原平衡相比,反应进程①_____② A(g) B(g) +C(g)____向移动②_____③2A(g) B(g) +C(g)____向移动③_____若在恒压密闭容器中发生上述变化,则①②③的移动方向均为____向,与原平衡相比,A的转化率均_____。(3) 密闭容器中发生反应A(g)+3B(g) 2C(g) +D(g),若恒压条件下充入一定量He,平衡_________移动;若恒容条件下充入一定量He,平衡_________移动。(4)① A(g)+3B(g) 2C(g) +D(g)若向初始容积相等的甲(恒容)、乙(恒压)两容器中分别充入完全相同的反应物A、B,达平衡后,A的转化率甲____乙② A(g)+3B(g) 2C(g) +4D(g)甲____乙(5)对于已达平衡的可逆反应2NO2 (g) N2O4(g);ΔH<0。若升温,保持恒容,再达平衡后, ______[析:升温使得平衡向____移动,与原平衡相比,m气____,n气____]。(6)对于已达平衡的可逆反应,加压( )向移动有色组分的n容积V_____,,由勒夏特列原理中“_______________”可知,有色组分的c体系颜色①I2 (g) + H2 (g) 2HI(g)②2NO2 (g) N2O4(g)由此可知,加压达到平衡后,各气态组分的c与原平衡相比,均_____等效平衡一定条件下,同一个反应建立的平衡状态X平、Y平,各组分在X平、Y平中的_________________若分别相等,则X平、Y平互为等效平衡。恒容由此建立X平由此建立Y平N2 (g)+3H2 (g) 2NH3(g)1mol N23mol H2 1L1mol N23mol H2 1Lc(N2) X____ c(N2)YV(N2)% X____ V(N2)% YX平、Y平互为等效平衡N2 (g)+3H2 (g) 2NH3(g)1mol N23mol H2 1L2mol N26mol H2 2Lc(N2) X____ c(N2)YV(N2)% X____ V(N2)% YI2 (g) + H2 (g) 2HI(g)1mol I21mol H2 1L0.5mol I20.5mol H2 2Lc(I2) X____ c(I2)YV(I2)% X____ V(I2)% YⅠ、恒温,在1L容器中充入1molA和2molB,发生反应A(g)+2B(g) 2C(g),达平衡时,测得V(B)%= a ;c(B)= b mol/L,若按照以下情形在另一容器中充入起始物质,要求达平衡时也满足V(B)%= a ,恒容(1)1L,充____________molC;(2) 1L,充____________molA+1molB+____________molC (3) 0.5L,充____________molC;(4) 0.5L,充____________molA+0.2molB+____________molC(5) 2L,充___________molA+____________molB+0.8molC;(6) _______L,充___________molA+4molB+4molC;Ⅱ、恒温,在1L容器中充入1molA和4molB,发生反应A(g)+2B(g) 2C(g),达平衡时,测得V(B)%= x ;c(B)= y mol/L,若按照以下情形在另一容器中充入起始物质,要求达平衡时也满足V(B)%= x ,恒容,(1)1L容器中,充____________molA+____________molB+1.6molC(2)_______L容器中,充____________molB+0.8molCⅢ、恒温,在1L容器中充入1molA和1molB,发生反应A(g)+ B(g) 2C(g),达平衡时,测得V(B)%= m ;c(B)= nmol/L,若按照以下情形在另一容器中充入起始物质,要求达平衡时也满足V(B)%= m ,恒容(1)1L,充___________molC;(2) 1L,充______molA+1molB+_________molC;(3) 5L,充___________molC;恒压(1)充___________molA+____________molB+2molC;(2) 充____________molA+2molB+____________molCⅣ、恒温,在1L容器中充入1molA和1molB,发生反应A(g)+ B(g) 2C(g),达平衡时,测得V(B)%= m ;c(B)= nmol/L,若按照以下情形在另一容器中充入起始物质,要求达平衡时也满足c(B)= nmol/L,恒容(1) 1L,充______molA+1molB+_____molC;(2) 5L,充_______molC;恒压,充____________molA+2molB+____________molCⅤ、恒温,在1L容器中充入2molA和1molB,发生反应A(g)+ B(g) 2C(g),达平衡时,测得V(B)%= p ;c(B)= q mol/L,若按照以下情形在另一容器中充入起始物质,若要求达平衡时也满足V(B)%= p ,恒容,1L容器中,充4molA +__________molC;恒压,充____________molA+1molC化学平衡图像Ⅰ、拐点图像:横坐标为_____,纵坐标通常为表示组成、含量等物理量拐点之前的曲线表示的含义是_______________;拐点之后的曲线表示的含义是_________________。反应 A(g)+B(g) 2C(g)+3D(g) ΔH<0,(1)在图中画出1条曲线,表示60℃下体系中c(C)与时间的关系。(2) 在图中分别画出3条曲线,分别表示20MPa(有催化剂) 、20MPa(无催化剂)、10MPa(无催化剂)条件下,V(B)% 与时间的关系。Ⅱ、等温线、等压线:当曲线表示等温线时,横坐标表示______;当曲线表示等压线时,横坐标表示______。对于已达平衡的可逆反应3A(g)+xB(g) 4C(g)+ D(g) ,图a中有一条曲线,表示10℃时, B的转化率与压强的关系,由图a可知,x的取值为___________。图b中有一条曲线,表示1MPa下,B的转化率与温度的关系,由图b可知,ΔH______0。请在图a中画出一条曲线,表示70℃时,B的转化率与压强的关系。请在图b中画出一条曲线,表示2MPa下,B的转化率与温度的关系。化学平衡常数在一定温度下,一个给定的可逆反应达到平衡状态时,____________物浓度的__________与_________物浓度的_______的比值是一个常数,这个常数称为该温度下该可逆反应的化学平衡常数,用符号________表示。可逆反应CO+H2C+ H2O在150℃下反应达平衡,其化学平衡常数表达式为__________________________。t℃下,0.5L恒容容器中投入0.15mol NO2,反应达平衡时发现各组分物质的量相等,2NO2 (g) N2O4(g)在反应达平衡,该温度下化学平衡常数K=___________________。t1℃,向密闭容器中充入1mol N2和3mol H2,发生反应N2 (g)+3H2 (g) 2NH3(g),达平衡后,c(N2)、c(H2)、c(NH3)分别为a、b、c(mol/L)化学平衡常数表达式:K1=______________________,单位__________若缩小容积,达到新平衡时,化学平衡常数为K2K2与K1的关系__________________若再充入1mol NH3,达到新平衡时,化学平衡常数为K3K3与K1的关系__________________若升高温度至t2℃,达到新平衡时,化学平衡常数为K4K4与K1的关系__________________t1℃,若向密闭容器中充入0.1 mol NH3,发生反2NH3(g) N2 (g)+3H2 (g),达平衡时,化学平衡常数为K5K5与K1的关系__________________K只受_________的影响。若可逆反应ΔH<0,则升高温度,K______;降低温度,K______;反之,若可逆反应ΔH>0,则升高温度,K______;降低温度,K______。化学平衡常数的应用:①一般地,K >______时,认为反应进行得基本完全了;②同一个反应在不同条件下,K值越大,表示反应进行得越________,反应物转化率越_____;③2L恒容密闭容器中,可逆反应CO+H2C+ H2O在150℃下已达平衡,各组分物质的量均为1mol;(a)若保持恒温、恒容,同时将各组分物质的量增加至原来的2倍,则平衡将_____移动。( )A. B. C. K的计算方式,将各组分的即时浓度带入计算所得的结果用Qc表示。若Qc<K,表示平衡将_____移动;若Qc>K,表示平衡将_____移动。 D. 化学反应进行的方向 E. ________(符号S)来量度混乱(无序)的程度。同一物质,由固态转变为液态,进而转变为________态;一个由固体或液体参加的化学反应中,有气态物质生成(或反应物气体计量数之和_______生成物气体计量数之和);这些过程都表现为熵______。 F. <0,_________________;若ΔG >0,_________________;若ΔG =0,________________。 G. H______0且ΔS ___0 ,则该反应需在较______温度下反应才具有自发性。 H______0且ΔS ___0 ,T无论取何值,ΔG 始终______0,意味着该反应的自发性不受温度高低的影响。 O2C+O,ΔH______0且ΔS ___0 ,无论T取何值,ΔG 始终________0,即使在高温下,反应__________自发性。 ____________________的,但若从外界输入能量,该过程可以发生。过程的自发性只能用于判断过程的______,不能确定过程是否___________和过程发生的____________。
(二)化学平衡
化学平衡状态
“化学平衡”研究的对象是______反应——即在_____________下,既可以向_____________进行;也可以向___________进行的反应,方程式中用________符号表示。中学化学中常见的可逆反应(除水解平衡、溶解平衡)有:
___________________________________________________________________________________________________
__________________________________________________________________________________________________。
化学平衡状态是指可逆反应在一定条件下_____________________________相等的状态(本质特征),处于化学平衡状态时,化学反应_______进行,达到该条件下反应的_____________;通常表现为某一组分的质量或浓度_______时间变化而变化,表明某一组分的______速率等于其______速率。
对于一定条件下进行反应A(g)+3B(g) 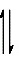 3C(g) +2D(g),
3C(g) +2D(g),
①若恒容,ρ(气)不变,
若恒压,ρ(气)不变,
②若恒容,Mr(气)不变,
③若恒容,V(B)% 不变,
④若生成1molA同时,消耗3molC
⑤若3v(D)逆=2 v(C)正,
______表明反应已达平衡状态;
______表明反应已达平衡状态;
______表明反应已达平衡状态;
______表明反应已达平衡状态;
______表明反应已达平衡状态;
______表明反应已达平衡状态;
对于一定条件下进行反应A(g)+4B(g) 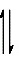 3C(g) +2D(g),
3C(g) +2D(g),
①若恒容,ρ(气)不变,
若恒压,ρ(气)不变,
②若恒容,Mr(气)不变,
③若恒容,V(B)% 不变,
④若生成4molB同时,消耗2molD
⑤若v(A)正=4v(B)逆,
______表明反应已达平衡状态;
______表明反应已达平衡状态;
______表明反应已达平衡状态;
______表明反应已达平衡状态;
______表明反应已达平衡状态;
______表明反应已达平衡状态;
化学平衡的移动
根据平衡移动原理,若增加某一组分浓度,平衡向着___________________________的方向移动;若增大压强,平衡向着___________________的方向移动;若升高温度,平衡向着___________________________的方向移动;使用催化剂与否,____________________化学平衡状态。
K2Cr2O7溶液中存在平衡:Cr2O2- 7(______色)+ H2O  ________+ ________ (_____色),若滴入几滴浓硫酸,溶液____色加深(___向移动);若滴入几滴浓NaOH溶液,溶液____色加深(___向移动)。
________+ ________ (_____色),若滴入几滴浓硫酸,溶液____色加深(___向移动);若滴入几滴浓NaOH溶液,溶液____色加深(___向移动)。
⑴对于已达平衡的N2 (g)+3H2 (g) 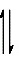 2NH3(g),若在某时刻,恒容充入一定量H2,瞬时的v正 ___v逆___;达新平衡的过程中v正 ___________、v逆_____________;原平衡_____向移动。与原平衡状态相比,在新平衡中,V(N2)%______、α(H2)_____、α( N2)_____。
2NH3(g),若在某时刻,恒容充入一定量H2,瞬时的v正 ___v逆___;达新平衡的过程中v正 ___________、v逆_____________;原平衡_____向移动。与原平衡状态相比,在新平衡中,V(N2)%______、α(H2)_____、α( N2)_____。
(2)恒容密闭容器中,充入一定量反应物A,一段时间后达平衡,再充入一定量A,
移动方向
利用_____________分析
A的转化率
①3A(g) B(g) +C(g)
____向移动
将再充入的A置于一假想容器中, 其建立的平衡状态与原平衡_________,然后再“加压”。与原平衡相比,反应进程
①_____
② A(g) B(g) +C(g)
____向移动
②_____
③2A(g) B(g) +C(g)
____向移动
③_____
若在恒压密闭容器中发生上述变化,则①②③的移动方向均为____向,与原平衡相比,A的转化率均_____。
(3) 密闭容器中发生反应A(g)+3B(g) 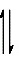 2C(g) +D(g),若恒压条件下充入一定量He,平衡_________移动;若恒容条件下充入一定量He,平衡_________移动。
2C(g) +D(g),若恒压条件下充入一定量He,平衡_________移动;若恒容条件下充入一定量He,平衡_________移动。
(4)
① A(g)+3B(g) 2C(g) +D(g)
若向初始容积相等的甲(恒容)、乙(恒压)两容器中分别充入完全相同的反应物A、B,达平衡后,
A的
转化率
甲____乙
② A(g)+3B(g) 2C(g) +4D(g)
甲____乙
(5)对于已达平衡的可逆反应2NO2 (g) 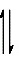 N2O4(g);ΔH<0。若升温,保持恒容,再达平衡后,
N2O4(g);ΔH<0。若升温,保持恒容,再达平衡后,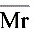 ______[析:升温使得平衡向____移动,与原平衡相比,m气____,n气____]。
______[析:升温使得平衡向____移动,与原平衡相比,m气____,n气____]。
(6)对于已达平衡的可逆反应,加压
( )向
移动
有色组分的
n
容积V_____,,由勒夏特列原理中“_______________”可知,有色组分的c
体系
颜色
①I2 (g) + H2 (g) 2HI(g)
②2NO2 (g) N2O4(g)
由此可知,加压达到平衡后,各气态组分的c与原平衡相比,均_____
等效平衡
一定条件下,同一个反应建立的平衡状态X平、Y平,各组分在X平、Y平中的_________________若分别相等,则X平、Y平互为等效平衡。
恒容
由此建立X平
由此建立Y平
N2 (g)+3H2 (g) 2NH3(g)
1mol N2
3mol H2 1L
1mol N2
3mol H2 1L
c(N2) X____ c(N2)Y
V(N2)% X____ V(N2)% Y
X平、Y平互为
等效平衡
N2 (g)+3H2 (g) 2NH3(g)
1mol N2
3mol H2 1L
2mol N2
6mol H2 2L
c(N2) X____ c(N2)Y
V(N2)% X____ V(N2)% Y
I2 (g) + H2 (g) 2HI(g)
1mol I2
1mol H2 1L
0.5mol I2
0.5mol H2 2L
c(I2) X____ c(I2)Y
V(I2)% X____ V(I2)% Y
Ⅰ、
恒温,在1L容器中充入1molA和2molB,发生反应A(g)+2B(g) 2C(g),达平衡时,测得V(B)%= a ;c(B)= b mol/L,若按照以下情形在另一容器中充入起始物质,要求达平衡时也满足V(B)%= a ,
恒容(1)1L,充____________molC;(2) 1L,充____________molA+1molB+____________molC
(3) 0.5L,充____________molC;(4) 0.5L,充____________molA+0.2molB+____________molC
(5) 2L,充___________molA+____________molB+0.8molC;
(6) _______L,充___________molA+4molB+4molC;
Ⅱ、
恒温,在1L容器中充入1molA和4molB,发生反应A(g)+2B(g) 2C(g),达平衡时,测得V(B)%= x ;c(B)= y mol/L,若按照以下情形在另一容器中充入起始物质,要求达平衡时也满足V(B)%= x ,
恒容,(1)1L容器中,充____________molA+____________molB+1.6molC
(2)_______L容器中,充____________molB+0.8molC
Ⅲ、
恒温,在1L容器中充入1molA和1molB,发生反应A(g)+ B(g) 2C(g),达平衡时,测得V(B)%= m ;c(B)= nmol/L,若按照以下情形在另一容器中充入起始物质,要求达平衡时也满足V(B)%= m ,
恒容(1)1L,充___________molC;(2) 1L,充______molA+1molB+_________molC;(3) 5L,充___________molC;
恒压(1)充___________molA+____________molB+2molC;(2) 充____________molA+2molB+____________molC
Ⅳ、
恒温,在1L容器中充入1molA和1molB,发生反应A(g)+ B(g) 2C(g),达平衡时,测得V(B)%= m ;c(B)= nmol/L,若按照以下情形在另一容器中充入起始物质,要求达平衡时也满足c(B)= nmol/L,
恒容(1) 1L,充______molA+1molB+_____molC;(2) 5L,充_______molC;
恒压,充____________molA+2molB+____________molC
Ⅴ、
恒温,在1L容器中充入2molA和1molB,发生反应A(g)+ B(g) 2C(g),达平衡时,测得V(B)%= p ;c(B)= q mol/L,若按照以下情形在另一容器中充入起始物质,若要求达平衡时也满足V(B)%= p ,
恒容,1L容器中,充4molA +__________molC;
恒压,充____________molA+1molC
 化学平衡图像
化学平衡图像
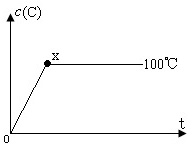
Ⅰ、拐点图像:横坐标为_____,纵坐标通常为表示组成、含量等物理量拐点之前
的曲线表示的含义是_______________;拐点之后的曲线表示的含义是_________________。
反应 A(g)+B(g) 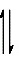 2C(g)+3D(g) ΔH<0,(1)在图中画出1条曲线,表示60℃下体系中c(C)与时间的关系。
2C(g)+3D(g) ΔH<0,(1)在图中画出1条曲线,表示60℃下体系中c(C)与时间的关系。
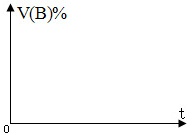 (2) 在图中分别画出3条曲线,分别表示20MPa(有催化剂) 、20MPa(无催化剂)、
(2) 在图中分别画出3条曲线,分别表示20MPa(有催化剂) 、20MPa(无催化剂)、
10MPa(无催化剂)条件下,V(B)% 与时间的关系。
Ⅱ、等温线、等压线:当曲线表示等温线时,横坐标表示______;当曲线
 表示等压线时,横坐标表示______。
表示等压线时,横坐标表示______。
对于已达平衡的可逆反应3A(g)+xB(g) 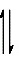 4C(g)+ D(g) ,
4C(g)+ D(g) ,
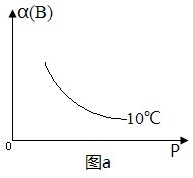
图a中有一条曲线,表示10℃时, B的转化率与压强的关系,由图a可知,
x的取值为___________。
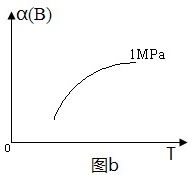 图b中有一条曲线,表示1MPa下,B的转化率与温度的关系,由图b可知,
图b中有一条曲线,表示1MPa下,B的转化率与温度的关系,由图b可知,
ΔH______0。
请在图a中画出一条曲线,表示70℃时,B的转化率与压强的关系。
请在图b中画出一条曲线,表示2MPa下,B的转化率与温度的关系。
化学平衡常数
在一定温度下,一个给定的可逆反应达到平衡状态时,____________物浓度的__________与_________物浓度的_______的比值是一个常数,这个常数称为该温度下该可逆反应的化学平衡常数,用符号________表示。
可逆反应CO+H2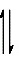 C+ H2O在150℃下反应达平衡,其化学平衡常数表达式为__________________________。t℃下,0.5L恒容容器中投入0.15mol NO2,反应达平衡时发现各组分物质的量相等,2NO2 (g)
C+ H2O在150℃下反应达平衡,其化学平衡常数表达式为__________________________。t℃下,0.5L恒容容器中投入0.15mol NO2,反应达平衡时发现各组分物质的量相等,2NO2 (g) 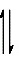 N2O4(g)在反应达平衡,该温度下化学平衡常数K=___________________。
N2O4(g)在反应达平衡,该温度下化学平衡常数K=___________________。
t1℃,向密闭容器中充入1mol N2和3mol H2,发生反应N2 (g)+3H2 (g) 2NH3(g),达平衡后,c(N2)、c(H2)、c(NH3)分别为a、b、c(mol/L)
化学平衡常数表达式:
K1=______________________,单位__________
若缩小容积,达到新平衡时,化学平衡常数为K2
K2与K1的关系__________________
若再充入1mol NH3,达到新平衡时,化学平衡常数为K3
K3与K1的关系__________________
若升高温度至t2℃,达到新平衡时,化学平衡常数为K4
K4与K1的关系__________________
t1℃,若向密闭容器中充入0.1 mol NH3,发生反2NH3(g)
N2 (g)+3H2 (g),达平衡时,化学平衡常数为K5
K5与K1的关系__________________
K只受_________的影响。若可逆反应ΔH<0,则升高温度,K______;降低温度,K______;反之,若可逆反应ΔH>0,则升高温度,K______;降低温度,K______。
化学平衡常数的应用:①一般地,K >______时,认为反应进行得基本完全了;
②同一个反应在不同条件下,K值越大,表示反应进行得越________,反应物转化率越_____;
③2L恒容密闭容器中,可逆反应CO+H2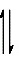 C+ H2O在150℃下已达平衡,各组分物质的量均为1mol;(a)若保持恒温、恒容,同时将各组分物质的量增加至原来的2倍,则平衡将_____移动。( )
C+ H2O在150℃下已达平衡,各组分物质的量均为1mol;(a)若保持恒温、恒容,同时将各组分物质的量增加至原来的2倍,则平衡将_____移动。( )
B.
C. K的计算方式,将各组分的即时浓度带入计算所得的结果用Qc表示。若Qc<K,表示平衡将_____移动;若Qc>K,表示平衡将_____移动。
D. 化学反应进行的方向
E. ________(符号S)来量度混乱(无序)的程度。同一物质,由固态转变为液态,进而转变为________态;一个由固体或液体参加的化学反应中,有气态物质生成(或反应物气体计量数之和_______生成物气体计量数之和);这些过程都表现为熵______。
F. <0,_________________;若ΔG >0,_________________;若ΔG =0,________________。
G. H______0且ΔS ___0 ,则该反应需在较______温度下反应才具有自发性。
H______0且ΔS ___0 ,T无论取何值,ΔG 始终______0,意味着该反应的自发性不受温度高低的影响。
O
 2C+O,ΔH______0且ΔS ___0 ,无论T取何值,ΔG 始终________0,即使在高温下,反应__________自发性。
2C+O,ΔH______0且ΔS ___0 ,无论T取何值,ΔG 始终________0,即使在高温下,反应__________自发性。____________________的,但若从外界输入能量,该过程可以发生。过程的自发性只能用于判断过程的______,不能确定过程是否___________和过程发生的____________。
题目解答
答案
b