题目
[例 https:/img.zuoyebang.cc/zyb_505822fd3f5f457e812d1927b5429633.jpg-81 表 1-11 所示为 Fe-Cu 系在1873K时铜以纯物质为标准态的活度。试计-|||-算铜以假想纯物质和质量1%溶液为标准态的活度。-|||-表 1-11 Fe-Cu 系中Cu的活度(a Cu(R))-|||-x[Cu] 0.015 0.025 0.061 0.217 0.467 0.626 0.792 1.000-|||-aCu(R) 0.119 0.1823 0.424 0.730 0.820 0.870 0.888 1.00
题目解答
答案
解析
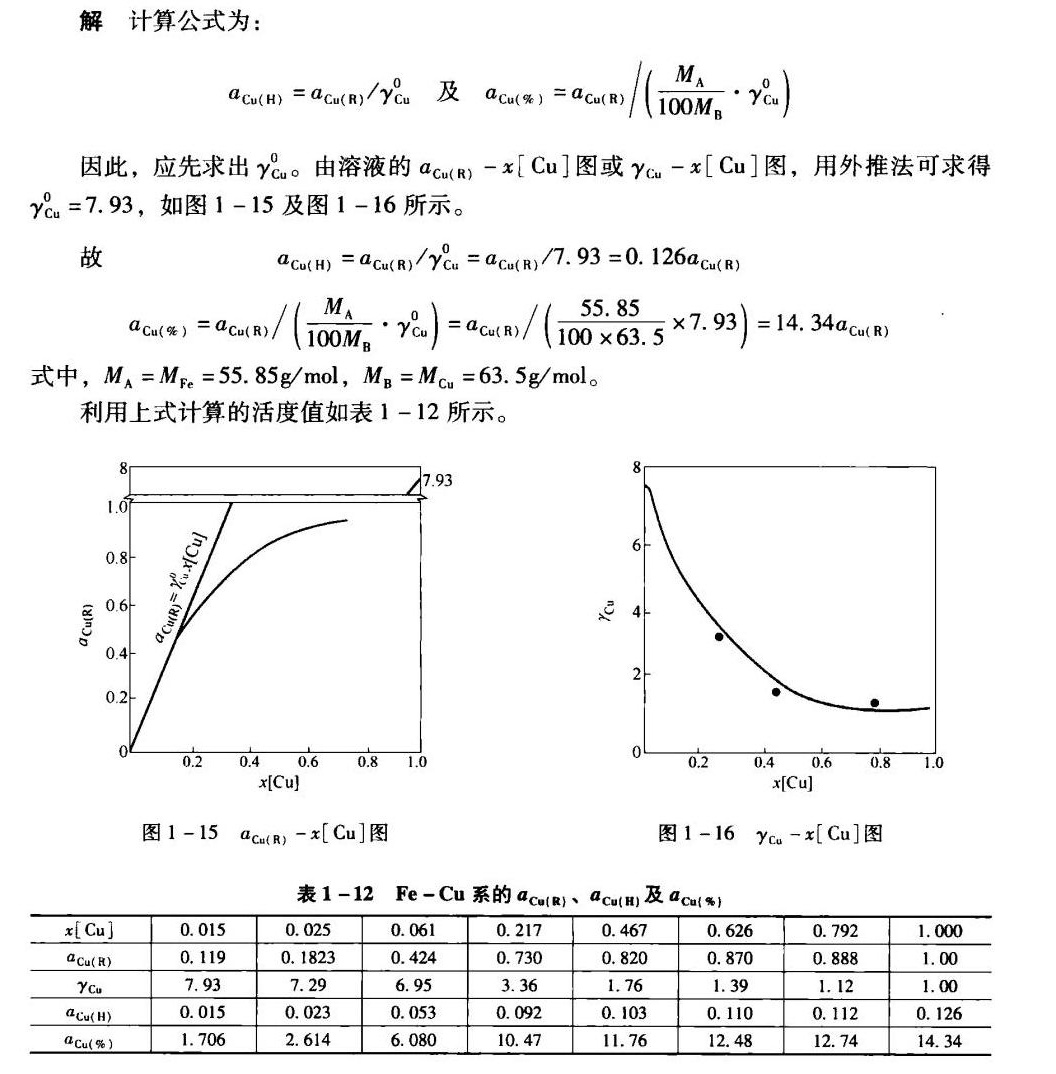
步骤 1:计算铜以假想纯物质为标准态的活度
根据题目,铜以纯物质为标准态的活度为 $a_{Cu}(R)$。假想纯物质的活度 $a_{Cu}(H)$ 可以通过以下公式计算:
$$
a_{Cu}(H) = \frac{a_{Cu}(R)}{y_{Cu}}
$$
其中,$y_{Cu}$ 是铜的摩尔分数。根据题目,$y_{Cu}$ 可以通过以下公式计算:
$$
y_{Cu} = \frac{x_{Cu} \cdot M_{Fe}}{x_{Cu} \cdot M_{Fe} + (1 - x_{Cu}) \cdot M_{Cu}}
$$
其中,$x_{Cu}$ 是铜的质量分数,$M_{Fe}$ 和 $M_{Cu}$ 分别是铁和铜的摩尔质量。
步骤 2:计算铜以质量1%溶液为标准态的活度
铜以质量1%溶液为标准态的活度 $a_{Cu}(\%)$ 可以通过以下公式计算:
$$
a_{Cu}(\%) = \frac{a_{Cu}(R)}{y_{Cu}^{0.01}}
$$
其中,$y_{Cu}^{0.01}$ 是铜在质量1%溶液中的摩尔分数。根据题目,$y_{Cu}^{0.01}$ 可以通过以下公式计算:
$$
y_{Cu}^{0.01} = \frac{0.01 \cdot M_{Fe}}{0.01 \cdot M_{Fe} + 0.99 \cdot M_{Cu}}
$$
步骤 3:计算并列出结果
根据上述公式,计算出铜以假想纯物质和质量1%溶液为标准态的活度,并列出结果。
根据题目,铜以纯物质为标准态的活度为 $a_{Cu}(R)$。假想纯物质的活度 $a_{Cu}(H)$ 可以通过以下公式计算:
$$
a_{Cu}(H) = \frac{a_{Cu}(R)}{y_{Cu}}
$$
其中,$y_{Cu}$ 是铜的摩尔分数。根据题目,$y_{Cu}$ 可以通过以下公式计算:
$$
y_{Cu} = \frac{x_{Cu} \cdot M_{Fe}}{x_{Cu} \cdot M_{Fe} + (1 - x_{Cu}) \cdot M_{Cu}}
$$
其中,$x_{Cu}$ 是铜的质量分数,$M_{Fe}$ 和 $M_{Cu}$ 分别是铁和铜的摩尔质量。
步骤 2:计算铜以质量1%溶液为标准态的活度
铜以质量1%溶液为标准态的活度 $a_{Cu}(\%)$ 可以通过以下公式计算:
$$
a_{Cu}(\%) = \frac{a_{Cu}(R)}{y_{Cu}^{0.01}}
$$
其中,$y_{Cu}^{0.01}$ 是铜在质量1%溶液中的摩尔分数。根据题目,$y_{Cu}^{0.01}$ 可以通过以下公式计算:
$$
y_{Cu}^{0.01} = \frac{0.01 \cdot M_{Fe}}{0.01 \cdot M_{Fe} + 0.99 \cdot M_{Cu}}
$$
步骤 3:计算并列出结果
根据上述公式,计算出铜以假想纯物质和质量1%溶液为标准态的活度,并列出结果。