题目
有H2、CH4、的混合气体气体25.0mL,加入过量的氧气燃烧,体积缩减了35.0mL,生成二氧化碳体积17.0mL,求混合气中各组分体积分数。
有H2、CH4、的混合气体气体25.0mL,加入过量的氧气燃烧,体积缩减了35.0mL,生成二氧化碳体积17.0mL,求混合气中各组分体积分数。
题目解答
答案
解: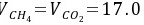
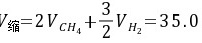
得 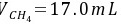
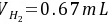
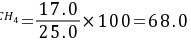
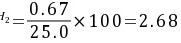
解析
步骤 1:确定甲烷的体积
根据题目,生成的二氧化碳体积为17.0mL,由于甲烷燃烧生成二氧化碳的化学方程式为:
\[ CH_4 + 2O_2 \rightarrow CO_2 + 2H_2O \]
因此,生成的二氧化碳体积等于甲烷的体积,即:
\[ V_{CH_4} = 17.0mL \]
步骤 2:确定氢气的体积
根据题目,混合气体总体积为25.0mL,其中甲烷的体积为17.0mL,因此氢气的体积为:
\[ V_{H_2} = 25.0mL - 17.0mL = 8.0mL \]
步骤 3:计算体积分数
甲烷的体积分数为:
\[ \phi_{CH_4} = \frac{V_{CH_4}}{V_{总}} \times 100\% = \frac{17.0mL}{25.0mL} \times 100\% = 68.0\% \]
氢气的体积分数为:
\[ \phi_{H_2} = \frac{V_{H_2}}{V_{总}} \times 100\% = \frac{8.0mL}{25.0mL} \times 100\% = 32.0\% \]
根据题目,生成的二氧化碳体积为17.0mL,由于甲烷燃烧生成二氧化碳的化学方程式为:
\[ CH_4 + 2O_2 \rightarrow CO_2 + 2H_2O \]
因此,生成的二氧化碳体积等于甲烷的体积,即:
\[ V_{CH_4} = 17.0mL \]
步骤 2:确定氢气的体积
根据题目,混合气体总体积为25.0mL,其中甲烷的体积为17.0mL,因此氢气的体积为:
\[ V_{H_2} = 25.0mL - 17.0mL = 8.0mL \]
步骤 3:计算体积分数
甲烷的体积分数为:
\[ \phi_{CH_4} = \frac{V_{CH_4}}{V_{总}} \times 100\% = \frac{17.0mL}{25.0mL} \times 100\% = 68.0\% \]
氢气的体积分数为:
\[ \phi_{H_2} = \frac{V_{H_2}}{V_{总}} \times 100\% = \frac{8.0mL}{25.0mL} \times 100\% = 32.0\% \]